解题方法
1 . 部分含钠或硫的“价类二维图”如下图所示。下列推断合理的是

| A.b、c均具有还原性 | B.d、g、h中均存在共价键 |
| C.a可与氧气一步生成d或e | D.f一定可用做膨松剂 |
您最近一年使用:0次
2 . 化学助力蓝天保卫战。工业上可利用氨水吸收SO2尾气,生成NH4HSO3,再将其氧化得到(NH4)2SO4化肥。设NA为阿伏加德罗常数的值,下列说法正确的是
| A.22.4LNH3所含的分子数目为NA |
| B.64gSO2中所含的σ键数目为2NA |
C.2mol 完全氧化生成 完全氧化生成 ,转移的电子数目为2NA ,转移的电子数目为2NA |
D.1L0.1mol/L(NH4)2SO4溶液中所含的 数目为0.2NA 数目为0.2NA |
您最近一年使用:0次
解题方法
3 . 光催化氧化甲烷制甲醛的机理如图所示。设NA为阿伏加德罗常数的值。下列说法不正确的是
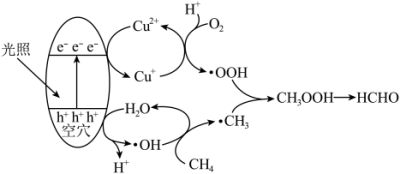
A.在光催化剂表面会发生反应 |
| B.CH3OOH为中间产物 |
| C.上述过程中有非极性键的断裂与生成 |
| D.每生成30 g HCHO,总反应转移电子数目为4NA |
您最近一年使用:0次
名校
解题方法
4 . X、Y、Z、W、E均为短周期主族元素,原子序数依次增大,且E与其他元素均不在同一周期。这五种元素组成的一种化合物的结构如图所示。下列说法不正确的是
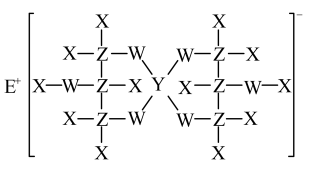

| A.W和E形成的化合物中可能存在共价键 |
| B.第一电离能:W>Z>Y |
| C.沸点:EX>X2W>ZX4 |
| D.Y的氟化物YF3中所有原子均为8电子稳定结构 |
您最近一年使用:0次
2023-04-28更新
|
793次组卷
|
3卷引用:广东省2022-2023学年高三下学期二模考试化学试题
名校
解题方法
5 . 六氟磷酸盐离子液体可用于有机合成的溶剂和催化剂,其结构如图所示,下列说法错误的是
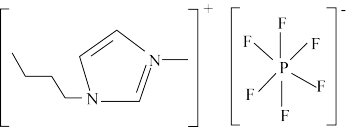

A.阳离子中碳原子有 和 和 两种杂化方式 两种杂化方式 |
| B.阴、阳离子体积较大,离子之间作用力较弱,晶体的熔点较低 |
| C.该物质中存在的化学键类型:离子键、共价键 |
| D.所有原子均符合8电子稳定结构 |
您最近一年使用:0次
2023-04-27更新
|
1105次组卷
|
2卷引用:广东省大湾区2023届普通高中毕业班下学期联合模拟考试(二)化学试题
名校
解题方法
6 . W、Y、Z为原子序数依次增大的短周期元素,Y原子序数为W原子最外层电子数的3倍,由这三种元素构成的某物质结构如图所示。下列说法错误的是
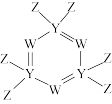

| A.Y的最高价氧化物的水化物是弱酸 |
| B.Z、W和氢三种元素可形成既有离子键又有共价键的化合物 |
C.Z的简单氢化物可用于刻蚀玻璃,其电子式可表示为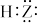 |
| D.最简单氢化物的沸点:W>Y |
您最近一年使用:0次
2022-02-24更新
|
628次组卷
|
3卷引用:广东省(梅县东山中学 广州五中 珠海二中 佛山三中)四校2021-2022学年高三下学期第二次联考化学试题
广东省(梅县东山中学 广州五中 珠海二中 佛山三中)四校2021-2022学年高三下学期第二次联考化学试题广东省四校2022届高三第二次联考化学试卷(已下线)押广东卷化学第13题 元素周期律-备战2022年高考化学临考题号押题
名校
解题方法
7 . 半导体工业中用到多种化学试剂及材料,下列有关说法正确的是
| A.一种光刻胶所含的聚乙烯醇月桂酸酯属于有机高分子材料 |
| B.刻蚀二氧化硅的HF和NH4F所含化学键类型相同 |
| C.清洗半导体硅片用的去离子水适合长期饮用 |
| D.半导体材料氮化镓(GaN)属于合金 |
您最近一年使用:0次
2022-01-25更新
|
305次组卷
|
3卷引用:广东省梅州市丰顺县和五华县2022届高三1月质检(一模)化学试题
名校
解题方法
8 . 短周期主族元素X、Y、Z、W原子序数依次增大,四种元素组成的一种食品添加剂结构如图所示,Z的原子半径在短周期中最大,W基态原子的s能级电子总数是p能级电子总数的2/3。
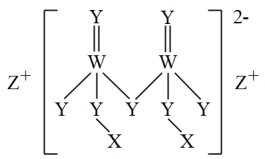
下列说法不正确的是

下列说法不正确的是
| A.Y、Z形成的简单离子半径: Y> Z |
| B.W、Y形成的简单氢化物沸点: Y > W |
| C.Z分别与X、Y形成的化合物中所含化学键类型一定完全相同 |
| D.WX3、X2Y中W原子和Y原子的杂化轨道类型相同 |
您最近一年使用:0次
2022-01-22更新
|
1060次组卷
|
8卷引用:广东省梅州市梅江区梅州中学2022-2023学年高三上学期8月阶段性考试化学试题
解题方法
9 . 元素周期表第IIIA族包括B、Al、Ga等元素,它们参与形成的化合物有重要研究和应用价值,回答下列问题:
(1)Ga原子的价电子排布式为___________ ;Ga、As和Se的第一电离能由小到大的顺序是___________ 。
(2)实验发现,氯化铝的蒸气或溶于非极性溶剂中或处于熔融状态时,都以二聚态(Al2Cl6)形式存在。其球棍模型如图所示。
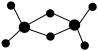
①该分子中Al原子采取___________ 杂化。
②Al2Cl6与过量NaOH溶液反应生成Na[Al(OH)4],[Al(OH)4]-中存在的化学作用力类型有___________ (填标号)。
A.离子键 B.极性共价键 C.金属键 D.非极性共价键 E.配位键 F.σ键 G.氢键
(3)更高温度下Al2Cl6二聚体则离解成AlCl3,BF3是AlCl3的一种等电子体,结合价层电子对互斥理论判断,BF3的分子构型为___________ 。
(4)GaN是第三代半导体材料的研究热点,在干燥的NH3气流中焙烧磨细的GaAs可制得GaN。GaN熔点约为1500℃,GaAs熔点为1238℃,GaN熔点高于GaAs的原因是___________ 。
(5)GaN的其中一种晶胞结构如图所示,与金刚石的晶体结构高度相似。该晶胞中Ga原子处于N原子形成的___________ (填“正四面体形” 或“正八面体形”)空隙。已知GaN的密度为ρ g/cm3,Ga和As的摩尔质量分别为a g/mol和b g/mol,则GaN晶胞的边长为___________ pm(列出表达式)。

(1)Ga原子的价电子排布式为
(2)实验发现,氯化铝的蒸气或溶于非极性溶剂中或处于熔融状态时,都以二聚态(Al2Cl6)形式存在。其球棍模型如图所示。

①该分子中Al原子采取
②Al2Cl6与过量NaOH溶液反应生成Na[Al(OH)4],[Al(OH)4]-中存在的化学作用力类型有
A.离子键 B.极性共价键 C.金属键 D.非极性共价键 E.配位键 F.σ键 G.氢键
(3)更高温度下Al2Cl6二聚体则离解成AlCl3,BF3是AlCl3的一种等电子体,结合价层电子对互斥理论判断,BF3的分子构型为
(4)GaN是第三代半导体材料的研究热点,在干燥的NH3气流中焙烧磨细的GaAs可制得GaN。GaN熔点约为1500℃,GaAs熔点为1238℃,GaN熔点高于GaAs的原因是
(5)GaN的其中一种晶胞结构如图所示,与金刚石的晶体结构高度相似。该晶胞中Ga原子处于N原子形成的

您最近一年使用:0次
10 . 下列说法正确的是
| A.氕、氘和氚中子数不同,互称为同素异形体 |
| B.对于∆H>0自发进行的化学反应,有∆S>0 |
C.同质量的水,体积大小为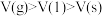 |
| D.两原子形成化学键时要有电子得失或电子偏移 |
您最近一年使用:0次



