17. 某学习小组在实验室中利用下图装置(夹持装置略去)测定某铁硫化物(Fe
xS
y)的组成,并探究反应后D装置所得溶液中含硫化合物的组成。
(一)硫化物(Fe
xS
y)的组成
实验步骤:
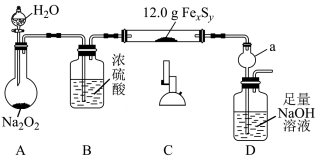
步骤Ⅰ 如图连接装置,检查装置气密性,装入药品;
步骤Ⅱ 打开分液漏斗旋塞,缓缓滴入水,并点燃酒精喷灯;
步骤Ⅲ 当硬质玻璃管中固体质量不再改变时,停止加热,继续通入—段时间的O
2步骤Ⅳ 实验结束后,将D中所得溶液加水配制成250 mL溶液;
……
请回答:
(1)仪器a的作用为
___________。
(2)步骤Ⅲ中,停止加热后还需继续通入一段时间的O
2,其目的为
___________。
(3)步骤Ⅳ中配制溶液时所需的玻璃仪器除玻璃棒和烧杯外,还有
___________。
(4)取25. 00 mL步骤Ⅳ中所配溶液,加入足量的双氧水,再加入足量盐酸酸化的BaCl
2溶液,将所得沉淀过滤、洗涤、干燥,称其质量为4.66g。则Fe
xS
y的化学式为
___________。
(5)问题讨论:有同学认为可将装置D改为装有足量碱石灰的干燥管,通过测定反应前后干燥管的增重来计算硫元素的含量。你认为此方案
___________(填“是”或“否”)合理,原因为
___________。
(二)探究反应后D装置所得溶液中含硫化合物的组成。
实验方案:取D溶液25.00 mL于锥形瓶中,用0.3000 mol • L
-1KMnO
4酸性溶液进行滴定,到达滴定终点时,消耗标准液的体积为24.00 mL,回答下列问题:。
(6)滴定终点的现象为
___________,结合(一)的数据,计算滴定前D中
c(Na
2SO
4) =
___________。