名校
1 . 已知A、B、C、D是短周期元素的气态单质,其中A是黄绿色的气体单质,C在空气中含量最高,D是最轻的气体;E是一种最常用的金属;Y是一种常见的液态物质,Z是唯一显碱性的气体; M是一种红棕色的有毒气体;I为红褐色难溶于水的固体。有关的转化关系如下图所示(反应条件均已略去)。
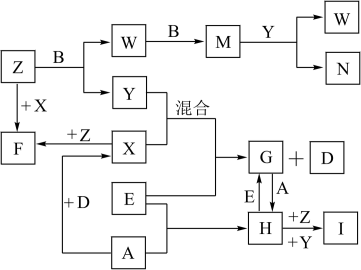
回答下列问题:
(1)A的组成元素在元素周期表的位置为____ ;
(2)F中化学键的类型是___ 、____ ;
(3)Z和W在催化剂作用下反应生成C和Y,这是很有实际意义的反应,可以消除W对环境的污染,该反应的化学方程式为_ ;
(4)将过量的E加到N的稀溶液中,若过程中转移电子的数目为3.01×1023,则参加反应的E的质量为____ g。

回答下列问题:
(1)A的组成元素在元素周期表的位置为
(2)F中化学键的类型是
(3)Z和W在催化剂作用下反应生成C和Y,这是很有实际意义的反应,可以消除W对环境的污染,该反应的化学方程式为
(4)将过量的E加到N的稀溶液中,若过程中转移电子的数目为3.01×1023,则参加反应的E的质量为
您最近一年使用:0次
名校
解题方法
2 . 按下列要求填空
(1)下列变化:①碘的升华,②冰熔化,③氯化钠溶于水,④氯化氢溶于水,⑤碳酸氢钠加热分解。化学键未被破坏的是___ ;仅共价键被破坏的是___ 。
(2)写出Na2O2的电子式:___ 。
(3)用电子式表示NH3的形成过程:___ 。
(4)4 g甲烷在氧气中燃烧生成CO2和液态水,放出222.5 kJ热量,写出表示甲烷燃烧热的热化学方程式____ 。
(5)拆开1 mol H—H键、1 mol N—H键、1 mol N≡N键分别需要的能量是436 kJ、391 kJ、946 kJ,则合成氨反应的热化学方程式为___ 。
(6)氢能的储存是氢能利用的前提,科学家研究出一种储氢合金Mg2Ni,已知:
Mg(s)+H2(g)=MgH2(s) ΔH1=-74.5 kJ·mol-1;
Mg2Ni(s)+2H2(g)=Mg2NiH4(s) ΔH2=-64.4 kJ·mol-1;
Mg2Ni(s)+2MgH2(s)=2Mg(s)+Mg2NiH4(s) ΔH3。
则ΔH3=___ kJ·mol-1
(1)下列变化:①碘的升华,②冰熔化,③氯化钠溶于水,④氯化氢溶于水,⑤碳酸氢钠加热分解。化学键未被破坏的是
(2)写出Na2O2的电子式:
(3)用电子式表示NH3的形成过程:
(4)4 g甲烷在氧气中燃烧生成CO2和液态水,放出222.5 kJ热量,写出表示甲烷燃烧热的热化学方程式
(5)拆开1 mol H—H键、1 mol N—H键、1 mol N≡N键分别需要的能量是436 kJ、391 kJ、946 kJ,则合成氨反应的热化学方程式为
(6)氢能的储存是氢能利用的前提,科学家研究出一种储氢合金Mg2Ni,已知:
Mg(s)+H2(g)=MgH2(s) ΔH1=-74.5 kJ·mol-1;
Mg2Ni(s)+2H2(g)=Mg2NiH4(s) ΔH2=-64.4 kJ·mol-1;
Mg2Ni(s)+2MgH2(s)=2Mg(s)+Mg2NiH4(s) ΔH3。
则ΔH3=
您最近一年使用:0次
名校
解题方法
3 . 已知X、Y、Z、W四种元素是短周期的元素,且原子序数依次增大。X、W同主族,Y、Z为同周期的相邻元素。W是该元素所在周期原子半径最大的元素,W原子的质子数等于Y、Z原子的最外层电子数之和。Y与X形成的分子中有3个共价键,该分子中含有10个电子。Z原子最外层电子数是次外层电子数的3倍,试判断:
(1)X、Z两种元素的元素符号为X________ ,Z________ 。
(2)由以上元素两两形成的化合物中:溶于水显碱性的气态氢化物的电子式为________________ 。
(3)①由X、Y、Z所形成的常见离子化合物是__________________ (写化学式)。
②该化合物与W的最高价氧化物对应的水化物的浓溶液加热时反应的离子方程式为_______ 。
③化合物WY3的晶体结构中含有的化学键为________ (选填序号)。
A.只含离子键 B.只含共价键 C.既含离子键又含共价键
④X与W形成的化合物与水反应生成X2,其中水作________ (填“氧化剂”或“还原剂”)。
(4)用电子式表示化合物W2Z的形成过程:______________________________________ 。
(1)X、Z两种元素的元素符号为X
(2)由以上元素两两形成的化合物中:溶于水显碱性的气态氢化物的电子式为
(3)①由X、Y、Z所形成的常见离子化合物是
②该化合物与W的最高价氧化物对应的水化物的浓溶液加热时反应的离子方程式为
③化合物WY3的晶体结构中含有的化学键为
A.只含离子键 B.只含共价键 C.既含离子键又含共价键
④X与W形成的化合物与水反应生成X2,其中水作
(4)用电子式表示化合物W2Z的形成过程:
您最近一年使用:0次
2019-06-19更新
|
266次组卷
|
3卷引用:【全国百强校】黑龙江省牡丹江市第一高级中学2018-2019学年高一下学期期中考试化学试题
【全国百强校】黑龙江省牡丹江市第一高级中学2018-2019学年高一下学期期中考试化学试题【全国百强校】吉林省长春市外国语学校2018-2019学年高一下学期第二次月考化学试题(已下线)专题04 物质结构和元素周期律——备战2021年高考化学纠错笔记
4 . 国家航天局计划2020年实施火星探测任务。据了解火星上存在大量的含氮化合物,科学家推测火星生命可能主要以氮、碳、硅、铜为基体构成。
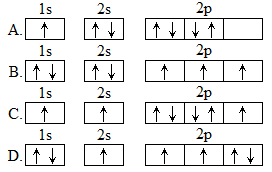
(1)下列氮原子的电子排布图表示的状态中,能量最高的是___________ (填字母标号)。
(2)某种铀氮化物的晶体结构是NaCl型。NaCl的Bom-Haber循环如下图所示。已知:元素的一个气态基态原子获得电子成为气态阴离子时所放出的能量称为电子亲和能。下列有关说法正确的是___________ (填字母标号)。
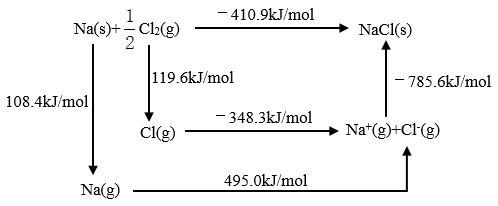
a.Cl-Cl键的键能为119.6kJ/mol
b.Na的第一电离能为603.4kJ/mol
c.NaCl的晶格能为785.6kJ/mol
d.Cl的第一电子亲和能为348.3kJ/mol
(3)乙二胺(H2N—CH2—CH2—NH2)是一种重要的配体,可简写为En。
①乙二胺分子中氮原子的杂化轨道类型为___________ 。
②乙二胺和三甲胺[N(CH3)3]均属于胺,且相对分子质量相近,但乙二胺比三甲胺的沸点高得多,原因是___________ 。
③乙二胺能与Mg2+、Cu2+等金属离子形成稳定环状离子,其中与乙二胺形成的化合物稳定性相对较高的是___________ (填“Mg2+”或“Cu2+”)。
(4)K3[Fe(CN)6](铁氰化钾)溶液可以检验铁陨石中铁元素价态。
①铁氰化钾中不存在的作用力有___________ (填字母)。
a.离子键 b.极性键 c.非极性键
d.π键 e.配位键 f.氢键
②1mol[Fe(CN)6]3-中含有的σ键数目为___________ (用NA表示阿伏加德罗常数的值)。
(5)CuF的晶胞结构如下图所示。在CuF晶体中距离Cu+最近的F-有___________ 个。已知CuF的密度为7.5g∙cm-3,则CuF的晶胞参数a=___________ nm(列出计算式)。

(1)下列氮原子的电子排布图表示的状态中,能量最高的是

(2)某种铀氮化物的晶体结构是NaCl型。NaCl的Bom-Haber循环如下图所示。已知:元素的一个气态基态原子获得电子成为气态阴离子时所放出的能量称为电子亲和能。下列有关说法正确的是

a.Cl-Cl键的键能为119.6kJ/mol
b.Na的第一电离能为603.4kJ/mol
c.NaCl的晶格能为785.6kJ/mol
d.Cl的第一电子亲和能为348.3kJ/mol
(3)乙二胺(H2N—CH2—CH2—NH2)是一种重要的配体,可简写为En。
①乙二胺分子中氮原子的杂化轨道类型为
②乙二胺和三甲胺[N(CH3)3]均属于胺,且相对分子质量相近,但乙二胺比三甲胺的沸点高得多,原因是
③乙二胺能与Mg2+、Cu2+等金属离子形成稳定环状离子,其中与乙二胺形成的化合物稳定性相对较高的是
(4)K3[Fe(CN)6](铁氰化钾)溶液可以检验铁陨石中铁元素价态。
①铁氰化钾中不存在的作用力有
a.离子键 b.极性键 c.非极性键
d.π键 e.配位键 f.氢键
②1mol[Fe(CN)6]3-中含有的σ键数目为
(5)CuF的晶胞结构如下图所示。在CuF晶体中距离Cu+最近的F-有

您最近一年使用:0次
解题方法
5 . A、B、C、D、E、F是六种短周期元素,它们的原子序数依次增大;A元素的原子半径最小;B元素的一种单质是空气中含量最多的一种成分;D与A同主族;F元素原子的最外层电子数是其次外层电子数的 ;A、B、D、F这四种元素,每一种都能与C元素形成原子个数比不相同的化合物。D、E、F三种元素最高价氧化物对应的水化物两两之间皆能反应。请回答下列问题:
;A、B、D、F这四种元素,每一种都能与C元素形成原子个数比不相同的化合物。D、E、F三种元素最高价氧化物对应的水化物两两之间皆能反应。请回答下列问题:
(1)B元素的原子结构示意图______ ;E元素在周期表中的位置是______ 。
(2)A、B、C和F可组成一种化合物,其原子个数之比为5:1:4:1。写出该化合物的化学式______ 。
(3)写出含E元素的氧化物与氢氧化钠溶液反应的离子方程式______ 。
(4)C、D、E、F四种元素的简单离子半径由大到小的顺序是______ (用离子符号表示)。
(5)由C、D两种元素形成的原子个数之比为1:1的化合物中,所含化学键的类型有______ 。
(6)用电子式表示D的简单氢化物的形成过程______ 。
 ;A、B、D、F这四种元素,每一种都能与C元素形成原子个数比不相同的化合物。D、E、F三种元素最高价氧化物对应的水化物两两之间皆能反应。请回答下列问题:
;A、B、D、F这四种元素,每一种都能与C元素形成原子个数比不相同的化合物。D、E、F三种元素最高价氧化物对应的水化物两两之间皆能反应。请回答下列问题:(1)B元素的原子结构示意图
(2)A、B、C和F可组成一种化合物,其原子个数之比为5:1:4:1。写出该化合物的化学式
(3)写出含E元素的氧化物与氢氧化钠溶液反应的离子方程式
(4)C、D、E、F四种元素的简单离子半径由大到小的顺序是
(5)由C、D两种元素形成的原子个数之比为1:1的化合物中,所含化学键的类型有
(6)用电子式表示D的简单氢化物的形成过程
您最近一年使用:0次
6 . 下表列出了9种元素在元素周期表中的位置示意。
请回答下列问题:
(1)考古工作者利用元素②的一种核素测定一些文物的年代,这种核素的符号是_____
(2)画出元素⑧形成的简单离子的结构示意图_________________
(3)写出元素④和⑥的单质在加热条件下反应,所得产物的电子式为_________
(4)⑥元素的最高价氧化物对应的水化物含有的化学键是__________________
(5)②、③、④、⑤四种元素的简单气态氢化物中,稳定性最强的是_______ (填化学式),写出元素⑥的单质与水反应的离子反应方程式___________________ ,写出一个能证明元素⑧比元素⑨非金属性强的反应事实的离子方程式__________
| 周期 | ⅠA 1 | 0 18 | ||||||
| 1 | ⅡA 2 | ⅢA 13 | ⅣA 14 | ⅤA 15 | ⅥA 16 | ⅦA 17 | ||
| 2 | ① | ② | ③ | ④ | ⑤ | |||
| 3 | ⑥ | ⑦ | ⑧ | |||||
| 4 | ⑨ | |||||||
(1)考古工作者利用元素②的一种核素测定一些文物的年代,这种核素的符号是
(2)画出元素⑧形成的简单离子的结构示意图
(3)写出元素④和⑥的单质在加热条件下反应,所得产物的电子式为
(4)⑥元素的最高价氧化物对应的水化物含有的化学键是
(5)②、③、④、⑤四种元素的简单气态氢化物中,稳定性最强的是
您最近一年使用:0次
2020-01-26更新
|
189次组卷
|
2卷引用:山东省济宁市2019-2020学年高一上学期期末考试化学试题
名校
解题方法
7 . 2008年北京奥运会的“水立方”,在2022年冬奥会上华丽转身为“冰立方”,实现了奥运场馆的再利用,其美丽的透光气囊材料由乙烯 与四氟乙烯
与四氟乙烯 的共聚物
的共聚物 制成。
制成。
(1)2015年2月,科学家首次观测到化学键的形成。化学键不存在于_______。
(2)第三周期元素的原子中,未成对电子不可能有_______。
(3)基态F原子的轨道表示式为_______ ,四氟乙烯的电子式为_______ 。
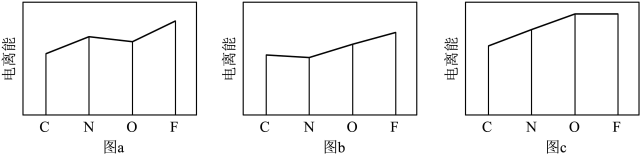
(4)图a、b、c分别表示C、N、O和F的逐级电离能I变化趋势(纵坐标的标度不同)。第一电离能的变化图是_______ (填字母),第三电离能的变化图是_______ (填字母)。
(5) 和
和 分子中C的杂化轨道类型分别为
分子中C的杂化轨道类型分别为_______ 和_______ ;聚四氟乙烯的化学稳定性高于聚乙烯,从化学键的角度解释原因_______ 。
(6)比较甲醚和乙醇的沸点高低,并说明理由_______ 。
 与四氟乙烯
与四氟乙烯 的共聚物
的共聚物 制成。
制成。(1)2015年2月,科学家首次观测到化学键的形成。化学键不存在于_______。
| A.原子与原子之间 | B.分子与分子之间 | C.离子与离子之间 | D.离子与电子之间 |
(2)第三周期元素的原子中,未成对电子不可能有_______。
| A.4个 | B.3个 | C.2个 | D.1个 |
(3)基态F原子的轨道表示式为
(4)图a、b、c分别表示C、N、O和F的逐级电离能I变化趋势(纵坐标的标度不同)。第一电离能的变化图是

(5)
 和
和 分子中C的杂化轨道类型分别为
分子中C的杂化轨道类型分别为(6)比较甲醚和乙醇的沸点高低,并说明理由
您最近一年使用:0次
名校
解题方法
8 . 电镀废水中常含有剧毒的NaCN,可用两段氧化法处理:
①第一段:NaCN+NaClO→NaOCN+NaCl
②第二段:NaOCN+NaClO→Na2CO3+CO2↑+NaCl+N2↑(未配平)
完成下列填空:
(1)上述反应涉及的元素Na、N、O中,简单离子半径最小的是___ (填离子符号),氢原子最外层电子的轨道表示式是___ 。
(2)NaCN中所含有的化学键类型是___ ,N2的电子式为___ 。
(3)已知NaOCN中N元素为-3价,配平第二段过程的化学方程式并标出电子转移的方向和数目___ 。
(4)综合两段反应,处理含有0.01molNaCN的废水,至少需NacClO___ mol。
(5)请用一个方程式证明氮元素的非金属性大于碳元素___ 。
①第一段:NaCN+NaClO→NaOCN+NaCl
②第二段:NaOCN+NaClO→Na2CO3+CO2↑+NaCl+N2↑(未配平)
完成下列填空:
(1)上述反应涉及的元素Na、N、O中,简单离子半径最小的是
(2)NaCN中所含有的化学键类型是
(3)已知NaOCN中N元素为-3价,配平第二段过程的化学方程式并标出电子转移的方向和数目
(4)综合两段反应,处理含有0.01molNaCN的废水,至少需NacClO
(5)请用一个方程式证明氮元素的非金属性大于碳元素
您最近一年使用:0次
名校
解题方法
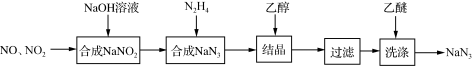
9 . 叠氮化钠(NaN3)是一种无色晶体,易溶于水,微溶于乙醇,不溶于乙醚,广泛应用于汽车安全气囊。某硝酸工厂拟通过下列方法处理尾气并制备叠氮化钠。___________ 。
(2)已知NaN3阳离子与阴离子个数比为1:1,则NaN3中所含的化学键为___________ ,1mol该阴离子中所含的电子总数为___________ mol
(3)汽车剧烈碰撞时,安全气囊中发生反应:10NaN3+2KNO3 K2O+5Na2O+16N2↑。假定汽车中某个安全气囊容积为56L。
K2O+5Na2O+16N2↑。假定汽车中某个安全气囊容积为56L。
①该反应中的还原剂为___________ (填化学式)。
②欲使气囊中充满标准状况下氮气,则该安全气囊中生成的K2O和Na2O的总质量为多少克___________ ?(写出计算过程,保留一位小数,不考虑固体的体积)。
(2)已知NaN3阳离子与阴离子个数比为1:1,则NaN3中所含的化学键为
(3)汽车剧烈碰撞时,安全气囊中发生反应:10NaN3+2KNO3
 K2O+5Na2O+16N2↑。假定汽车中某个安全气囊容积为56L。
K2O+5Na2O+16N2↑。假定汽车中某个安全气囊容积为56L。①该反应中的还原剂为
②欲使气囊中充满标准状况下氮气,则该安全气囊中生成的K2O和Na2O的总质量为多少克
您最近一年使用:0次
10 . 某混合物浆液含Al(OH)3、MnO2和少量Na2CrO4。考虑到胶体的吸附作用使Na2CrO4不易完全被水浸出,某研究小组利用设计的电解分离装置(见下图),使浆液分离成固体混合物和含铬元素溶液,并回收利用。回答I和Ⅱ中的问题。
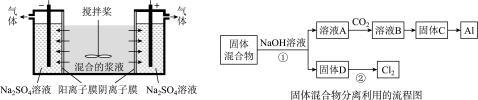
I.固体混合物的分离和利用(流程图中的部分分离操作和反应条件未标明)
(1)Cl在元素周期表中的位置为_____ ,CO2的电子式为___ ,NaOH中存在的化学键类型为_____ 。
(2)B-C的反应条件为_____ ,C→Al的制备反应化学方程式为__________ 。
(3)该小组探究反应②发生的条件。D与浓盐酸混合,不加热,无变化:加热有Cl2生成,当反应停止后,固体有剩余,此时滴加硫酸,又产生Cl2。由此判断影响该反应有效进行的因素有(填序号)______ 。
a.温度 b.Cl的浓度 c.溶液的酸度
Ⅱ.含铬元素溶液的分离和利用
(4)用情性电极电解时,CrO42-能从浆液中分离出来的原因是____ ,分离后含铬元素的粒子是____ ;阴极室生成的物质为_______ (写化学式)。

I.固体混合物的分离和利用(流程图中的部分分离操作和反应条件未标明)
(1)Cl在元素周期表中的位置为
(2)B-C的反应条件为
(3)该小组探究反应②发生的条件。D与浓盐酸混合,不加热,无变化:加热有Cl2生成,当反应停止后,固体有剩余,此时滴加硫酸,又产生Cl2。由此判断影响该反应有效进行的因素有(填序号)
a.温度 b.Cl的浓度 c.溶液的酸度
Ⅱ.含铬元素溶液的分离和利用
(4)用情性电极电解时,CrO42-能从浆液中分离出来的原因是
您最近一年使用:0次



