1 . 下列化学用语表述正确的是
A.熟石膏的化学式: | B. 分子的VSEPR模型: 分子的VSEPR模型: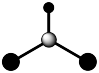 |
C.基态溴原子的价层电子排布式:[Ar] | D.含有8个中子的碳原子: |
您最近一年使用:0次
解题方法
2 . 硒(Se)和碲(Te)均为硫(S)的同族元素,原子序数分别为34、52,它们的单质和化合物在电子、冶金、材料等领域有广阔的发展前景。科研小组以精炼铜的阳极泥为原料(含有 、
、 、
、 和少量金属单质Ag)回收Se、Te并制备胆矾的一种流程如图:
和少量金属单质Ag)回收Se、Te并制备胆矾的一种流程如图:

回答下列问题:
(1)Cu原子的价电子排布式为_______ ; 属于
属于_______ (填“酸性”“碱性”或“两性”)氧化物。
(2) 的稳定性比
的稳定性比 的
的_______ (填“强”或“弱”); ,
, ,
, 的沸点由高到低为
的沸点由高到低为_______ 。
(3)“水溶”反应的离子方程式为_______ 。
(4)“碱溶”的目的为_______ 。
(5)“分离”过程需控制适当温度,不宜过高或过低的理由为_______ 。
(6)若滤液2的 ,其中
,其中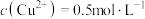 、
、 、
、 ,则滤渣Ⅱ的成分为
,则滤渣Ⅱ的成分为_______ 。[已知 、
、 ]
]
(7)用滤液2制备 的操作为
的操作为_______ 。
 、
、 、
、 和少量金属单质Ag)回收Se、Te并制备胆矾的一种流程如图:
和少量金属单质Ag)回收Se、Te并制备胆矾的一种流程如图:
回答下列问题:
(1)Cu原子的价电子排布式为
 属于
属于(2)
 的稳定性比
的稳定性比 的
的 ,
, ,
, 的沸点由高到低为
的沸点由高到低为(3)“水溶”反应的离子方程式为
(4)“碱溶”的目的为
(5)“分离”过程需控制适当温度,不宜过高或过低的理由为
(6)若滤液2的
 ,其中
,其中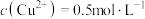 、
、 、
、 ,则滤渣Ⅱ的成分为
,则滤渣Ⅱ的成分为 、
、 ]
](7)用滤液2制备
 的操作为
的操作为
您最近一年使用:0次
名校
3 . 依据原子结构知识回答下列问题。
(1)基态硅原子的电子排布式是___________ 。
(2)基态铁原子有___________ 个未成对电子,基态 的价电子排布图为
的价电子排布图为___________ 。
(3)下列说法错误的是___________(填字母)。
(4)过氧化氢( )是一种医用消毒杀菌剂。已知
)是一种医用消毒杀菌剂。已知 的结构如图所示。
的结构如图所示。 不是直线形的,两个氢原子犹如在半展开的书的两面纸上,书面角为93°52′,两个
不是直线形的,两个氢原子犹如在半展开的书的两面纸上,书面角为93°52′,两个 与
与 的夹角均为96°52′。
的夹角均为96°52′。

① 的电子式为
的电子式为___________ ,结构式为___________ 。
② 中存在
中存在___________ 键和___________ 键,为___________ (填“极性”或“非极性”)分子。
(1)基态硅原子的电子排布式是
(2)基态铁原子有
 的价电子排布图为
的价电子排布图为(3)下列说法错误的是___________(填字母)。
A.元素的电负性: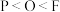 | B.元素的第一电离能: |
C.离子半径: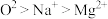 | D.原子的未成对电子数: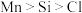 |
(4)过氧化氢(
 )是一种医用消毒杀菌剂。已知
)是一种医用消毒杀菌剂。已知 的结构如图所示。
的结构如图所示。 不是直线形的,两个氢原子犹如在半展开的书的两面纸上,书面角为93°52′,两个
不是直线形的,两个氢原子犹如在半展开的书的两面纸上,书面角为93°52′,两个 与
与 的夹角均为96°52′。
的夹角均为96°52′。
①
 的电子式为
的电子式为②
 中存在
中存在
您最近一年使用:0次
2024-02-03更新
|
338次组卷
|
2卷引用:江西省景德镇市乐平中学2023-2024学年高二下学期3月月考化学试题
4 . 1906年,哈伯在60℃高温、200兆帕高压的条件下,用锇(Os)作催化剂,首次成功得到了氨,但产率较低。随着科学的进步以及科学家们对催化剂的研究改进,现在工业上普遍采用铁触媒做合成氨的催化剂,大大提高了合成氨的产率。
(1)基态氮原子中,核外电子有_______ 种空间运动状态,能量最高的电子的电子云在空间有_______ 个伸展方向。
(2)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用“ ”表示,与之相反的用“
”表示,与之相反的用“ ”表示,称为电子的自旋磁量子数。对于基态的氮原子,其价电子自旋磁量子数的代数和为
”表示,称为电子的自旋磁量子数。对于基态的氮原子,其价电子自旋磁量子数的代数和为_______ 。
(3)铁触媒是普遍使用的以铁为主体的多成分催化剂,通常还含有 、
、 、
、 、
、 、
、 等氧化物中的几种。
等氧化物中的几种。
①Cr原子的价电子排布图为_______ ;第四周期ds区元素中,与基态Cr原子最外层电子数目相同的元素的元素符号为_______ 。
②上述氧化物所涉及的元素中,处于元素周期表中p区的元素有_______ (填元素符号)。
(4)我国科研人员研制出了 (M为Fe、Mn等金属)等催化剂,使得合成氨工业的温度,压强分别降到了350℃、
(M为Fe、Mn等金属)等催化剂,使得合成氨工业的温度,压强分别降到了350℃、 ,这是近年来合成氨反应研究中的重要突破。
,这是近年来合成氨反应研究中的重要突破。
①Mn在元素周期表中的位置_______ ,基态Mn原子未成对的电子数为_______ 。
②第三电离能
_______ 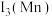 (填“>”或“<”),原因是
(填“>”或“<”),原因是_______ 。
(5)我国长征系列运载火箭使用的液态燃料主要是偏二甲肼[结构简式: ,可看作是肼
,可看作是肼 中同一氮原子上的两个氢原子被甲基取代]和四氧化二氮,燃烧时发生反应:
中同一氮原子上的两个氢原子被甲基取代]和四氧化二氮,燃烧时发生反应: 。当该反应消耗
。当该反应消耗 时将形成
时将形成_______  。
。
(1)基态氮原子中,核外电子有
(2)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用“
 ”表示,与之相反的用“
”表示,与之相反的用“ ”表示,称为电子的自旋磁量子数。对于基态的氮原子,其价电子自旋磁量子数的代数和为
”表示,称为电子的自旋磁量子数。对于基态的氮原子,其价电子自旋磁量子数的代数和为(3)铁触媒是普遍使用的以铁为主体的多成分催化剂,通常还含有
 、
、 、
、 、
、 、
、 等氧化物中的几种。
等氧化物中的几种。①Cr原子的价电子排布图为
②上述氧化物所涉及的元素中,处于元素周期表中p区的元素有
(4)我国科研人员研制出了
 (M为Fe、Mn等金属)等催化剂,使得合成氨工业的温度,压强分别降到了350℃、
(M为Fe、Mn等金属)等催化剂,使得合成氨工业的温度,压强分别降到了350℃、 ,这是近年来合成氨反应研究中的重要突破。
,这是近年来合成氨反应研究中的重要突破。①Mn在元素周期表中的位置
②第三电离能

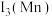 (填“>”或“<”),原因是
(填“>”或“<”),原因是(5)我国长征系列运载火箭使用的液态燃料主要是偏二甲肼[结构简式:
 ,可看作是肼
,可看作是肼 中同一氮原子上的两个氢原子被甲基取代]和四氧化二氮,燃烧时发生反应:
中同一氮原子上的两个氢原子被甲基取代]和四氧化二氮,燃烧时发生反应: 。当该反应消耗
。当该反应消耗 时将形成
时将形成 。
。
您最近一年使用:0次
2024-02-02更新
|
227次组卷
|
2卷引用:江西省景德镇市乐平中学2023-2024学年高二下学期3月月考化学试题
名校
5 . 下列说法正确的是
A.元素周期表每一周期元素原子的最外层电子排布均是从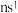 过渡到 过渡到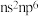 |
| B.元素周期表中可以把元素分成s、p、d、f四个区 |
C.原子的价层电子排布为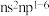 的元素一定是主族元素 的元素一定是主族元素 |
| D.Cu位于元素周期表中第四周期第ⅠB族,属于ds区元素 |
您最近一年使用:0次
2024-01-21更新
|
129次组卷
|
2卷引用:江西省景德镇市乐平中学2023-2024学年高二下学期3月月考化学试题
6 . 下列化学用语或图示表达正确的是
| A.基态K原子的核外电子的空间运动状态共有10种 |
B.MgCl2的形成过程为 |
| C.基态碘原子简化电子排布式为[ Kr]5s25p5 |
D.根据洪特规则可知,电子排布式为1s22s22p2的元素的电子轨道表示式为 |
您最近一年使用:0次
2024-01-21更新
|
309次组卷
|
3卷引用:江西省景德镇市乐平中学2023-2024学年高二下学期3月月考化学试题
名校
解题方法
7 . “夏禹铸九鼎,天下分九州”,青铜器在古时被称为“吉金”,是红铜与锡、铅等的合金。铜锈大多呈青绿色,主要含有 和
和 。下列说法错误的是
。下列说法错误的是
| A.基态铜原子核外电子有15种不同的空间运动状态 |
| B.青铜的熔点低于纯铜 |
| C.青铜器中锡、铅对铜有保护作用 |
D.可用 溶液浸泡青铜器来清洗水铜器的铜锈 溶液浸泡青铜器来清洗水铜器的铜锈 |
您最近一年使用:0次
2024-01-15更新
|
344次组卷
|
3卷引用:江西省景德镇市乐平中学2023-2024学年高二下学期3月月考化学试题
江西省景德镇市乐平中学2023-2024学年高二下学期3月月考化学试题福建师范大学附属中学2023-2024学年高三上学期12月月考化学试卷(已下线)化学(九省联考考后提升卷,吉林、黑龙江卷)-2024年1月“九省联考”真题完全解读与考后提升
名校
解题方法
8 . 黑磷与石墨类似,也具有层状结构(如图1)。科学家最近研发了黑磷-石墨复合负极材料,其单层结构的俯视图如图2所示。下列说法错误的是


| A.黑磷区中P—P的键能不完全相同 |
| B.单层复合材料中C和P间的作用力为共价键 |
| C.基态磷原子核外电子中,两种自旋状态的电子数之比为3:2 |
| D.黑磷中P原子的杂化方式和石墨中C原子的杂化方式相同 |
您最近一年使用:0次
2023-12-24更新
|
311次组卷
|
3卷引用:江西省景德镇市乐平中学2023-2024学年高二下学期3月月考化学试题
名校
解题方法
9 . 硒(Se)是一种有抗癌、抗氧化作用的元素,可形成多种化合物。某化合物是潜在热电材料之一,其晶胞结构如图1,沿x、y、z轴方向的投影均为图2。

A.Se的基态原子价电子排布式为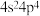 |
| B.该化合物的晶体类型是离子晶体 |
C.该化合物的化学式为 |
D.距离K最近的 八面体有4个 八面体有4个 |
您最近一年使用:0次
2023-11-06更新
|
782次组卷
|
8卷引用:江西省景德镇市乐平中学2023-2024学年高二下学期3月月考化学试题
解题方法
10 . 卡尔·巴里·夏普莱斯(KarlBarrySharpless),2001年因“不对称合成”获得诺贝尔化学奖;2022年因“点击化学”再次获得诺贝尔化学奖,成为目前在世的唯一一位2次获得诺贝尔化学奖的化学家。下图是夏普莱斯发明的一种锰手性催化剂(B)的制备过程,回答相应问题。

(1)写出基态Mn3+的价电子的轨道表示式___________ 。A中N原子的杂化方式为___________ 。
(2)单个B分子内不存在的作用力有___________ 。
a.极性键b.非极性键c.配位键d.离子键e.氢键
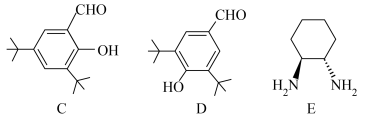
(3)A可以由C和E反应制备,C与D互为同分异构体。E分子含有___________ 个手性碳原子;比较C与D的熔点高低并说明理由___________ 。
(4)比较第三电离能:Mn___________ Fe;VSEPR模型一般不适用过渡元素,但高锰酸根适用,则高锰酸根的空间构型为___________ 。
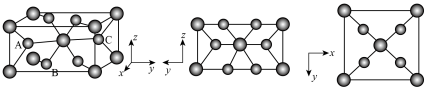
(5)Mn的某种氧化物的晶胞图和投影图如下图。已知晶胞参数为:a=b>c,α=β=γ=90°且a<1.5c.以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分数坐标,如A、B点原子的分数坐标分别为(0.8,0.2,0.5)、(0.3,0.3,0)。已知该晶体中Mn-O键长只有2种。则C点原子的分数坐标为___________ ;Mn和O之间的最短距离为___________ 。

(1)写出基态Mn3+的价电子的轨道表示式
(2)单个B分子内不存在的作用力有
a.极性键b.非极性键c.配位键d.离子键e.氢键
(3)A可以由C和E反应制备,C与D互为同分异构体。E分子含有

(4)比较第三电离能:Mn
(5)Mn的某种氧化物的晶胞图和投影图如下图。已知晶胞参数为:a=b>c,α=β=γ=90°且a<1.5c.以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分数坐标,如A、B点原子的分数坐标分别为(0.8,0.2,0.5)、(0.3,0.3,0)。已知该晶体中Mn-O键长只有2种。则C点原子的分数坐标为

您最近一年使用:0次



