解题方法
1 . 利用反应: 制备无水CrCl3.下列说法正确的是
制备无水CrCl3.下列说法正确的是
 制备无水CrCl3.下列说法正确的是
制备无水CrCl3.下列说法正确的是| A.该反应属于氧化还原反应 |
| B.SOCl2的中心原子S上有孤电子对 |
| C.上述反应涉及元素中,电负性:Cl>S>O |
D.基态Cr原子价层电子排布式为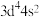 |
您最近半年使用:0次
解题方法
2 . 下列化学用语或图示不正确的是
A.基态 的价电子轨道表示式: 的价电子轨道表示式: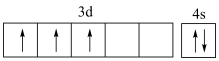 |
B.用离子方程式表示 溶于烧碱溶液: 溶于烧碱溶液: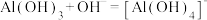 |
C.1,3-丁二烯的键线式: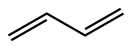 |
D.甲烷分子的空间填充模型: |
您最近半年使用:0次
3 . 下列符号表征或说法正确的是
A.HClO的电子式: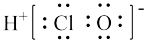 |
B. 的VSEPR模型: 的VSEPR模型: |
C. 的离子结构示意图: 的离子结构示意图: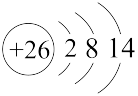 |
D.基态S原子的价电子排布图: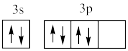 |
您最近半年使用:0次
名校
解题方法
4 . 氧化钪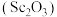 可用作半导体镀层的蒸镀材料,也可制成可变波长的固体激光器和高清晰度的电视电子枪、金属卤化物灯等。以钛白工业废酸(含
可用作半导体镀层的蒸镀材料,也可制成可变波长的固体激光器和高清晰度的电视电子枪、金属卤化物灯等。以钛白工业废酸(含 、
、 等离子)为原料制备氧化钪
等离子)为原料制备氧化钪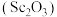 的一种流程如下图。
的一种流程如下图。
(1)基态钪原子的价层电子排布式为___________ 。
(2)“萃取”时,钛白工业废酸中加入 可降低钛的萃取率,可能是生成了难萃取的
可降低钛的萃取率,可能是生成了难萃取的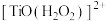 ,其中
,其中 的作用是
的作用是___________ (填标号)。
A.作氧化剂 B.作还原剂 C.提供配体
(3)“洗涤”时,洗涤剂是用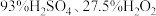 和
和 三种试剂按一定比例混合而成。实验室中混合三种试剂的操作是:将A试剂沿烧杯内壁缓慢注入B试剂中,并用玻璃棒不断搅拌,冷却后再将所得混合液缓慢注入C试剂中,并不断搅拌,则A、C分别对应上述试剂中的
三种试剂按一定比例混合而成。实验室中混合三种试剂的操作是:将A试剂沿烧杯内壁缓慢注入B试剂中,并用玻璃棒不断搅拌,冷却后再将所得混合液缓慢注入C试剂中,并不断搅拌,则A、C分别对应上述试剂中的___________ 、___________ 。
(4)萃取剂萃取 的原理为
的原理为 (
(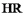 代表萃取剂)。在“反萃取”中,加入
代表萃取剂)。在“反萃取”中,加入 溶液后生成
溶液后生成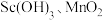 等物质,其中生成含
等物质,其中生成含 化合物的化学方程式为
化合物的化学方程式为___________ 。 时,经“反萃取”后所得滤液的
时,经“反萃取”后所得滤液的 ,则残留的
,则残留的 浓度为
浓度为___________  (已知:
(已知: 时,
时, 。
。
(5)“沉钪”时用到草酸。已知草酸的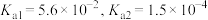 ,则在
,则在 时,
时, 的草酸溶液中
的草酸溶液中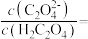
___________ 。
(6)在空气中焙烧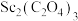 的化学方程式为
的化学方程式为___________ 。
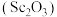 可用作半导体镀层的蒸镀材料,也可制成可变波长的固体激光器和高清晰度的电视电子枪、金属卤化物灯等。以钛白工业废酸(含
可用作半导体镀层的蒸镀材料,也可制成可变波长的固体激光器和高清晰度的电视电子枪、金属卤化物灯等。以钛白工业废酸(含 、
、 等离子)为原料制备氧化钪
等离子)为原料制备氧化钪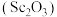 的一种流程如下图。
的一种流程如下图。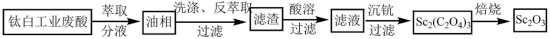
(1)基态钪原子的价层电子排布式为
(2)“萃取”时,钛白工业废酸中加入
 可降低钛的萃取率,可能是生成了难萃取的
可降低钛的萃取率,可能是生成了难萃取的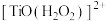 ,其中
,其中 的作用是
的作用是A.作氧化剂 B.作还原剂 C.提供配体
(3)“洗涤”时,洗涤剂是用
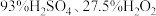 和
和 三种试剂按一定比例混合而成。实验室中混合三种试剂的操作是:将A试剂沿烧杯内壁缓慢注入B试剂中,并用玻璃棒不断搅拌,冷却后再将所得混合液缓慢注入C试剂中,并不断搅拌,则A、C分别对应上述试剂中的
三种试剂按一定比例混合而成。实验室中混合三种试剂的操作是:将A试剂沿烧杯内壁缓慢注入B试剂中,并用玻璃棒不断搅拌,冷却后再将所得混合液缓慢注入C试剂中,并不断搅拌,则A、C分别对应上述试剂中的(4)萃取剂萃取
 的原理为
的原理为 (
(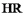 代表萃取剂)。在“反萃取”中,加入
代表萃取剂)。在“反萃取”中,加入 溶液后生成
溶液后生成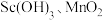 等物质,其中生成含
等物质,其中生成含 化合物的化学方程式为
化合物的化学方程式为 时,经“反萃取”后所得滤液的
时,经“反萃取”后所得滤液的 ,则残留的
,则残留的 浓度为
浓度为 (已知:
(已知: 时,
时, 。
。(5)“沉钪”时用到草酸。已知草酸的
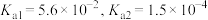 ,则在
,则在 时,
时, 的草酸溶液中
的草酸溶液中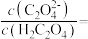
(6)在空气中焙烧
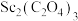 的化学方程式为
的化学方程式为
您最近半年使用:0次
名校
解题方法
5 . NH4NO3、Pb(N3)2、N5AsF6、2,4,6-三硝基甲苯均可用作炸药。下列关于它们的说法正确的是
A.NH4NO3是一种常见的炸药,其分解反应为2NH4NO3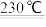 2N2↑+O2↑+4H2O↑,上述反应中,每生成0.15molO2转移电子数为0.6NA 2N2↑+O2↑+4H2O↑,上述反应中,每生成0.15molO2转移电子数为0.6NA |
B. 的中心原子N的杂化方式为sp杂化 的中心原子N的杂化方式为sp杂化 |
| C.基态As原子的价层电子中成对电子数与未成对电子数的比值为12∶3 |
| D.NH4NO3、Pb(N3)2、N5AsF6、2,4,6-三硝基甲苯形成的晶体均为离子晶体 |
您最近半年使用:0次
名校
6 . 元素及其化合物因其结构的差异导致性质各异。请回答:
(1)某激发态磷原子的电子排布式为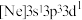 ,该磷原子中有
,该磷原子中有____ 种空间运动状态不同的电子。
(2)NCl3的空间结构为_____ ,和BCl3相比二者中沸点更高的物质是_____ ,第一电离能介于B、N之间的第二周期元素有_____ 种。
(3)M是氮杂氟硼二吡咯类物质,常用作光敏剂,其结构如图。 键,则虚线框中氮元素采用杂化方式为
键,则虚线框中氮元素采用杂化方式为____ ,M中存在的微粒间作用力有____ (填标号)。
A.共价键 B.离子键 C.氢键 D.配位键
(4)FeS2晶体的晶胞形状为立方体,边长为anm,结构如图。____ 个。
②FeS2的摩尔质量为120g∙mol-1,阿伏加德罗常数为NA.该晶体的密度为____ g∙cm-3。
(1)某激发态磷原子的电子排布式为
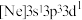 ,该磷原子中有
,该磷原子中有(2)NCl3的空间结构为
(3)M是氮杂氟硼二吡咯类物质,常用作光敏剂,其结构如图。
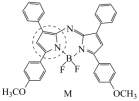
 键,则虚线框中氮元素采用杂化方式为
键,则虚线框中氮元素采用杂化方式为A.共价键 B.离子键 C.氢键 D.配位键
(4)FeS2晶体的晶胞形状为立方体,边长为anm,结构如图。

②FeS2的摩尔质量为120g∙mol-1,阿伏加德罗常数为NA.该晶体的密度为
您最近半年使用:0次
解题方法
7 . 江四矿产资源丰富,其中铁、锰、钛、钒、铜、锌、金、银等储量居全国前3位,有亚洲最大的铜矿和中国最大的铜冶炼基地。回答下列问题:
(1)铜原子价层电子排布图______ 。
(2) 是一种常见农药,能防治真菌、细菌和霉菌引起的多种病害。1mol
是一种常见农药,能防治真菌、细菌和霉菌引起的多种病害。1mol  中含有的
中含有的 键数目为
键数目为______ ; 分子与
分子与 形成配合物后
形成配合物后 键角
键角______ (填“变大”“变小”或“不变”)。
(3)Cu与Fe的第二电离能分别为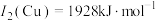 、
、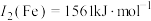 ,
,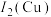 大于
大于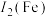 的主要原因是
的主要原因是______ 。
(4) 蒸气状态下以双聚分子形式在(如图),其中Fe的配位数为
蒸气状态下以双聚分子形式在(如图),其中Fe的配位数为______ ,双聚分子中存在配位键,提供空轨道的是______ (填元素符号)原子。______ ;若合金的密度为 ,
, 代表阿伏加德罗常数的值,则晶胞中两个钛原子间的最近距离是
代表阿伏加德罗常数的值,则晶胞中两个钛原子间的最近距离是______ pm(用含 和
和 的计算式表示,不必化简)。
的计算式表示,不必化简)。
(1)铜原子价层电子排布图
(2)
 是一种常见农药,能防治真菌、细菌和霉菌引起的多种病害。1mol
是一种常见农药,能防治真菌、细菌和霉菌引起的多种病害。1mol  中含有的
中含有的 键数目为
键数目为 分子与
分子与 形成配合物后
形成配合物后 键角
键角(3)Cu与Fe的第二电离能分别为
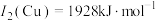 、
、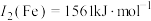 ,
,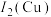 大于
大于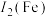 的主要原因是
的主要原因是(4)
 蒸气状态下以双聚分子形式在(如图),其中Fe的配位数为
蒸气状态下以双聚分子形式在(如图),其中Fe的配位数为
 ,
, 代表阿伏加德罗常数的值,则晶胞中两个钛原子间的最近距离是
代表阿伏加德罗常数的值,则晶胞中两个钛原子间的最近距离是 和
和 的计算式表示,不必化简)。
的计算式表示,不必化简)。
您最近半年使用:0次
解题方法
8 . 下列化学用语表示正确的是
A.基态氧原子的轨道表示式: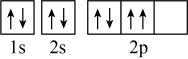 |
B. 分子的空间填充模型: 分子的空间填充模型: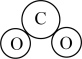 |
C. 分子的VSEPR模型: 分子的VSEPR模型: |
D.聚丙烯的结构简式: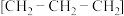 |
您最近半年使用:0次
9 . 下列化学用语表述正确的是
A.熟石膏的化学式: | B. 分子的VSEPR模型: 分子的VSEPR模型: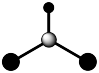 |
C.基态溴原子的价层电子排布式:[Ar] | D.含有8个中子的碳原子: |
您最近半年使用:0次
解题方法
10 . 硒和碲是重要的稀散元素,都可以作为半导体材料。一种从碲碱渣(碲和硒的含量较高,还含有少量 、
、 等元素)分离硒回收碲的工艺流程如下:
等元素)分离硒回收碲的工艺流程如下: 、
、 及少量可溶性的铜、铅化合物等。
及少量可溶性的铜、铅化合物等。
② 为两性氧化物,微溶于水。
为两性氧化物,微溶于水。
③亚硒酸为二元弱酸,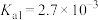 、
、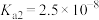
回答下列问题:
(1)硒与氧同族,基态 原子价电子排布式为
原子价电子排布式为___________ 。比较键角大小:
___________  (填“>”“<”或“=”),原因是
(填“>”“<”或“=”),原因是___________ 。
(2)“除杂渣”的主要成分为___________ 。
(3)“中和”时控制 为
为 ,生成
,生成 沉淀,若硫酸过量,将导致
沉淀,若硫酸过量,将导致 的回收率下降的原因是
的回收率下降的原因是___________ 。
(4)“酸浸液”中硒主要以亚硒酸的形式存在。若控制“酸浸液”的 为2,此时溶液中
为2,此时溶液中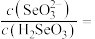
___________ 。
(5)“沉硒”时生成了一种无污染的单质气体,写出“沉硒”时发生的主要反应的化学方程式___________ 。
(6)一种以 和
和 为电极、
为电极、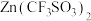 水溶液为电解质的电池,放电时,
水溶液为电解质的电池,放电时, 插入
插入 层间形成
层间形成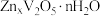 。写出该电池放电时正极的电极反应式
。写出该电池放电时正极的电极反应式___________ 。
 、
、 等元素)分离硒回收碲的工艺流程如下:
等元素)分离硒回收碲的工艺流程如下:
 、
、 及少量可溶性的铜、铅化合物等。
及少量可溶性的铜、铅化合物等。②
 为两性氧化物,微溶于水。
为两性氧化物,微溶于水。③亚硒酸为二元弱酸,
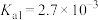 、
、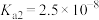
回答下列问题:
(1)硒与氧同族,基态
 原子价电子排布式为
原子价电子排布式为
 (填“>”“<”或“=”),原因是
(填“>”“<”或“=”),原因是(2)“除杂渣”的主要成分为
(3)“中和”时控制
 为
为 ,生成
,生成 沉淀,若硫酸过量,将导致
沉淀,若硫酸过量,将导致 的回收率下降的原因是
的回收率下降的原因是(4)“酸浸液”中硒主要以亚硒酸的形式存在。若控制“酸浸液”的
 为2,此时溶液中
为2,此时溶液中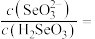
(5)“沉硒”时生成了一种无污染的单质气体,写出“沉硒”时发生的主要反应的化学方程式
(6)一种以
 和
和 为电极、
为电极、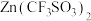 水溶液为电解质的电池,放电时,
水溶液为电解质的电池,放电时, 插入
插入 层间形成
层间形成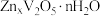 。写出该电池放电时正极的电极反应式
。写出该电池放电时正极的电极反应式
您最近半年使用:0次



