解题方法
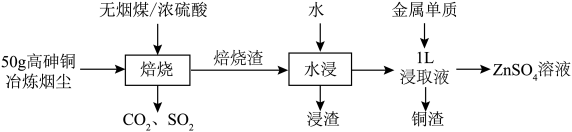
1 . 某研究小组模拟用硫酸化焙烧—水浸工艺从高砷铜冶炼烟尘中浸出铜、锌的流程如下。 及氧化物,焙烧时,金属砷酸盐转化为硫酸盐与
及氧化物,焙烧时,金属砷酸盐转化为硫酸盐与 。各元素质量分数如下:
。各元素质量分数如下:
②25℃时,硫酸铅的溶度积常数 ;
;
③浸出率的计算:浸出率 。
。
回答下列问题:
(1)基态Zn原子的价层电子排布式为___________ 。
(2)“焙烧”时,无烟煤除了为焙烧提供热量外,还表现___________ 的作用。请补全 参与反应的化学方程式:
参与反应的化学方程式:
___________ 。
(3)“水浸”时,所得浸渣的主要成分为___________ (写化学式),往浸取液中加入的金属单质是___________ (写化学式)。
(4)高砷铜冶炼烟尘经过焙烧、水浸等工序后,测得浸取液中 为
为 ,请从理论上分析铅是否沉淀完全?
,请从理论上分析铅是否沉淀完全?___________ (列式计算并得出结论)。
(5)铜浸出率的测定:从上述流程中得到的1L浸取液中取50mL与过量的酸性KI完全反应后,过滤,往滤液中滴加淀粉溶液为指示剂,用 标准溶液滴定,滴定终点时消耗
标准溶液滴定,滴定终点时消耗 标准溶液21.00mL。
标准溶液21.00mL。
(已知: ,
, )
)
①滴定终点的现象为___________ 。
②忽略流程中的损失,可得铜的浸出率为___________ 。
 及氧化物,焙烧时,金属砷酸盐转化为硫酸盐与
及氧化物,焙烧时,金属砷酸盐转化为硫酸盐与 。各元素质量分数如下:
。各元素质量分数如下:| Cu | Zn | As | Pb | In | Ag |
| 5.60% | 15.60% | 28.68% | 22.34% | 0.073% | 0.01% |
 ;
;③浸出率的计算:浸出率
 。
。回答下列问题:
(1)基态Zn原子的价层电子排布式为
(2)“焙烧”时,无烟煤除了为焙烧提供热量外,还表现
 参与反应的化学方程式:
参与反应的化学方程式:
(3)“水浸”时,所得浸渣的主要成分为
(4)高砷铜冶炼烟尘经过焙烧、水浸等工序后,测得浸取液中
 为
为 ,请从理论上分析铅是否沉淀完全?
,请从理论上分析铅是否沉淀完全?(5)铜浸出率的测定:从上述流程中得到的1L浸取液中取50mL与过量的酸性KI完全反应后,过滤,往滤液中滴加淀粉溶液为指示剂,用
 标准溶液滴定,滴定终点时消耗
标准溶液滴定,滴定终点时消耗 标准溶液21.00mL。
标准溶液21.00mL。(已知:
 ,
, )
)①滴定终点的现象为
②忽略流程中的损失,可得铜的浸出率为
您最近一年使用:0次
2 . 硫化锶(SrS)可用作发光材料、光谱纯试剂和燃料添加剂。工业上可用碳热还原法制备SrS,相关反应及信息如下表所示:
回答下列问题:
(1)Sr与Ca同族且相邻。基态Sr原子的电子排布式为___________ 。
(2)反应Ⅰ、Ⅱ、Ⅲ中,自发进行所需温度最高的是___________ (填反应序号)。
(3)将1 mol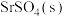 和3 mol
和3 mol 加入10 L恒容密闭容器中制备SrS,实验测得平衡体系中各成分的物质的量分数与温度的关系如图所示:
加入10 L恒容密闭容器中制备SrS,实验测得平衡体系中各成分的物质的量分数与温度的关系如图所示: ℃时容器内几乎不发生反应Ⅲ的原因为
℃时容器内几乎不发生反应Ⅲ的原因为___________ 。
②若 ℃时,从反应开始到恰好达到平衡的时间为t min,则0~t min内,反应的平均速率
℃时,从反应开始到恰好达到平衡的时间为t min,则0~t min内,反应的平均速率
___________ (用含t的代数式表示)。
③温度高于 ℃时,容器内发生主要反应的热化学方程式为
℃时,容器内发生主要反应的热化学方程式为___________ 。
④ ℃时,反应Ⅰ的平衡常数
℃时,反应Ⅰ的平衡常数
___________ ( 是用平衡浓度表示的平衡常数)。
是用平衡浓度表示的平衡常数)。
⑤M、N点对应状态下继续反应一段时间,其平均反应速率 :M
:M___________ N(填“>”“<”或“=”),理由为___________ 。
(4)若起始以物质的量之比为1∶1向密闭容器中加入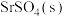 和
和 发生反应,达到平衡后,其他条件不变,改变下列条件,有利于提高
发生反应,达到平衡后,其他条件不变,改变下列条件,有利于提高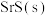 平衡产量的是
平衡产量的是___________ (填选项字母)。
A.适当升高温度 B.适当增大压强 C.使用更高效的催化剂
| 反应 | 焓变 /kJ·mol /kJ·mol | 熵变 /kJ·mol /kJ·mol ·K ·K |
Ⅰ. | +189.1 | 0.37 |
Ⅱ. | +534.0 | 0.72 |
Ⅲ.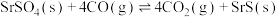 | -155.8 | 0.015 |
(1)Sr与Ca同族且相邻。基态Sr原子的电子排布式为
(2)反应Ⅰ、Ⅱ、Ⅲ中,自发进行所需温度最高的是
(3)将1 mol
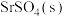 和3 mol
和3 mol 加入10 L恒容密闭容器中制备SrS,实验测得平衡体系中各成分的物质的量分数与温度的关系如图所示:
加入10 L恒容密闭容器中制备SrS,实验测得平衡体系中各成分的物质的量分数与温度的关系如图所示:
 ℃时容器内几乎不发生反应Ⅲ的原因为
℃时容器内几乎不发生反应Ⅲ的原因为②若
 ℃时,从反应开始到恰好达到平衡的时间为t min,则0~t min内,反应的平均速率
℃时,从反应开始到恰好达到平衡的时间为t min,则0~t min内,反应的平均速率
③温度高于
 ℃时,容器内发生主要反应的热化学方程式为
℃时,容器内发生主要反应的热化学方程式为④
 ℃时,反应Ⅰ的平衡常数
℃时,反应Ⅰ的平衡常数
 是用平衡浓度表示的平衡常数)。
是用平衡浓度表示的平衡常数)。⑤M、N点对应状态下继续反应一段时间,其平均反应速率
 :M
:M(4)若起始以物质的量之比为1∶1向密闭容器中加入
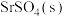 和
和 发生反应,达到平衡后,其他条件不变,改变下列条件,有利于提高
发生反应,达到平衡后,其他条件不变,改变下列条件,有利于提高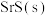 平衡产量的是
平衡产量的是A.适当升高温度 B.适当增大压强 C.使用更高效的催化剂
您最近一年使用:0次
解题方法
3 . 常用浓硫酸吸收工业废气中的 (NO与
(NO与 的混合气体)并制取亚硝基硫酸(
的混合气体)并制取亚硝基硫酸(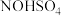 ),反应原理为
),反应原理为 。下列说法错误的是
。下列说法错误的是
 (NO与
(NO与 的混合气体)并制取亚硝基硫酸(
的混合气体)并制取亚硝基硫酸(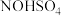 ),反应原理为
),反应原理为 。下列说法错误的是
。下列说法错误的是A. 分子的空间结构为平面三角形 分子的空间结构为平面三角形 |
B. 在水中电离方程式为 在水中电离方程式为 |
C.基态N原子的价层电子轨道表示式: |
| D.亚硝基硫酸分子与水分子可以形成分子间氢键 |
您最近一年使用:0次
4 . 一种从火法炼铜烟道灰(主要成分是 的硫酸盐,还有少量
的硫酸盐,还有少量 和
和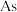 的氧化物)中回收铅,并制取三盐基硫酸铅(
的氧化物)中回收铅,并制取三盐基硫酸铅(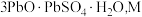 为
为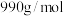 )的工艺如图:
)的工艺如图:
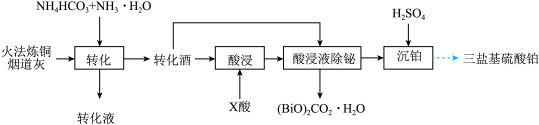
已知: 微溶于水
微溶于水
(1)写出铅原子的核外电子排布式:
_______ ,它位于元素周期表的_______ 区。
(2)转化过程温度选择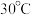 ,原因是
,原因是_______ 。
(3)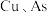 元素均进入转化液中,相关的离子分别为
元素均进入转化液中,相关的离子分别为_______ 、_______ (填离子符号)。
(4)转化渣主要成分为碳酸铅和碳酸氧铋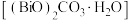 ,写出
,写出 转化为
转化为 的离子反应方程式:
的离子反应方程式:_______ 。
(5)加入适量的 酸,
酸, 酸宜为_______(填序号)。
酸宜为_______(填序号)。
(6)转化渣除铋的离子方程式为_______ 。
(7)若使用 烟道灰,最终制得纯度为
烟道灰,最终制得纯度为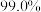 的三盐基硫酸铅
的三盐基硫酸铅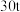 ,已知该工艺铅的回收率约为
,已知该工艺铅的回收率约为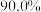 ,则烟道灰中含铅的质量分数为
,则烟道灰中含铅的质量分数为_______ 。
 的硫酸盐,还有少量
的硫酸盐,还有少量 和
和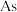 的氧化物)中回收铅,并制取三盐基硫酸铅(
的氧化物)中回收铅,并制取三盐基硫酸铅(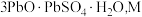 为
为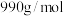 )的工艺如图:
)的工艺如图:
已知:
 微溶于水
微溶于水(1)写出铅原子的核外电子排布式:

(2)转化过程温度选择
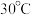 ,原因是
,原因是(3)
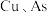 元素均进入转化液中,相关的离子分别为
元素均进入转化液中,相关的离子分别为(4)转化渣主要成分为碳酸铅和碳酸氧铋
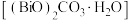 ,写出
,写出 转化为
转化为 的离子反应方程式:
的离子反应方程式:(5)加入适量的
 酸,
酸, 酸宜为_______(填序号)。
酸宜为_______(填序号)。| A.盐酸 | B.硫酸 | C.硝酸 | D.氢硫酸 |
(6)转化渣除铋的离子方程式为
(7)若使用
 烟道灰,最终制得纯度为
烟道灰,最终制得纯度为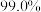 的三盐基硫酸铅
的三盐基硫酸铅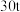 ,已知该工艺铅的回收率约为
,已知该工艺铅的回收率约为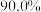 ,则烟道灰中含铅的质量分数为
,则烟道灰中含铅的质量分数为
您最近一年使用:0次
名校
5 . 科学家合成了一种含硼阴离子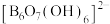 ,其结构如图所示下列叙述错误的是
,其结构如图所示下列叙述错误的是
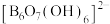 ,其结构如图所示下列叙述错误的是
,其结构如图所示下列叙述错误的是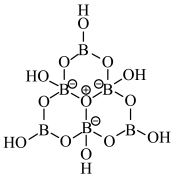
| A.基态硼原子的核外电子的空间运动状态有3种 |
| B.电负性大小为:O>B>H |
| C.该结构中硼原子的杂化方式为sp2、sp3 |
| D.该结构中共有4种不同化学环境的氧原子 |
您最近一年使用:0次
2024-05-01更新
|
561次组卷
|
3卷引用:2024届江西省南昌市第十九中学高三下学期模拟预测化学试题
解题方法
6 . 某化工厂利用废旧锂离子电池正极材料(含有LiCoO2以及少量Ca、Mg、Fe、Al、C等)制备Co2O3和Li2CO3。工艺流程如下:
①已知LiCoO2难溶于水,酸浸后的溶液中含有的部分金属离子有:Co2+、Fe2+、Al3+、Mg2+等;
②NaHCO3溶液中存在 的自耦电离:
的自耦电离: ;
;
③常温时,有关物质Ksp如下表:
(1)为了使拆解后的“正极材料”与酸充分反应,可采取的措施有___________ (任写一种)。
(2)元素Co在周期表中的位置为___________ ;Co2+价层电子轨道表示式为___________ 。
(3)“酸浸”时,LiCoO2参与反应的离子方程式为___________ ;下列试剂中最适宜替换H2C2O4的是___________ 。
A.Na2CO3溶液 B.Na2S2O5溶液 C.NaNO3溶液 D.浓盐酸
(4)滤渣1的主要成分有___________ 。
(5)加NaOH调节pH=10时,可以完全沉淀的金属离子有___________ (一般认为离子浓度≤10-5mol/L时,离子沉淀完全)。
(6)滤液3中含金属元素的离子主要是 ,则滤渣2与NH3∙H2O,(NH4)2CO3混合溶液主要反应的离子方程式为
,则滤渣2与NH3∙H2O,(NH4)2CO3混合溶液主要反应的离子方程式为___________ 。
(7)沉锂操作过程中需将温度升高到90℃,原因①是加快反应速率,并降低Li2CO3的溶解度②是(结合平衡原理解释)___________ 。

①已知LiCoO2难溶于水,酸浸后的溶液中含有的部分金属离子有:Co2+、Fe2+、Al3+、Mg2+等;
②NaHCO3溶液中存在
 的自耦电离:
的自耦电离: ;
;③常温时,有关物质Ksp如下表:
| 物质 |  |  |  |  |
| Ksp | 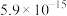 |  | 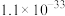 |  |
(1)为了使拆解后的“正极材料”与酸充分反应,可采取的措施有
(2)元素Co在周期表中的位置为
(3)“酸浸”时,LiCoO2参与反应的离子方程式为
A.Na2CO3溶液 B.Na2S2O5溶液 C.NaNO3溶液 D.浓盐酸
(4)滤渣1的主要成分有
(5)加NaOH调节pH=10时,可以完全沉淀的金属离子有
(6)滤液3中含金属元素的离子主要是
 ,则滤渣2与NH3∙H2O,(NH4)2CO3混合溶液主要反应的离子方程式为
,则滤渣2与NH3∙H2O,(NH4)2CO3混合溶液主要反应的离子方程式为(7)沉锂操作过程中需将温度升高到90℃,原因①是加快反应速率,并降低Li2CO3的溶解度②是(结合平衡原理解释)
您最近一年使用:0次
名校
解题方法
7 . 中医药学认为,雄黄(As4S4),外用可以治疗疥癣恶疮、蛇虫咬伤等;微量内服,可治惊痫、疮毒等症。雄黄遇热易氧化为As2O3(俗称砒霜),虽在古时常用做毒药,但科学家却发现它对治疗白血病有明显的作用。砷的其它化合物也在研究和生产中有着许多重要用途。____ ,核外电子占据的最高能级的电子云轮廓图形状为____ 。
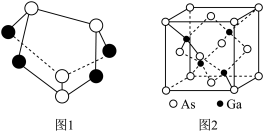
(2)雄黄(As4S4)的结构如上图1所示,As原子的杂化形式为_____ 。
(3)Na3AsO4常用作杀虫剂、防腐剂,它含有的化学键类型包括____ ;AsO43-的空间构型为_____ 。
(4)砷化镓是优良的半导体材料,其晶胞结构如图2所示。立方砷化镓晶体与立方氮化硼晶体结构类似,两种晶体中熔点较高的是____ ;砷化镓密度为 ,Ga和As原子半径分别为r1pm和r2pm,阿伏加德罗常数值为
,Ga和As原子半径分别为r1pm和r2pm,阿伏加德罗常数值为 ,则砷化镓晶体的空间利用率为
,则砷化镓晶体的空间利用率为_____ 。
(2)雄黄(As4S4)的结构如上图1所示,As原子的杂化形式为
(3)Na3AsO4常用作杀虫剂、防腐剂,它含有的化学键类型包括
(4)砷化镓是优良的半导体材料,其晶胞结构如图2所示。立方砷化镓晶体与立方氮化硼晶体结构类似,两种晶体中熔点较高的是
 ,Ga和As原子半径分别为r1pm和r2pm,阿伏加德罗常数值为
,Ga和As原子半径分别为r1pm和r2pm,阿伏加德罗常数值为 ,则砷化镓晶体的空间利用率为
,则砷化镓晶体的空间利用率为
您最近一年使用:0次
名校
解题方法
8 . 过渡金属元素铬( )是不锈钢的重要成分,在工农业生产和国防建设中有着广泛应用。回答下列问题:
)是不锈钢的重要成分,在工农业生产和国防建设中有着广泛应用。回答下列问题:
(1)请写出基态铬( )原子价电子的轨道表示式
)原子价电子的轨道表示式___________ 。
(2)超分子的定义是广义的,包括离子。一种羟甲基酚钠盐形成的含铁超分子的化学式为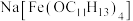 ,已知羟甲基酚属于杯酚,请写出该含铁超分子的一种特性:
,已知羟甲基酚属于杯酚,请写出该含铁超分子的一种特性:___________ 。
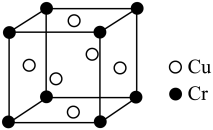
(3)某铜铬合金的立方晶胞结构如图所示。该铜铬合金的化学式为___________ ;离 原子最近的
原子最近的 原子数目为
原子数目为___________ ,离 原子最近的
原子最近的 原子数目为
原子数目为___________ 。若该晶胞参数为apm,则该晶体的密度为___________  。
。___________ 种。其同主族元素Si可形成硅酸盐,下图中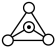 表示硅氧四面体,则该硅酸盐结构的通式为
表示硅氧四面体,则该硅酸盐结构的通式为___________ 。
 )是不锈钢的重要成分,在工农业生产和国防建设中有着广泛应用。回答下列问题:
)是不锈钢的重要成分,在工农业生产和国防建设中有着广泛应用。回答下列问题:(1)请写出基态铬(
 )原子价电子的轨道表示式
)原子价电子的轨道表示式(2)超分子的定义是广义的,包括离子。一种羟甲基酚钠盐形成的含铁超分子的化学式为
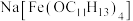 ,已知羟甲基酚属于杯酚,请写出该含铁超分子的一种特性:
,已知羟甲基酚属于杯酚,请写出该含铁超分子的一种特性:(3)某铜铬合金的立方晶胞结构如图所示。该铜铬合金的化学式为
 原子最近的
原子最近的 原子数目为
原子数目为 原子最近的
原子最近的 原子数目为
原子数目为 。
。
 表示硅氧四面体,则该硅酸盐结构的通式为
表示硅氧四面体,则该硅酸盐结构的通式为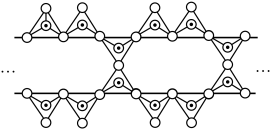
您最近一年使用:0次
名校
解题方法
9 . 氨硼烷(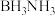 )是一种重要的储氢材料。1955年,Shore和Parry首次合成出氨硼烷。其反应如下:
)是一种重要的储氢材料。1955年,Shore和Parry首次合成出氨硼烷。其反应如下: 。下列说法错误的是
。下列说法错误的是
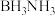 )是一种重要的储氢材料。1955年,Shore和Parry首次合成出氨硼烷。其反应如下:
)是一种重要的储氢材料。1955年,Shore和Parry首次合成出氨硼烷。其反应如下: 。下列说法错误的是
。下列说法错误的是A.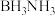 和 和 中均含有配位键 中均含有配位键 |
B.基态N原子核外价层电子排布图: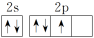 |
| C.上述反应涉及的第二周期元素中,电负性最大的是N |
D. 和 和 中, 中, 与 与 具有相似的空间结构 具有相似的空间结构 |
您最近一年使用:0次
2024-04-07更新
|
414次组卷
|
4卷引用:江西省部分地区2023-2024学年高三下学期3月月考化学试题
名校
10 . 下列关于晶体的说法正确的个数是
①2p、3p、4p能级的轨道数依次增加
②金刚石、NaF、NaCl、H2S、H2O晶体的熔点依次降低
③形成氢键的三个原子不一定在同一条直线上
④晶体中分子间作用力越大,分子越稳定
⑤HF晶体沸点高于HCl,是因为HCl共价键键能小于HF
⑥同周期,与Sc元素未成对电子数相等的元素有3种
⑦基态Cr3+的最高能层中成对电子与未成对电子的数目比为8:3
⑧元素Ge位于周期表第四周期ⅣA族,核外电子排布式为[Ar]4s24p2,属于P区
①2p、3p、4p能级的轨道数依次增加
②金刚石、NaF、NaCl、H2S、H2O晶体的熔点依次降低
③形成氢键的三个原子不一定在同一条直线上
④晶体中分子间作用力越大,分子越稳定
⑤HF晶体沸点高于HCl,是因为HCl共价键键能小于HF
⑥同周期,与Sc元素未成对电子数相等的元素有3种
⑦基态Cr3+的最高能层中成对电子与未成对电子的数目比为8:3
⑧元素Ge位于周期表第四周期ⅣA族,核外电子排布式为[Ar]4s24p2,属于P区
| A.2 | B.3 | C.4 | D.5 |
您最近一年使用:0次
2024-04-01更新
|
273次组卷
|
2卷引用:江西省南昌市第十九中学2023-2024学年高二下学期3月月考化学试题



