名校
1 . 下列说法错误的是
| A.能层序数较大的能级,能量不一定较高 |
B.某离子 层和 层和 层上的电子数均为 层上的电子数均为 层的4倍 层的4倍 |
C.原子核外每一能层最多可容纳的电子数为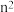 |
| D.存在核电荷数与最外层电子数相等的离子 |
您最近半年使用:0次
名校
解题方法
2 . 回答下列问题
(1)基态硫原子电子占据的最高能层符号为______ ,核外有______ 种能量不同的电子,硫原子核外电子有______ 种空间运动状态。
(2)与S同主族,位于第四周期的元素的符号是______ ,其价电子排布式为______
(3)已知有下列转化:
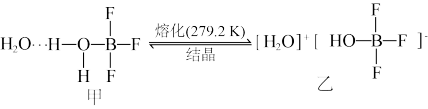
 的VSEPR模型为
的VSEPR模型为______ 。化合物乙中微粒间不存在的化学键有______ (填序号)。
A.离子键 B.共价键 C. 键 D.
键 D. 键 E.氢键
键 E.氢键
(4)相同条件下 与
与 分子在水中的溶解度较大的是
分子在水中的溶解度较大的是______ (写分子式),理由是______ 。 中的
中的 键角
键角______ (填“>”“<”或“=”) 中的
中的 键角。
键角。
(5)已知 是直线形分子,且有对称性,则
是直线形分子,且有对称性,则 分子的结构式为
分子的结构式为______ ,其中 键与
键与 键的个数比为
键的个数比为______ 。
(1)基态硫原子电子占据的最高能层符号为
(2)与S同主族,位于第四周期的元素的符号是
(3)已知有下列转化:
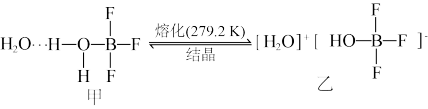
 的VSEPR模型为
的VSEPR模型为A.离子键 B.共价键 C.
 键 D.
键 D. 键 E.氢键
键 E.氢键(4)相同条件下
 与
与 分子在水中的溶解度较大的是
分子在水中的溶解度较大的是 中的
中的 键角
键角 中的
中的 键角。
键角。(5)已知
 是直线形分子,且有对称性,则
是直线形分子,且有对称性,则 分子的结构式为
分子的结构式为 键与
键与 键的个数比为
键的个数比为
您最近半年使用:0次
名校
3 . NA设为阿伏加德罗常数的值,下列说法正确的是
| A.40g处于基态的氩气中含有的p轨道电子总数为12NA |
| B.0.1mol/L的CH3COOH溶液中H+数目一定小于0.1NA |
| C.电解精炼含锌等杂质的粗铜,阴极增加64g,转移电子总数小于2NA |
D.100mL0.1mol/L的K2Cr2O7溶液中, 数目为0.01NA 数目为0.01NA |
您最近半年使用:0次
4 . 下列表述不正确 的是
A.原子轨道能量: |
| B.M电子层存在3个能级、9个原子轨道 |
| C.焰色试验中产生的火焰颜色是因为电子从基态跃迁到了激发态 |
| D.同一周期,碱金属元素的第一电离能最小,最容易失电子 |
您最近半年使用:0次
名校
5 . 第n电子层,其作为原子的最外层容纳的电子数最多与( )层的相同;当它作为次外层,其容纳的电子数比(
)层的相同;当它作为次外层,其容纳的电子数比( )层上电子数最多能多10个,第n层为
)层上电子数最多能多10个,第n层为
 )层的相同;当它作为次外层,其容纳的电子数比(
)层的相同;当它作为次外层,其容纳的电子数比( )层上电子数最多能多10个,第n层为
)层上电子数最多能多10个,第n层为| A.K层 | B.L层 | C.M层 | D.N层 |
您最近半年使用:0次
6 . 电子层数与该电子层中的能级数、原子轨道数有什么关系?能级与原子轨道数之间又有什么关系?______
您最近半年使用:0次
7 . 下列说法不正确 的是
A.氧原子可以形成 、 、 ,也可能形成 ,也可能形成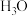 |
B.氯化铯晶体中,每个 周围紧邻且距离相等的 周围紧邻且距离相等的 共有6个 共有6个 |
C.同一原子中, 、 、 、 、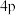 能级的轨道数目相等 能级的轨道数目相等 |
| D.缺角的氯化钠晶体在饱和氯化钠溶液中慢慢变为完美的立方体块 |
您最近半年使用:0次
名校
解题方法
8 . A、B、C、D、 E、F代表6种元素。请填空:
(1)A元素基态原子的最外层有3个未成对电子,次外层有2个电子,其元素符号为___________ 。
(2)B元素的负一价离子和C元素的正一价离子的电子层结构都与氩相同,B的元素符号为___________ ,C的元素符号为___________ 。
(3)D元素的正三价离子的3d能级为半充满,D的元素符号为___________
(4)E元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,E的元素符号为___________
(5)F元素的原子最外层电子排布式为nsnnpn+2,则n=___________ ;原子中能量最高的是___________ 电子。
(6)下列Li原子电子排布图表示的状态中,能量最低和最高的分别为___________ ,___________ (填标号)
A.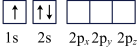 B.
B.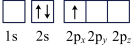 C.
C.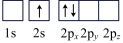 D.
D.
(7)Li+与H-具有相同的电子构型,r(Li+)小于r(H-),原因是___________ ,某原子的电子排布式为 [Ne]3s23p1,则该原子的元素符号为___________ ,最高正价为___________ ,该原子位于元素周期表第___________ 周期第___________ 族,位于元素周期表___________ 区。
(1)A元素基态原子的最外层有3个未成对电子,次外层有2个电子,其元素符号为
(2)B元素的负一价离子和C元素的正一价离子的电子层结构都与氩相同,B的元素符号为
(3)D元素的正三价离子的3d能级为半充满,D的元素符号为
(4)E元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,E的元素符号为
(5)F元素的原子最外层电子排布式为nsnnpn+2,则n=
(6)下列Li原子电子排布图表示的状态中,能量最低和最高的分别为
A.
 B.
B. C.
C. D.
D.
(7)Li+与H-具有相同的电子构型,r(Li+)小于r(H-),原因是
您最近半年使用:0次
9 . 密胺树脂是仿瓷餐具的主要成分,其反应中间体的结构简式如下。下列关于该中间体说法正确的是
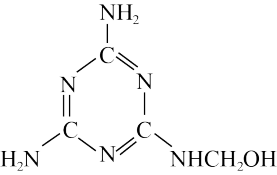

A.部分元素的第一电离能: |
| B.所有元素都处于元素周期表的p区 |
C.1个分子中采取 杂化的原子数为5 杂化的原子数为5 |
| D.基态碳原子最高能级的轨道形状为球形 |
您最近半年使用:0次
10 . 回答下列问题:
(1)基态Fe2+与Fe3+离子中未成对的电子数之比为___________ ,Sm的价层电子排布式4f66s2,Sm3+的价层电子排布式为___________ 。
(2)Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得。
①基态Cl原子中,电子占据的最高能层符号为___________ ,该能层具有的原子轨道数为___________ ,电子占据最高能级的电子云轮廓图为___________ 形。
②离子半径Li+___________ H-(填“>”“=”或“<”)。
(3)查表得知,元素X的电负性是1.5,元素Y的电负性是3.0,请判断X是___________ (填“金属”或“非金属”),该化合物中显负价的是___________ (填“X”或“Y”)。
(4) 的空间构型为
的空间构型为___________ ;O3是___________ 分子(填“极性”或“非极性”)。
(1)基态Fe2+与Fe3+离子中未成对的电子数之比为
(2)Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得。
①基态Cl原子中,电子占据的最高能层符号为
②离子半径Li+
(3)查表得知,元素X的电负性是1.5,元素Y的电负性是3.0,请判断X是
(4)
 的空间构型为
的空间构型为
您最近半年使用:0次



