1 . 氟化钠主要应用在涂装工业中做磷化促进剂、农业杀虫剂、防腐剂等各个领域。下列说法中正确的是
A.离子半径大小关系: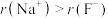 |
B.实验室盛放 溶液或 溶液或 溶液,可以用带玻璃塞的试剂瓶保存 溶液,可以用带玻璃塞的试剂瓶保存 |
| C.一般来说,同族元素从上到下元素电负性逐渐变小,第VIIA族中氟的电负性最大 |
D.基态钠原子中,其电子占据的最高能层的符号是 |
您最近一年使用:0次
名校
解题方法
2 . 元素周期表有许多有趣的编排方式,一种元素周期表的一部分如图所示,0、I~VIII均代表族序数,A~I代表不同的元素。
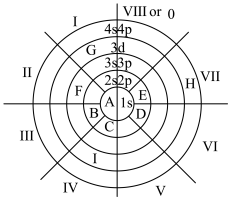
回答下列问题:
(1)H所代表的元素为_____ (填元素符号),I元素在周期表中的位置是_____ ,基态I原子的外围电子排布式为_____ 。
(2)图示周期表所列的元素中,电负性最大的元素是_____ (填元素符号,下同);B、C、D、E的第一电离能从大到小的顺序为_____ 。
(3)F、G分别与D形成的化合物中均含的键是_____ (填“离子键”或“共价键”),均属于_____ 晶体。
(4)利用图示周期表中所列元素,完成表格:(中心原子X上没有孤电子对,所用元素均为图中元素)

回答下列问题:
(1)H所代表的元素为
(2)图示周期表所列的元素中,电负性最大的元素是
(3)F、G分别与D形成的化合物中均含的键是
(4)利用图示周期表中所列元素,完成表格:(中心原子X上没有孤电子对,所用元素均为图中元素)
| XYn | 分子的空间结构 | 典型例子(填化学式) |
| n=2 | ① | ② |
| n=3 | ③ | ④ |
| n=4 | ⑤ | ⑥ |
您最近一年使用:0次
名校
3 . 下列是某同学学习相关知识后总结的规律,其中错误的是
A.Zn、Fe、Cu单质活泼性依次减弱, 、 、 、 、 氧化性依次增强 氧化性依次增强 |
B.一定温度下,一元弱酸HA的 越小,则NaA的 越小,则NaA的 越大 越大 |
C.电解时, 、 、 、 、 放电能力依次减弱, 放电能力依次减弱, 、 、 、 、 氧化性依次增强 氧化性依次增强 |
| D.元素的电负性越大,该原子的第一电离能越大 |
您最近一年使用:0次
11-12高二·全国·课时练习
名校
4 . 下列各组元素的性质正确的是
| A.第一电离能:B>Al>Ga | B.电负性:F>N>O |
| C.最高正价:F>S>Si | D.原子半径:P>N>C |
您最近一年使用:0次
2019-04-20更新
|
293次组卷
|
17卷引用:河北省蠡县中学2016-2017学年高二6月月考化学试题
河北省蠡县中学2016-2017学年高二6月月考化学试题河北省保定市崇德实验中学2020-2021学年度高二下学期期中考试化学试题(已下线)2012年人教版高中化学选修3 1.2原子结构与元素的性质练习卷2014-2015山西省太原市五中高二上学期期末化学理试卷2015-2016学年湖北省黄香、航天等校高二下学期期末联化学试卷2017届河南信阳高考化学暑假自学自测专练:原子结构与性质内蒙古包头市第三十三中学2016-2017学年高二下学期期末考试化学试题宁夏回族自治区银川市长庆高级中学2018-2019学年高二下学期第二次月考化学试题人教化学选修3第一章第二节课时4河北省正定中学2019-2020学年高二3月线上月考化学试题河北省邢台市2019-2020学年高二下学期期末考试化学试题河北省沧州市任丘市第一中学2019-2020学年高二6月月考化学试题宁夏长庆高级中学2020-2021学年高二上学期期中考试化学试卷辽宁省清原满族自治县第二高级中学2020-2021学年高二下学期期中考试化学试题云南省景东彝族自治县第一中学2021-2022学年高二下学期3月份考试化学试题新疆乌鲁木齐市第四中学2021-2022学年高二下学期期末考试化学试题新疆生产建设兵团第六师芳草湖农场中学2021-2022学年高二上学期期末考试化学试题
名校
解题方法
5 . 邻氨基吡啶的铜配合物在有机不对称合成中起催化诱导效应,其结构简式如图所示。下列相关说法正确的是
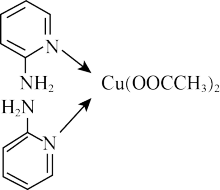

A.Cu原子的价电子排布图为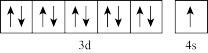 |
| B.组成该配合物的第二周期元素的电负性大小顺序为N>O>C |
| C.所有N原子的杂化方式相同,所有C原子的杂化方式也相同 |
D.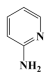 分子中可能有13个原子在同一平面上 分子中可能有13个原子在同一平面上 |
您最近一年使用:0次
解题方法
6 . 现有4种元素的基态原子的电子排布式如下:①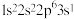 ;②
;②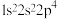 ;③
;③ ;④
;④ 。下列比较中,正确的是
。下列比较中,正确的是
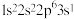 ;②
;②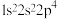 ;③
;③ ;④
;④ 。下列比较中,正确的是
。下列比较中,正确的是| A.非金属性:④>②>③>① | B.简单离子半径:①>③>②>④ |
| C.原子半径:①>④>③>② | D.元素的电负性:④>③>①>② |
您最近一年使用:0次
2022-07-03更新
|
131次组卷
|
2卷引用:河北省保定市2021-2022学年高二下学期期末考试化学试题
名校
解题方法
7 . 一种可用作有机化工原料的化合物Q的结构如图。已知X、Y、Z、W、M为原子序数依次增大的主族元素,其中X的核电荷数等于其主族序数,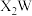 是常温下常见的液态化合物,基态Y原子核外未成对电子数与基态W原子核外未成对电子数相等,M的单质是常温下唯一的液态非金属单质。下列说法正确的是
是常温下常见的液态化合物,基态Y原子核外未成对电子数与基态W原子核外未成对电子数相等,M的单质是常温下唯一的液态非金属单质。下列说法正确的是
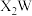 是常温下常见的液态化合物,基态Y原子核外未成对电子数与基态W原子核外未成对电子数相等,M的单质是常温下唯一的液态非金属单质。下列说法正确的是
是常温下常见的液态化合物,基态Y原子核外未成对电子数与基态W原子核外未成对电子数相等,M的单质是常温下唯一的液态非金属单质。下列说法正确的是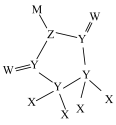
| A.原子半径:W>Z>Y | B.第一电离能:Z>W>Y |
| C.电负性:M>W>Z | D.键角: |
您最近一年使用:0次
2024-05-22更新
|
162次组卷
|
4卷引用:2024届河北省保定市十校高三下学期三模化学试题
名校
解题方法
8 . 元素周期表前四周期A、B、C、D、E五种元素,A元素的原子最外层电子排布式为ns1;B元素的原子价层电子排布式为ns2np2;C元素位于第二周期且原子中p能级与s能级电子总数相等;D元素原子的M能层的p能级中有3个未成对电子;E元素的原子有5个未成对电子。
(1)写出元素名称:C___________ 、D___________ 、E___________ 。
(2)C基态原子的轨道表示式为___________ 。
(3)与D元素同周期中第一电离能比D小的元素有___________ 种。
(4)当n=2时,BC2分子的电子式为___________ ;当n=3时,B与C形成的化合物与氢氧化钠溶液反应的离子方程式是___________ 。
(5)若A元素的原子最外层电子排布式为2s1,B元素的原子价层电子排布式为3s23p2,A、B、C、D四种元素的电负性由大到小的顺序是___________ (用元素符号表示)。
(6)E元素原子的价层电子排布式是___________ ,其最高价氧化物的化学式是___________ 。
(1)写出元素名称:C
(2)C基态原子的轨道表示式为
(3)与D元素同周期中第一电离能比D小的元素有
(4)当n=2时,BC2分子的电子式为
(5)若A元素的原子最外层电子排布式为2s1,B元素的原子价层电子排布式为3s23p2,A、B、C、D四种元素的电负性由大到小的顺序是
(6)E元素原子的价层电子排布式是
您最近一年使用:0次
名校
解题方法
9 . 下列物质的结构或性质及解释均正确且具有因果关系的是
| 选项 | 物质的结构或性质 | 解释 |
| A | 硬度;SiC>Si | 晶体类型不同 |
| B | 分解温度: | 相对分子质量越大,范德华力越大 |
| C |  在 在 中的榕解度大于在 中的榕解度大于在 中的溶解度 中的溶解度 |  的相对分子质量大于 的相对分子质量大于 的相对分子质量 的相对分子质量 |
| D | 酸性: | 氟的电负性大于氯的电负性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-05-21更新
|
105次组卷
|
2卷引用:2024届河北省保定市十校高三下学期三模化学试题
名校
10 . 下列说法中错误的是
| A.根据对角线规则,铍和铝的性质具有相似性 |
| B.[Cu(H2O)4]2+中Cu提供空轨道,H2O中O提供孤对电子形成配位键 |
| C.元素电负性越大的原子,吸引电子的能力越强 |
| D.手性分子互为镜像,它们的性质没有区别 |
您最近一年使用:0次
2016-12-09更新
|
520次组卷
|
5卷引用:河北省保定市保定三中2016-2017学年度第二学期3月月考高二化学试题



