名校
1 . Ti、Na、Mg、C、N、O、Fe等元素的研究一直在进行中,其单质及化合物在诸多领域都有广泛的应用。回答下列问题:
(1)钠在火焰上灼烧的黄光是一种___________ (填字母)。
A.吸收光谱 B.发射光谱
(2)下列Mg原子的核外电子排布式中,能量最高的是___________ ,能量最低的是___________ (填序号)。
a. b.
b.
c. d.
d.
(3)Ti原子位于元素周期表中的___________ 区,最高能层电子的电子云轮廓形状为___________ ,其价电子排布式为___________ 。与Ti同周期的过渡元素中,未成对电子数最多的的基态原子的外围电子的轨道表示式___________ 。
(4)Fe3+与Fe2+的离子半径大小关系为Fe3+___________ Fe2+(填“大于”或“小于”)
(5)下列各组多电子原子的能级能量比较不正确的是___________
①2p=3p ②4s>2s ③4p>4f ④4d>3d
(1)钠在火焰上灼烧的黄光是一种
A.吸收光谱 B.发射光谱
(2)下列Mg原子的核外电子排布式中,能量最高的是
a.
 b.
b.
c.
 d.
d.
(3)Ti原子位于元素周期表中的
(4)Fe3+与Fe2+的离子半径大小关系为Fe3+
(5)下列各组多电子原子的能级能量比较不正确的是___________
①2p=3p ②4s>2s ③4p>4f ④4d>3d
| A.①④ | B.①③ | C.③④ | D.②③ |
您最近一年使用:0次
2022-02-18更新
|
1336次组卷
|
7卷引用:河北省邯郸市大名县第一中学2021-2022学年高二上学期第二次月考化学试题
解题方法
2 . 食用碱是人们生活中常用的食品疏松剂和肉类嫩化剂,其成分为纯碱 和小苏打
和小苏打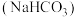 。下列说法正确的是
。下列说法正确的是
 和小苏打
和小苏打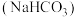 。下列说法正确的是
。下列说法正确的是A.离子半径: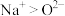 | B.电负性: |
C.非金属性: | D.第一电离能: |
您最近一年使用:0次
2023-12-01更新
|
550次组卷
|
5卷引用:河北省邯郸市六校联考2023-2024学年高二上学期11月月考化学试题
解题方法
3 . 氢气和二氧化碳在催化剂作用下,在180-280℃温度下合成甲醇,该反应放热。催化过程可解释为“吸附-活化-解离”,催化反应机理如图所示。下列说法正确的是
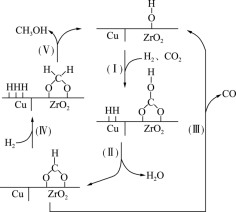
| A.反应过程中I-V步,C化合价不变 |
| B.单位时间内,生成水越多,甲醇产率越大 |
| C.增大催化剂的表面积,可以提高甲醇的平衡产率 |
| D.因为电负性O>C,所以CO2中的C与吸附在氧化锆晶格表面的OH上的O原子结合 |
您最近一年使用:0次
2023-05-18更新
|
551次组卷
|
2卷引用:河北省邯郸市2023届高考第三次模拟(保温卷)化学试题
名校
解题方法
4 . 磷酸铁锂(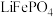 )电极材料主要用于各种锂离子电池。回答下列问题
)电极材料主要用于各种锂离子电池。回答下列问题
(1)Fe位于元素周期表中第___________ 周期第___________ 族,其外围电子排布式为___________ 。
(2)离子半径: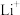
___________  ;第一电离能:Li
;第一电离能:Li___________ Be;电负性:O___________ P。(填“>”“<”或“=”)
(3)下列Li的轨道表示式表示的状态中,能量最低和最高的分别为___________ 、___________ (填标号)。
A. B.
B.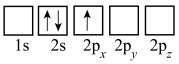
C.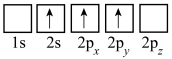 D.
D.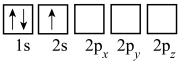
(4)基态P中未成对的电子数为___________ ,其原子核外电子占据的最高能级的电子云轮廓为___________ 形。
(5)Mn与Fe两元素的部分电离能数据如下,由表中两元素的 和
和 可知,气态
可知,气态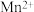 再失去一个电子比气态
再失去一个电子比气态 再失去一个电子更难,对此,你的解释是
再失去一个电子更难,对此,你的解释是___________ 。
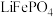 )电极材料主要用于各种锂离子电池。回答下列问题
)电极材料主要用于各种锂离子电池。回答下列问题(1)Fe位于元素周期表中第
(2)离子半径:
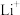
 ;第一电离能:Li
;第一电离能:Li(3)下列Li的轨道表示式表示的状态中,能量最低和最高的分别为
A.
 B.
B.
C.
 D.
D.
(4)基态P中未成对的电子数为
(5)Mn与Fe两元素的部分电离能数据如下,由表中两元素的
 和
和 可知,气态
可知,气态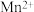 再失去一个电子比气态
再失去一个电子比气态 再失去一个电子更难,对此,你的解释是
再失去一个电子更难,对此,你的解释是| 元素 | Mn | Fe | |
| 电离能(kJ/mol) |  | 717 | 759 |
 | 1509 | 1561 | |
 | 3248 | 2957 |
您最近一年使用:0次
2024-02-11更新
|
509次组卷
|
2卷引用:河北省邯郸市永年区第二中学2023-2024学年高二上学期12月月考化学试题
名校
5 . 短周期元素X、Y、Z、W、E原子核外电子数依次增多。X的原子半径是短周期元素中最小的;Y、Z、W位于同一周期,Z元素基态原子中p轨道所含电子数与s轨道相等;E与W同主族。它们组成的某种分子的结构式如图所示,下列说法正确的是
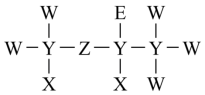
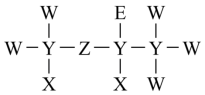
A.简单阴离子半径: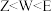 |
| B.同主族元素中E的最高价氧化物对应水化物的酸性最强 |
C.电负性: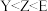 |
D.离子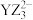 的中心原子的杂化方式是 的中心原子的杂化方式是 杂化 杂化 |
您最近一年使用:0次
2022-01-27更新
|
648次组卷
|
5卷引用:河北鸡泽县第一中学2021-2022学年高二下学期开学考试化学试题
解题方法
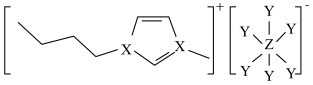
6 . 大多数离子液体含有体积很大的阴、阳离子,某离子液体结构如图所示,其中X、Y、Z为原子序数依次增大的短周期非金属元素,X、Z同主族。该物质可通过以物质M(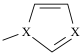 ,含有大π键,表示为Π
,含有大π键,表示为Π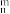 ,n为参与形成大π键的原子个数,m为参与形成大π键的电子个数)为原料合成得到。下列说法正确的是
,n为参与形成大π键的原子个数,m为参与形成大π键的电子个数)为原料合成得到。下列说法正确的是
 ,含有大π键,表示为Π
,含有大π键,表示为Π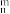 ,n为参与形成大π键的原子个数,m为参与形成大π键的电子个数)为原料合成得到。下列说法正确的是
,n为参与形成大π键的原子个数,m为参与形成大π键的电子个数)为原料合成得到。下列说法正确的是
| A.第一电离能:Y>X>Z | B.X2Y2分子为直线形分子 |
C.M分子中存在的大π键为Π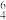 | D.电负性:X>Y>Z |
您最近一年使用:0次
解题方法
7 . 治疗新冠肺炎药物瑞德西韦的主要成分结构如图。下列说法错误的是


A.分子中存在 键、 键、 键 键 |
B.分子中的 键的键能小于 键的键能小于 键的键能 键的键能 |
C.分子中N、O、P原子的第一电离能由大到小的关系为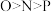 |
| D.分子中含有手性碳原子 |
您最近一年使用:0次
2022-01-23更新
|
447次组卷
|
4卷引用:河北鸡泽县第一中学2021-2022学年高二下学期开学考试化学试题
河北鸡泽县第一中学2021-2022学年高二下学期开学考试化学试题辽宁省锦州市2021-2022学年高二上学期期末考试化学试题(已下线)第二章 分子结构与性质 章节过关检测-2021-2022学年高二化学链接教材精准变式练(人教版2019选择性必修2)山东省烟台市华夏学校2021-2022学年高二上学期期中考试化学试题
名校
解题方法
8 . 现有三种元素的基态原子的电子排布式如下:
①1s22s22p63s23p4;②1s22s22p63s23p3;③1s22s22p5。
则下列有关比较中正确的是
①1s22s22p63s23p4;②1s22s22p63s23p3;③1s22s22p5。
则下列有关比较中正确的是
| A.第一电离能:③>②>① |
| B.原子半径:③>②>① |
| C.电负性:③>②>① |
| D.最高正化合价:③>②>① |
您最近一年使用:0次
2021-12-04更新
|
1046次组卷
|
92卷引用:河北省馆陶县第一中学2016-2017学年高二下学期期末考试化学试题
河北省馆陶县第一中学2016-2017学年高二下学期期末考试化学试题(已下线)2009一2010年度吉林一中下学期高二期中考试化学卷(已下线)2010年厦门一中高二暑期水平测试(已下线)09-10年辽宁大连23中高二下学期期末考试化学卷(已下线)09~10年牡丹江一中高二下学期期末考试化学卷(已下线)2011-2012学年四川省南山中学高二上学期期末模拟考试化学试卷(已下线)2011--2012学年四川省成都二十中高二上学期期中考试化学试卷(已下线)2011-2012学年山西省忻州一中高二下学期第一次月考化学试卷(已下线)2011-2012学年黑龙江省鹤岗一中高二下学期期中考试化学试卷(已下线)2011-2012学年湖北省武汉市五校高二下学期期中统考化学试卷(已下线)2011-2012年黑龙江龙东地区高二下学期期末考试化学试卷(已下线)2011-2012学年辽宁省沈阳二中高二下学期期中考试化学试卷(已下线)2012-2013学年黑龙江省鹤岗一中高二下学期期中考试化学试卷(已下线)2012-2013学年辽宁葫芦岛第一高级中学高二下学期期中考试化学试卷(已下线)2012-2013学年山东省济南一中高二下学期期中考试理科化学试卷(已下线)2012-2013学年黑龙江省鹤岗一中高二下学期期末考试化学试卷(已下线)2013届浙江省台州中学高三第一次统练化学试卷(已下线)2013-2014广西桂林中学高二下学期期中考试化学试卷(已下线)2013-2014黑龙江省鹤岗一中高二下学期期末考试化学试卷2014-2015江苏省射阳县盘湾中学高二上学期期末考试化学试卷2013-2014山东省即墨市高二下学期期中考试化学试卷2014-2015学年辽宁省沈阳市沈阳二中高二下期中化学试卷2014-2015学年湖北省部分重点高中高二下期末考试化学试卷2016届浙江省慈溪中学高三上学期期中考试化学试卷2015-2016学年四川省雅安市天全中学高二上学期期中测试化学试卷2015-2016学年安徽省六安一中高二上学期期末化学试卷2015-2016学年福建省师大附中高二上学期期末化学试卷2015-2016学年吉林省汪清六中高二3月月考化学试卷2015-2016学年吉林省辽源市田家炳高中高二下期中化学试卷2015-2016学年吉林省扶余一中高二下学期期中考试化学试卷2015-2016学年云南省德宏州芒一中高二下学期期末化学试卷2015-2016学年吉林省汪清六中高二下学期期末化学试卷2016-2017学年河南省郑州市第一中学高二下学期入学测试理综化学试卷2016-2017学年黑龙江哈三中高二下学期4月月考(验收)考试化学试卷河南省郑州市八校2016-2017学年高二下学期期中联考化学试题江苏省泰州市姜堰区2016-2017学年高二下学期期中考试化学试题山西省大同市第一中学2016-2017学年高二5月月考化学试题河北省唐山市开滦第二中学2016-2017学年高二6月月考化学试题福建省三明市第一中学2016-2017学年高二下学期第二次月考化学试题新疆呼图壁县第一中学2016-2017学年高二下学期期末考试化学试题河南省焦作市博爱一中2016-2017学年高二下学期第一次月考化学试题辽宁省实验中学分校2016-2017学年高二6月月考化学试题2017-2018学年人教版高中化学选修三 模块综合质量检测河北省石家庄市鹿泉一中2017-2018学年高二3月月考化学试题【全国百强校】内蒙古集宁一中(东校区)2017-2018学年高二下学期期中考试化学试题【全国百强校】广东省佛山市第一中学2017-2018学年高二下学期期中考试(理)化学试题【全国百强校】广东省中山市第一中学2017-2018学年高二下学期第二次段考化学试题河南省济源第一中学2017-2018学年高二下期6月月考化学试题陕西省西安中学2017-2018学年高二(平行班)下学期期末考试化学试题山东省微山县第二中学2018-2019学年高二上学期第三学段教学质量监测化学试题吉林省吉林市第五十五中学2018-2019学年高二下学期3月月考化学试题【全国百强校】内蒙古自治区赤峰市第二中学2018-2019学年高二下学期4月月考化学试题山西省阳泉市第二中学2018-2019学年高二下学期期中考试化学试题福建省平和县第一中学2018-2019学年高二下学期第二次月考化学试题黑龙江省哈尔滨市阿城区第二中学2018-2019学年高二下学期期中考试化学试题陕西省西安中学2018-2019学年高二下学期期末考试化学试题甘肃省临泽县第一中学2018-2019学年高二下学期期末考试化学试题甘肃省张掖市临泽一中2018-2019学年高二下学期期末考试化学试题河北省秦皇岛市卢龙中学2018-2019学年高二下学期期末考试化学试题湖北省宜昌市第二中学2018-2019学年高二上学期期中考试化学试题辽宁省实验中学东戴河分校2019-2020学年高二12月月考化学试题河北省石家庄市启明中学2019-2020学年高二四月月考化学试题吉林省辽源市东辽县第一高级中学2019-2020高二5月月考化学试题宁夏银川市长庆高级中学2019-2020学年高二下学期期中考试化学试题山西省晋中市平遥中学2019-2020高二下学期在线学习质量检测化学试题山西省忻州市第二中学2019-2020高二下学期3月考试化学试题陕西省西安市西北工业大学附属中学2019-2020学年高二下学期5月考试化学试题陕西省宝鸡市渭滨区2019-2020学年高二下学期期末考试化学试题宁夏青铜峡市高级中学(吴忠中学青铜峡分校)2019-2020学年高二下学期期末考试化学试题吉林省吉林地区普通高中友好学校联合体第三十届基础年段2019-2020学年高二下学期期末联考化学试题山西省晋中市祁县中学校2019-2020学年高二下学期6月月考化学试题陕西省咸阳市实验中学2020-2021学年高二上学期第一次月考化学试题天津市宝坻区宝坻九中2021届高三上学期第一次月考化学试题四川省内江市威远中学2020-2021学年高二上学期期中考试化学试题(鲁科版2019)选择性必修2 第1章 原子结构与元素性质 第3节 元素性质及其变化规律(已下线)第1章 原子结构与元素性质(基础过关)-2020-2021学年高二化学单元测试定心卷(鲁科版2019选择性必修2)新疆维吾尔自治区新源县第二中学2019-2020学年高二上学期第一次阶段测试化学试题吉林省吉化第一高级中学校2020-2021学年高二下学期3月月考化学试题新疆新源县第二中学2018-2019学年高二下学期期末考试化学试题吉林省通化县综合高级中学2020-2021学年高二下学期期中考试化学试题宁夏青铜峡市高级中学2020-2021学年高二下学期期中考试化学试题甘肃省兰州市第二十七中学2022届高三上学期8月月考化学试题河北省石家庄市第一中学2019-2020学年高二下学期第一次月考化学试题(已下线)第30讲 原子结构与性质(讲) — 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)北京市第四中学2021-2022学年高二上学期期末考试化学试题吉林省长春市第八中学2021-2022学年高二下学期线上月考化学试题福建省福州市四校联盟2021-2022学年高二下学期期中联考化学试题福建省建瓯市芝华中学2021-2022学年高二下学期第一次阶段考化学试题四川省平昌县得胜中学2021-2022学年高二上学期10月月考化学试题宁夏吴忠市吴忠中学2022-2023学年高三上学期阶段性测试 化学试题辽宁省大石桥市第三高级中学2021-2022学年高二12月月考化学试题宁夏青铜峡市宁朔中学2022-2023学年高二下学期期中考试化学试题
解题方法
9 . 磷酸铁锂(LiFePO4)电极材料主要用于各种锂离子电池。回答下列问题。
(1)Fe 位于元素周期表中第___________ 周期第___________ 族,其价层电子排布式为___________ 。
(2)用“>”“<”或“=”填空:离子半径:Li+___________ H-;第一电离能:Li___________ Be;电负性:O___________ P。
(3)在周期表中,与 Li 化学性质相似的邻族元素是___________ 。
(4)下列 Li 原子轨道表示式表示的状态中,能量最低和最高的分别为___________ 、___________ (填字母)。
A. B.
B.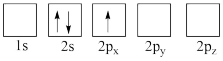
C.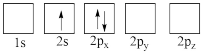 D.
D.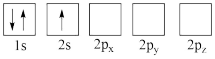
(5)基态 P 中未成对电子数为___________ ,其原子核外电子占据的最高能级的电子云轮廓图为___________ 形。
(1)Fe 位于元素周期表中第
(2)用“>”“<”或“=”填空:离子半径:Li+
(3)在周期表中,与 Li 化学性质相似的邻族元素是
(4)下列 Li 原子轨道表示式表示的状态中,能量最低和最高的分别为
A.
 B.
B.
C.
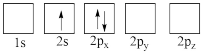 D.
D.
(5)基态 P 中未成对电子数为
您最近一年使用:0次
名校
解题方法
10 . 现有四种元素的基态原子的核外电子排布式如下:①1s22s22p3;②1s22s22p4;③1s22s22p63s23p2;④1s22s22p63s23p3。下列说法错误的是
| A.电负性:②>①>④>③ |
| B.原子半径:③>④>①>② |
| C.第一电离能:②>①>④>③ |
| D.简单气态氢化物的稳定性:②>①>④>③ |
您最近一年使用:0次
2022-01-24更新
|
517次组卷
|
3卷引用:河北省邯郸市永年区第二中学2023-2024学年高二上学期12月月考化学试题



