1 . 以 、ZnO等半导体材料制作的传感器和芯片具有能耗低、效率高的优势。回答问题:
、ZnO等半导体材料制作的传感器和芯片具有能耗低、效率高的优势。回答问题:
(1)基态O原子的电子排布式_______ ,其中未成对电子有_______ 个。
(2)Cu、Zn等金属具有良好的导电性,从金属键的理论看,原因是_______ 。
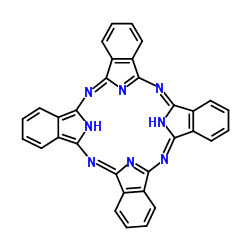
(3)酞菁的铜、锌配合物在光电传感器方面有着重要的应用价值。酞菁分子结构如下图,分子中所有原子共平面,所有N原子的杂化轨道类型相同,均采取_______ 杂化。邻苯二甲酸酐( )和邻苯二甲酰亚胺(
)和邻苯二甲酰亚胺(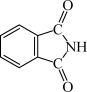 )都是合成酞菁的原料,后者熔点高于前者,主要原因是
)都是合成酞菁的原料,后者熔点高于前者,主要原因是_______ 。
(4)金属Zn能溶于氨水,生成以氨为配体,配位数为4的配离子,Zn与氨水反应的离子方程式为_______ 。
(5)ZnO晶体中部分O原子被N原子替代后可以改善半导体的性能,Zn-N键中离子键成分的百分数小于Zn-O键,原因是_______ 。
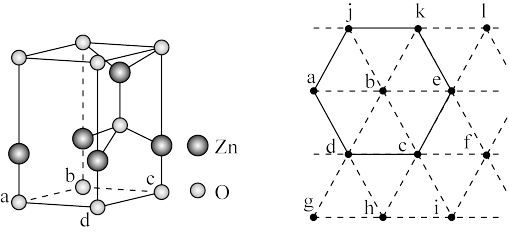
(6)下图为某ZnO晶胞示意图,下图是若干晶胞无隙并置而成的底面O原子排列局部平面图。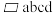 为所取晶胞的下底面,为锐角等于60°的菱形,以此为参考,用给出的字母表示出与所取晶胞相邻的两个晶胞的底面
为所取晶胞的下底面,为锐角等于60°的菱形,以此为参考,用给出的字母表示出与所取晶胞相邻的两个晶胞的底面_______ 、_______ 。
 、ZnO等半导体材料制作的传感器和芯片具有能耗低、效率高的优势。回答问题:
、ZnO等半导体材料制作的传感器和芯片具有能耗低、效率高的优势。回答问题:(1)基态O原子的电子排布式
(2)Cu、Zn等金属具有良好的导电性,从金属键的理论看,原因是
(3)酞菁的铜、锌配合物在光电传感器方面有着重要的应用价值。酞菁分子结构如下图,分子中所有原子共平面,所有N原子的杂化轨道类型相同,均采取
 )和邻苯二甲酰亚胺(
)和邻苯二甲酰亚胺( )都是合成酞菁的原料,后者熔点高于前者,主要原因是
)都是合成酞菁的原料,后者熔点高于前者,主要原因是
(4)金属Zn能溶于氨水,生成以氨为配体,配位数为4的配离子,Zn与氨水反应的离子方程式为
(5)ZnO晶体中部分O原子被N原子替代后可以改善半导体的性能,Zn-N键中离子键成分的百分数小于Zn-O键,原因是
(6)下图为某ZnO晶胞示意图,下图是若干晶胞无隙并置而成的底面O原子排列局部平面图。
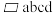 为所取晶胞的下底面,为锐角等于60°的菱形,以此为参考,用给出的字母表示出与所取晶胞相邻的两个晶胞的底面
为所取晶胞的下底面,为锐角等于60°的菱形,以此为参考,用给出的字母表示出与所取晶胞相邻的两个晶胞的底面
您最近半年使用:0次
2022-07-04更新
|
8909次组卷
|
11卷引用:2022年海南省高考真题化学试题
2022年海南省高考真题化学试题(已下线)2022年海南省高考真题变式题15-19(已下线)专题17 物质结构与性质(综合题)-2022年高考真题模拟题分项汇编(已下线)第19练 物质结构与性质综合题难点突破-2022年【暑假分层作业】高二化学(2023届一轮复习通用)山西省晋中市祁县中学2022-2023学年高三上学期10月月考化学试题(已下线)热点情景汇编-专题十四 结构性质中的新材料(已下线)【知识图鉴】单元讲练测选择性必修2第三章03单元测(已下线)专题九 物质结构与性质-实战高考·二轮复习核心突破(已下线)专题20 结构与性质(已下线)专题20 结构与性质(已下线)专题17 物质结构与性质综合题-2023年高考化学真题题源解密(新高考专用)
名校
解题方法
2 . X、Y、Z、W、P、Q为短周期元素,其中Y的原子序数最小,它们的最高正价与原子半径关系如图所示。下列说法正确的是


| A.Y在元素周期表中位于p区 | B.第一电离能: |
C.氧化物对应水化物的酸性: | D.电负性: |
您最近半年使用:0次
2023-06-22更新
|
1018次组卷
|
5卷引用:海南省海南中学2023-2024学年高三下学期第6次月考化学试题
海南省海南中学2023-2024学年高三下学期第6次月考化学试题广东省惠州市2024届高三第一次调研考试化学试题(已下线)第19讲元素周期律与元素周期表(已下线)考点18 元素周期律与元素周期表(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)广东省深圳市福田区福田中学2023-2024学年高三上学期12月月考化学考试
名校
3 . 科学家通过观察金星的酸性云层,分析出金星存在磷化氢气体,从而推测金星可能存在生命的迹象。下列关于P元素的说法中,不正确 的是
| A.第一电离能:P<S | B.原子半径:S<P |
| C.非金属性:P<S | D.电负性:P<S |
您最近半年使用:0次
2022-03-10更新
|
809次组卷
|
7卷引用:海南省儋州川绵中学2021-2022学年高二下学期第二次月考化学试题
2018·四川攀枝花·二模
名校
4 . 含氮、磷化合物在生活和生产中有许多重要用途,如:(CH3)3N、磷化硼(BP)、磷青铜(Cu3SnP)等。
回答下列问题:
(1)锡(Sn)是第五周期ⅣA元素。基态锡原子的价电子排布式为_________ ,据此推测,锡的最高正价是_________ 。
(2)与P同周期的主族元素中,电负性比P小的元素有____ 种 ,第一电离能比P大有____ 种。
(3)PH3分子的空间构型为___________ 。PH3的键角小于NH3的原因是__________ 。
(4)化合物(CH3)3N能溶于水,试解析其原因____________ 。
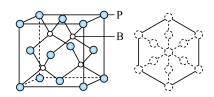
(5)磷化硼是一种耐磨涂料,它可用作金属的表面保护层。磷化硼晶体晶胞如图所示:
①在一个晶胞中磷原子空间堆积方式为________ ,磷原子的配位数为________ 。
②已知晶胞边长a pm,阿伏伽德罗常数为NA。则磷化硼晶体的密度为______ g/cm3。
③磷化硼晶胞沿着体对角线方向的投影如图,请将表示B原子的圆圈涂黑________ 。
回答下列问题:
(1)锡(Sn)是第五周期ⅣA元素。基态锡原子的价电子排布式为
(2)与P同周期的主族元素中,电负性比P小的元素有
(3)PH3分子的空间构型为
(4)化合物(CH3)3N能溶于水,试解析其原因

(5)磷化硼是一种耐磨涂料,它可用作金属的表面保护层。磷化硼晶体晶胞如图所示:
①在一个晶胞中磷原子空间堆积方式为
②已知晶胞边长a pm,阿伏伽德罗常数为NA。则磷化硼晶体的密度为
③磷化硼晶胞沿着体对角线方向的投影如图,请将表示B原子的圆圈涂黑
您最近半年使用:0次
2019-02-13更新
|
2515次组卷
|
8卷引用:2020年海南卷化学高考真题变式题15-19
(已下线)2020年海南卷化学高考真题变式题15-19【市级联考】四川省攀枝花市2019届高三上学期第二次统考化学试题【市级联考】山东省泰安市2019届高三下学期二轮模拟考试理科综合化学试题江西省上饶市2020届第一次高考模拟考试理科综合化学试题解题达人.化学选择题(2021全国卷)精编特训06(已下线)2021年高考全国甲卷化学试题变式题2020年全国卷Ⅰ理综化学高考真题变式题河南省驻马店市新蔡县第一高级中学2021-2022学年高二下学期7月份月考化学试题
名校
解题方法
5 . X、Y、Z、W四种短周期主族元素,原子序数依次增大。X、Y与Z位于同一周期,且只有X、Y元素相邻,X基态原子核外有2个未成对电子,W原子在同周期中原子半径最大。下列说法不正确 的是
A.第一电离能: |
B.电负性: |
C.Z、W原子形成稀有气体电子构型的简单离子的半径: |
D.Y与Z形成的分子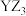 中每个原子均满足 中每个原子均满足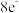 结构 结构 |
您最近半年使用:0次
2024-01-09更新
|
448次组卷
|
3卷引用:海南省农垦中学2023-2024学年高二上学期期中检测化学试题
解题方法
6 . 五种主族元素在周期表中的位置如图所示。L的单质在常温常压下呈液态,且保存时需要用水液封。下列推断正确的是
| X | Y | Z | T | |
| L |
| A.原子半径:X<Y<Z<T<L |
| B.气态氢化物的还原性:L>Z>T |
| C.X的电负性是五种元素中最小的 |
| D.Y和T组成的化合物是离子化合物 |
您最近半年使用:0次
7 . 第ⅣA族元素及其化合物在生产、生活中应用广泛。回答下列问题:
(1)基态锗原子的价层电子轨道表示式为______ ,第ⅣA族元素位于______ 区。
(2) 的电负性比
的电负性比 大,其主要原因是
大,其主要原因是_________________ 。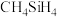 、
、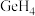 的稳定性依次减弱,其主要原因是
的稳定性依次减弱,其主要原因是______________________ 。
(3) 的VSEPR模型名称为
的VSEPR模型名称为________________________________ 。
(4)碳化硅( )熔点为2700°C,常作砂轮磨料,用于切割金属。由此推知,碳化硅晶体类型为
)熔点为2700°C,常作砂轮磨料,用于切割金属。由此推知,碳化硅晶体类型为______ 。
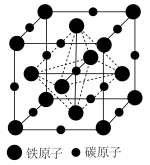
(5)铁和碳能形成如图所示的晶胞。它可以看成是铁晶胞中插入若干个碳原子,晶胞体积不变。铁碳晶体的化学式为______ ,铁晶体转化为铁碳晶体时晶体密度净增______ %(结果保留3位有效数字)。
(1)基态锗原子的价层电子轨道表示式为
(2)
 的电负性比
的电负性比 大,其主要原因是
大,其主要原因是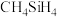 、
、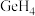 的稳定性依次减弱,其主要原因是
的稳定性依次减弱,其主要原因是(3)
 的VSEPR模型名称为
的VSEPR模型名称为(4)碳化硅(
 )熔点为2700°C,常作砂轮磨料,用于切割金属。由此推知,碳化硅晶体类型为
)熔点为2700°C,常作砂轮磨料,用于切割金属。由此推知,碳化硅晶体类型为(5)铁和碳能形成如图所示的晶胞。它可以看成是铁晶胞中插入若干个碳原子,晶胞体积不变。铁碳晶体的化学式为
您最近半年使用:0次
名校
解题方法
8 . 下列叙述中正确的个数有( )
①氧原子的电子排布图: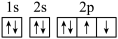 最外层违背了泡利原理
最外层违背了泡利原理
②处于最低能量状态原子叫基态原子,1s22s22px1→1s22s22py1过程中形成的是发射光谱
③所有元素中,氟的第一电离能最大
④具有相同核外电子排布的粒子,化学性质相同
⑤NCl3中N-Cl键的键长比CCl4中C-Cl键的键长短
⑥金属元素的电负性均小于1.8
⑦主族元素的电负性越大,其元素原子的第一电离能一定越大
⑧在任何情况下,都是σ键比π键强度大
①氧原子的电子排布图:
 最外层违背了泡利原理
最外层违背了泡利原理②处于最低能量状态原子叫基态原子,1s22s22px1→1s22s22py1过程中形成的是发射光谱
③所有元素中,氟的第一电离能最大
④具有相同核外电子排布的粒子,化学性质相同
⑤NCl3中N-Cl键的键长比CCl4中C-Cl键的键长短
⑥金属元素的电负性均小于1.8
⑦主族元素的电负性越大,其元素原子的第一电离能一定越大
⑧在任何情况下,都是σ键比π键强度大
| A.0个 | B.1个 | C.2个 | D.3个 |
您最近半年使用:0次
2019-11-27更新
|
1588次组卷
|
9卷引用:海南热带海洋学院附属中学2021-2022学年高二下学期第一次月考化学试题
海南热带海洋学院附属中学2021-2022学年高二下学期第一次月考化学试题安徽省毛坦厂中学2019-2020学年高二上学期期中考试化学试题(人教版2019)选择性必修2 阶段性综合评估测试卷(一)重庆市实验中学校2021-2022学年高二下学期第一次月考化学试题重庆市南华中学校2021-2022学年高二3月月考化学试题重庆实验外国语学校2021-2022学年高二下学期6月月考化学试题湖南省永州市祁阳县第四中学2022-2023学年高二下学期第一次段考化学试题黑龙江省齐齐哈尔市第八中学校2022-2023学年高二下学期期中考试化学试题陕西省西安市陕西师范大学附属中学渭北中学2022-2023学年高二下学期5月月考化学试题
2022·四川攀枝花·模拟预测
解题方法
9 . 材料是人类进步的基石,深入认识物质的结构有助于进一步开发新的材料。回答下列问题:
(1)按照杂化轨道理论,基态B原子的价电子先激发,再杂化成键形成BCl3。杂化前,处于激发态的B原子的价电子轨道表示式为_______ ( 选填标号)。
(2)已知:第四周期中3d轨道上没有未成对电子的过渡元素离子的水合离子为无色。下列离子形成的水合离子为无色的是_______。
(3)K3[Fe(CN)6]中所含元素电负性由大到小的顺序为_______ ,lmol K3[Fe(CN)6]含有_______ molσ键;Ti3+能形成化合物[TiCl(H2O)5]Cl2·H2O,该化合物中Ti3+的配位数为_______ 。
(4)Ni(CO)4常温下呈液态,其分子空间构型为正四面体。解释其易溶于CCl4、苯等有机溶剂的原因:_______ 。
(5)纯水电离产生H3O+、OH-,研究发现在某些水溶液中还存在 、
、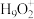 等微粒。
等微粒。
①H2O分子的键角小于H3O+离子的键角,原因是_______ 。
②画出 可能的一种结构式
可能的一种结构式_______ 。
(6)TiO2通过氮掺杂反应生成TiO2-xNy,表示如图。
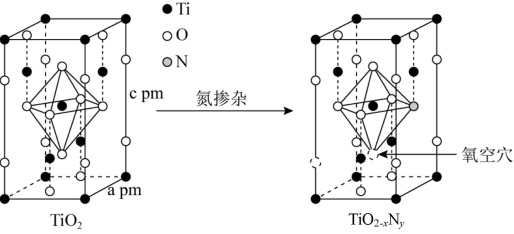
①立方晶系TiO2晶胞参数如图甲所示,若用NA表示阿伏加德罗常数,其晶体的密度为_______ g/cm3。
②图乙的结构可用化学式TiO2-xNy表示,其中x=_______ 。
(1)按照杂化轨道理论,基态B原子的价电子先激发,再杂化成键形成BCl3。杂化前,处于激发态的B原子的价电子轨道表示式为_______ ( 选填标号)。
A.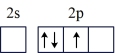 | B.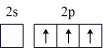 |
C.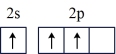 | D.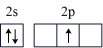 |
| A.Sc3+ | B.Cr3+ | C.Fe3+ | D.Zn2+ |
(4)Ni(CO)4常温下呈液态,其分子空间构型为正四面体。解释其易溶于CCl4、苯等有机溶剂的原因:
(5)纯水电离产生H3O+、OH-,研究发现在某些水溶液中还存在
 、
、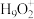 等微粒。
等微粒。①H2O分子的键角小于H3O+离子的键角,原因是
②画出
 可能的一种结构式
可能的一种结构式(6)TiO2通过氮掺杂反应生成TiO2-xNy,表示如图。

①立方晶系TiO2晶胞参数如图甲所示,若用NA表示阿伏加德罗常数,其晶体的密度为
②图乙的结构可用化学式TiO2-xNy表示,其中x=
您最近半年使用:0次
21-22高三下·广西河池·阶段练习
名校
解题方法
10 . 过氧乙酸又名过醋酸(C2H4O3),是重要化工原料。也是一种绿色生态杀菌剂,其制法为CH3COOH+H2O2=CH3COOOH+H2O。
(1)某同学写出了碳原子的4种不同状态的电子排布图____ 。
A.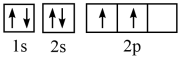 B.
B.
C.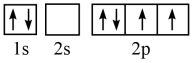 D.
D.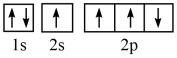
其中能量最低的是____ (填标号),电子由状态C到状态B所得到的光谱为____ 光谱(填“原子发射”或“原子吸收”)。
(2)过氧乙酸分子中C原子的杂化方式有____ 。
(3)乙酸比乙醇易电离出H+的原因____ 。
(4)乙酸和硝酸分子中所包含元素电负性由大到小的顺序是____ (用元素符号表示)。
(5)造纸中,用NaBH4与纸浆中的过氧乙酸以及过渡金属离子反应以提高漂白效率。硼氢化钠、硼氢化铝被认为是有机化学上的“万能还原剂”。
①两种硼氢化物的熔点如表所示:
解释表中两种物质熔点差异的原因____ 。
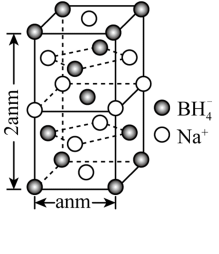
②硼氢化钠晶胞结构如图所示,该晶体中Na+的配位数为____ 。已知:硼氢化钠晶体的密度为ρg·cm-3,NA代表阿伏加德罗常数的值,则a=___ nm(用含ρ、NA的最简式子表示)
(1)某同学写出了碳原子的4种不同状态的电子排布图
A.
 B.
B.
C.
 D.
D.
其中能量最低的是
(2)过氧乙酸分子中C原子的杂化方式有
(3)乙酸比乙醇易电离出H+的原因
(4)乙酸和硝酸分子中所包含元素电负性由大到小的顺序是
(5)造纸中,用NaBH4与纸浆中的过氧乙酸以及过渡金属离子反应以提高漂白效率。硼氢化钠、硼氢化铝被认为是有机化学上的“万能还原剂”。
①两种硼氢化物的熔点如表所示:
| 硼氢化物 | NaBH4 | Al(BH4)3 |
| 熔点/℃ | 400 | -64.5 |
②硼氢化钠晶胞结构如图所示,该晶体中Na+的配位数为

您最近半年使用:0次
2022-06-29更新
|
606次组卷
|
4卷引用:2022年海南省高考真题变式题15-19
(已下线)2022年海南省高考真题变式题15-19广西河池高级中学2022届高三下学期4月考试理科综合化学试题宁夏六盘山高级中学2023-2024学年高三一模考试化学试题天津市第四十五中学2023-2024学年高三12月月考化学试题



