| A.电负性:X>Y>Z>W |
| B.原子半径:X<Y<Z<W |
| C.Y和W的单质都能与水反应生成气体 |
| D.Z元素最高价氧化物对应的水化物具有强氧化性 |
| A.X能与多种元素形成共价键 | B.简单氢化物沸点: |
C.第一电离能: | D.电负性: |
| A.元素Z在周期表中位于第3周期VA族 |
| B.原子半径:r(X)<r(Y) |
| C.Z的第一电离能比W的小. |
| D.X的简单气态氢化物的热稳定性比Z的弱 |
4 . 根据信息回答下列问题:
(1)如图是部分元素原子的第一电离能I1随原子序数变化的曲线图(其中12号至17号元素的有关数据缺失)。
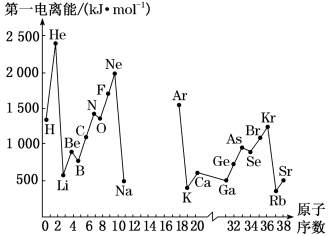
①认真分析图中同周期元素第一电离能的变化规律,推断Na~Ar元素中,Al的第一电离能的大小范围为
②图中Ge元素中未成对电子有
(2)已知元素的电负性和元素的化合价一样,也是元素的一种基本性质。下面给出部分元素的电负性:
元素 | Al | B | Be | C | Cl | F | Li |
电负性 | 2.0 | 1.5 | 2.5 | 3.0 | 4.0 | 1.0 | |
元素 | Mg | N | Na | O | P | S | Si |
电负性 | 1.2 | 3.0 | 0.9 | 3.5 | 2.1 | 2.5 | 1.8 |
已知:两成键元素间电负性差值大于1.7时,形成离子键,两成键元素间电负性差值小于1.7时,形成共价键。
①根据表中给出的数据,可推知元素的电负性具有的变化规律
②通过分析电负性值变化规律,确定Al元素电负性值的最小范围
③判断下列物质是离子化合物还是共价化合物:
A Li3N B PCl3 C MgCl2 D SiC
Ⅰ.属于离子化合物的是
Ⅱ.属于共价化合物的是
请设计一个实验方案证明上述所得到的结论
①1s22s22p63s23p4;②1s22s22p63s23p3;③1s22s22p5。
则下列有关比较中正确的是
| A.第一电离能:③>②>① |
| B.原子半径:③>②>① |
| C.电负性:③>②>① |
| D.最高正化合价:③>②>① |
| 元素 | 相关信息 |
| A | 元素的原子核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B | 元素原子的核外p电子数比s电子数少1 |
| C | 元素的第一至第四电离能分别是I1=738 kJ/mol、I2=1451 kJ/mol、I3= 7733 kJ/mol、I4= 10540 kJ/mol |
| D | 原子核外填充电子的所有p轨道全满或半满 |
| E | 元素的主族序数与周期序数的差为3 |
| F | 在元素周期表的第6列 |
(2)根据上述信息,画出C元素基态原子的轨道表示式
(3)F在元素周期表中属于
(4)D、E两元素的第一电离能大小关系是
(5)写出DA3的电子式:

| A.四种元素中X的电负性最小 |
| B.最简单气态氢化物的稳定性:Z<Y |
| C.W位于周期表的第二周期VIA族 |
| D.四种元素可组成既含离子键又含共价键的化合物 |
 到淀粉的全合成。其合成路线如下:
到淀粉的全合成。其合成路线如下: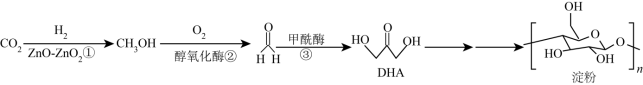
下列说法错误的是
| A.电负性:O>C>H>Zn |
| B.甲醇分子中H-C-O键角小于甲醛分子中H-C-O键角 |
| C.DHA分子间存在氢键 |
D.Zn2+溶于氨水形成配合物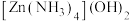 , , 的配位数为6 的配位数为6 |
| 选项 | 实例 | 解释 |
| A |  比 比 酸性强 酸性强 |  的电负性比 的电负性比 的电负性强,吸电子能力强,使羟基的极性增强,更容易电离 的电负性强,吸电子能力强,使羟基的极性增强,更容易电离 |
| B |  的沸点高于 的沸点高于 |  的非金属性强于 的非金属性强于 |
| C |  比 比 的稳定性高 的稳定性高 |  键的键能比 键的键能比 键的键能大 键的键能大 |
| D |  在 在 中的溶解度大于在 中的溶解度大于在 中的溶解度 中的溶解度 | 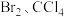 为非极性分子, 为非极性分子, 为极性分子 为极性分子 |
| A.A | B.B | C.C | D.D |
 ;基态Z原子核外电子有三个能级,p电子总数与s电子总数相等;W是第三周期电负性最大的元素。
;基态Z原子核外电子有三个能级,p电子总数与s电子总数相等;W是第三周期电负性最大的元素。(1)
 分子的空间构型为
分子的空间构型为(2)阴离子
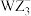 中W原子的杂化类型为
中W原子的杂化类型为(3)
 的沸点比Z同主族其他元素氢化物高,原因是
的沸点比Z同主族其他元素氢化物高,原因是(4)
 分子中各原子都满足最外层8电子结构,分子中π键与σ键数目之比为
分子中各原子都满足最外层8电子结构,分子中π键与σ键数目之比为


