1 . 化合物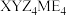 可作肥料,所含的5种元素位于主族,在每个短周期均有分布,仅有Y和M同族。Y的基态原子价层p轨道半充满,X的基态原子价层电子排布式为
可作肥料,所含的5种元素位于主族,在每个短周期均有分布,仅有Y和M同族。Y的基态原子价层p轨道半充满,X的基态原子价层电子排布式为 ,X与M同周期,E在地壳中含量最多。下列说法正确的是
,X与M同周期,E在地壳中含量最多。下列说法正确的是
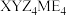 可作肥料,所含的5种元素位于主族,在每个短周期均有分布,仅有Y和M同族。Y的基态原子价层p轨道半充满,X的基态原子价层电子排布式为
可作肥料,所含的5种元素位于主族,在每个短周期均有分布,仅有Y和M同族。Y的基态原子价层p轨道半充满,X的基态原子价层电子排布式为 ,X与M同周期,E在地壳中含量最多。下列说法正确的是
,X与M同周期,E在地壳中含量最多。下列说法正确的是A.元素电负性: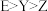 | B.氢化物沸点: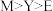 |
C.第一电离能: | D.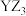 和 和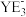 的空间结构均为三角锥形 的空间结构均为三角锥形 |
您最近一年使用:0次
2023-07-04更新
|
8028次组卷
|
15卷引用:河北省石家庄二中教育集团2023-2024学年高二年级上学期期末考试化学试题
河北省石家庄二中教育集团2023-2024学年高二年级上学期期末考试化学试题2023年高考广东卷化学真题(已下线)2023年广东卷高考真题变式题(选择题11-16)(已下线)第19讲元素周期律与元素周期表江西省宜春市宜丰中学2023-2024学年高三上学期开学考试化学试题(已下线)考点18 元素周期律与元素周期表(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)广东省江门市第一中学2023-2024学年高二上学期第一次段考化学试题(已下线)选择题1-5陕西师范大学附属中学2023-2024学年高二上学期期中考试化学试题(已下线)题型20 物质结构与性质基础-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)重庆市第七中学校2023-2024学年高三上学期月考(12月)化学试题安徽省合肥市第七中学2023-2024学年高二下学期第一次段考化学试卷 四川省南充市阆中中学校2023-2024学年高二下学期3月月考化学试卷福建省南安市侨光中学2023-2024学年高二下学期4月月考化学试题甘肃省白银市靖远县第四中学2023-2024学年高二下学期4月月考化学试题
名校
解题方法
2 . 下列说法正确的是
| A.第一电离能和电负性的大小可分别作为判断元素金属性和非金属性强弱的依据 |
| B.基态O原子核外电子的运动状态有8种 |
C.氢键 中的三原子均在一条直线上 中的三原子均在一条直线上 |
D. 的空间结构与其 的空间结构与其 模型相同 模型相同 |
您最近一年使用:0次
2024-03-08更新
|
574次组卷
|
3卷引用:河北省石家庄二中实验学校2023-2024学年高二下学期第一次月考化学试题
3 . 石墨烯、高温氯化钠、砷化镉等超导材料应用广泛。回答下列问题:
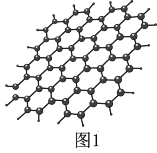
(1)石墨烯结构如图1所示,则碳原子的杂化方式为_______ ,12 g石墨烯中含有六元环个数与σ键个数之比为_______ 。
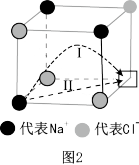
(2)温度升高时,NaCl晶体出现缺陷,如图2方格处填入Na+时,恰好构成氯化钠晶胞的 ,此时晶体的导电性大大增强。已知氯化钠晶体中两个相邻Cl-之间的间隙小于Na+直径,则Na+最可能通过途径
,此时晶体的导电性大大增强。已知氯化钠晶体中两个相邻Cl-之间的间隙小于Na+直径,则Na+最可能通过途径_______ (填图中序号)迁移到空位处。
(3)石墨烯限域单原子铁催化剂使CH4在室温条件下被H2O2直接氧化为HCHO、HCOOH,比较HCHO、HCOOH的沸点高低并说明理由_______ 。
(4)镉(Cd)与Zn同族且相邻,则基态Cd原子的价电子排布式为_______ ;与砷(As)同主族的N、P两种元素的氢化物水溶液的碱性:NH3强于PH3,原因是_______ 。
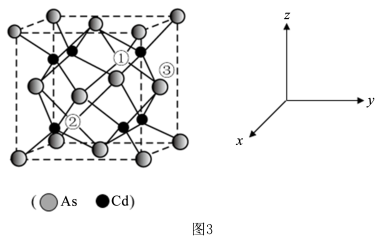
(5)砷化镉可以看作是石墨烯的3D版,其晶胞结构为正方体如图3, 占据顶点和面心,Cd占据As围成的四面体空隙,空隙占有率75%,故Cd为“具有两个真空的立方晶格”,其中“①”和“②”位是“真空”。建立如图的原子坐标系,①号位的坐标为(
占据顶点和面心,Cd占据As围成的四面体空隙,空隙占有率75%,故Cd为“具有两个真空的立方晶格”,其中“①”和“②”位是“真空”。建立如图的原子坐标系,①号位的坐标为( ,
, ,
, ),则③号位原子坐标参数为
),则③号位原子坐标参数为_______ 。晶胞的密度为 ,阿伏加德罗常数的值为NA,则该晶胞中距离最远的两个Cd原子之间的距离为
,阿伏加德罗常数的值为NA,则该晶胞中距离最远的两个Cd原子之间的距离为_______ pm(列计算式即可)。
(1)石墨烯结构如图1所示,则碳原子的杂化方式为

(2)温度升高时,NaCl晶体出现缺陷,如图2方格处填入Na+时,恰好构成氯化钠晶胞的
 ,此时晶体的导电性大大增强。已知氯化钠晶体中两个相邻Cl-之间的间隙小于Na+直径,则Na+最可能通过途径
,此时晶体的导电性大大增强。已知氯化钠晶体中两个相邻Cl-之间的间隙小于Na+直径,则Na+最可能通过途径
(3)石墨烯限域单原子铁催化剂使CH4在室温条件下被H2O2直接氧化为HCHO、HCOOH,比较HCHO、HCOOH的沸点高低并说明理由
(4)镉(Cd)与Zn同族且相邻,则基态Cd原子的价电子排布式为
(5)砷化镉可以看作是石墨烯的3D版,其晶胞结构为正方体如图3,
 占据顶点和面心,Cd占据As围成的四面体空隙,空隙占有率75%,故Cd为“具有两个真空的立方晶格”,其中“①”和“②”位是“真空”。建立如图的原子坐标系,①号位的坐标为(
占据顶点和面心,Cd占据As围成的四面体空隙,空隙占有率75%,故Cd为“具有两个真空的立方晶格”,其中“①”和“②”位是“真空”。建立如图的原子坐标系,①号位的坐标为( ,
, ,
, ),则③号位原子坐标参数为
),则③号位原子坐标参数为 ,阿伏加德罗常数的值为NA,则该晶胞中距离最远的两个Cd原子之间的距离为
,阿伏加德罗常数的值为NA,则该晶胞中距离最远的两个Cd原子之间的距离为
您最近一年使用:0次
2022-03-29更新
|
699次组卷
|
4卷引用:河北省石家庄市第二中学2022届高三2.5模化学试题
河北省石家庄市第二中学2022届高三2.5模化学试题山东省聊城市2021-2022学年下学期高三一模化学试题(已下线)必刷卷02-2022年高考化学考前信息必刷卷(山东专用)(已下线)必刷卷05-2022年高考化学考前信息必刷卷(河北专用)
名校
解题方法
4 . 由徐光宪院士发起院士学子同创的《分子共和国》科普读物生动形象地戏说了BF3、NH3、H2S、O3、CH3COOH、SOCl2等众多“分子共和国”中的明星。下列说法正确的是
| A.键角:NH3<BF3 |
| B.酸性:CH3COOH>CF3COOH |
| C.SOCl2分子中只存在σ键,不存在π键 |
| D.H2S、O3分子的空间结构均为直线形,且均为非极性分子 |
您最近一年使用:0次
2022-10-27更新
|
1202次组卷
|
14卷引用:河北省石家庄市第九中学2022-2023高三上学期10月月考化学试题
河北省石家庄市第九中学2022-2023高三上学期10月月考化学试题广东省云浮市2021-2022学年高二下学期期末教学质量检测化学试题湖北省恩施州高中教育联盟2021-2022学年高二下学期期末考试化学试题广东省梅州市梅江区梅州中学2022-2023学年高三上学期8月阶段性考试化学试题宁夏石嘴山市平罗中学2022-2023学年高二上学期期中考试(重点班)化学试题广东省深圳市福田区福田中学2022-2023学年高三上学期第二次月考化学试题(已下线)第37讲 分子结构与性质(练)-2023年高考化学一轮复习讲练测(全国通用)(已下线)专题七 非金属元素及其化合物-实战高考·二轮复习核心突破广东省广州市第二中学2022-2023学年高三 上学期(11月25日)周测化学试题 广东省广州市第六中学2022-2023学年高二下学期期末考试化学试题(已下线)第05讲 分子结构与物质的性质-【寒假自学课】2024年高二化学寒假提升学与练(人教版2019)(已下线)热点05 分子结构与物质的性质四川省达州市万源中学2023-2024学年高二下学期4月月考化学试题广东省广州市第六中学2023-2024学年高二下学期期中考试化学试题
名校
解题方法
5 . X、Y、Z、M是电负性逐渐减小的短周期非金属元素。X、Z、M位于三个不同周期,Y与Z的价电子数目之和为M价电子数的两倍;化合物 的电子总数为18个。下列说法错误的是
的电子总数为18个。下列说法错误的是
 的电子总数为18个。下列说法错误的是
的电子总数为18个。下列说法错误的是| A.原子半径:Z<X<Y<M | B.简单氢化物的稳定性:X>Y>M |
| C.Z与M形成的化合物具有较强的还原性 | D.Y的含氧酸为弱酸 |
您最近一年使用:0次
2023-04-10更新
|
741次组卷
|
5卷引用:河北省石家庄市部分学校2023届高中毕业年级教学质量检测(二)(一模)化学试题
河北省石家庄市部分学校2023届高中毕业年级教学质量检测(二)(一模)化学试题(已下线)专题06 物质结构与性质江西省吉安市吉州区部分学校联考2022-2023学年高二下学期期末考试化学试题(已下线)2019年高考江苏卷化学试题变式题(单选题6-10)江苏省江阴市华士高级中学2023-2024学年高二上学期10月学情调研化学(选修)试题
名校
解题方法
6 . 已知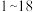 号元素的离子
号元素的离子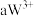 、
、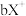 、
、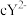 、
、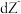 都具有相同电子层结构,下列关系正确的是
都具有相同电子层结构,下列关系正确的是
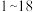 号元素的离子
号元素的离子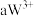 、
、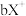 、
、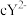 、
、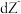 都具有相同电子层结构,下列关系正确的是
都具有相同电子层结构,下列关系正确的是A.质子数: ,离子的还原性: ,离子的还原性: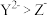 |
B.电负性: |
C.氢化物的稳定性: |
D.原子半径: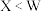 ,第一电离能: ,第一电离能: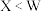 |
您最近一年使用:0次
2022-12-02更新
|
1063次组卷
|
33卷引用:河北省石家庄市启明中学2019-2020学年高二四月月考化学试题
河北省石家庄市启明中学2019-2020学年高二四月月考化学试题2015-2016学年贵州省思南中学高二下第一次月考化学试卷2015-2016学年山西大学附属中学高二下3月月考化学试卷2015-2016学年吉林省汪清六中高二3月月考化学试卷2015-2016学年山西大学附中高二下3月月考化学试卷2016-2017学年河北省衡水中学高二上学期五调考试化学试卷2016-2017学年河南省洛阳市第一高级中学高二(平行班)3月月考化学试卷2016-2017学年山西省大同市第一中学高二3月月考化学试卷福建省三明市第一中学2016-2017学年高二下学期半期考试化学试题贵州省思南中学2016-2017学年高二下学期期中考试化学试题人教版2017-2018学年高二化学选修三同步训练:第一章 原子结构与性质1河北省邢台市第二中学2017-2018学年高二化学选修三课时训练:第一章 综合检测1吉林省辽源五中2017-2018学年高二下学期第一次月考化学试题【全国百强校】甘肃省嘉峪关市酒钢三中2017-2018学年高二下学期期中考试化学试题【全国百强校】宁夏吴忠中学2017-2018学年高二6月月考化学试题2020届高三化学二轮物质结构题型专攻——元素性质的递变规律【选择提升专练】福建省厦门市思明区厦门外国语学校2019-2020学年高二上学期周末练习10——化学试题河南省林州市林虑中学2019-2020学年高二3月线上考试化学试题吉林省白山市第七中学2019-2020学年高二下学期3月份月考化学试题鲁科版(新)必修第二册第一章检测题辽宁省六校协作体2019-2020学年高二下学期期中考试化学试卷(鲁科版2019)选择性必修2 第1章 原子结构与元素性质 第3节 元素性质及其变化规律(人教版2019)选择性必修2 第一章 原子结构与性质 第二节 原子结构与元素的性质(人教版2019)选择性必修2第一章 原子结构与性质 第二节 原子结构与元素的性质 第3课时 元素的电负性及其变化规律鲁科版2019选择性必修2第1章 原子结构与元素性质 第3节 元素性质及其变化规律 第2课时 元素的电负性及其变化规律(已下线)模块同步卷03 第一章综合检测-《灯塔金卷系列》2020-2021学年高二化学模块同步卷(人教版选修3)专题强化练2 电离能和电负性的应用吉林省辉南县第六中学2022-2023学年高二上学期期中考试化学试题湖南省长沙市周南中学2022-2023学年高二上学期期末考试化学试题安徽省池州市第一中学2022-2023学年高二下学期第一次月考化学试题北京市第三十五中学2021-2022学年高三上学期期中考试化学试题四川省内江市资中县第二中学2023-2024学年高二下学期3月月考化学试题黑龙江省黑河市第一中学2023-2024学年高二下学期4月月考化学试题
解题方法
7 . 物质的结构决定其性质。下列实例与解释不相符的是
| 选项 | 事实 | 解释 |
| A | 金属是电的良导体 | 金属晶体中的自由电子在外电场作用下发生定向移动 |
| B | NF3不易与Cu2+形成配位键 | F的电负性大,导致N原子核对其孤电子对的吸引力大 |
| C | CO的沸点高于N2 | CO的极性大于N2 |
| D |  中的键角小于 中的键角小于 | S的原子半径较大,其价层σ键电子对之间的斥力较小 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-04-13更新
|
495次组卷
|
4卷引用:河北省石家庄市2024届高三下学期4月第二次质检化学试题
河北省石家庄市2024届高三下学期4月第二次质检化学试题河北省石家庄二中实验学校2023-2024学年高二下学期第一次月考化学试题(已下线)化学(天津卷01)-2024年高考押题预测卷河北省重点高中2023-2024学年高三下学期5月高考模拟化学试题(二)
解题方法
8 . 中国第一辆火星车“祝融号”成功登陆火星,探测发现火星上存在大量橄榄石矿物( ),已知晶体硅的晶胞如图,下列说法错误的是
),已知晶体硅的晶胞如图,下列说法错误的是
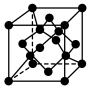
 ),已知晶体硅的晶胞如图,下列说法错误的是
),已知晶体硅的晶胞如图,下列说法错误的是
| A.Fe2+价电子排布式为3d6,未成对电子数是4 |
| B.橄榄石中各元素第一电离能和电负性大小顺序均为O>Si>Fe>Mg |
| C.硅的氯化物SiCl4分子是非极性分子,Si的杂化方式是sp3 |
D.若单晶硅晶胞参数是anm,则Si原子的原子半径为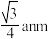 |
您最近一年使用:0次
2023-12-31更新
|
485次组卷
|
2卷引用:河北省石家庄市部分重点高中2023-2024学年高三上学期12月期末化学试题
名校
9 . 现有四种元素基态原子的电子排布式如下:① ②
② ③
③ ④
④ 。则下列有关比较中正确的是
。则下列有关比较中正确的是
 ②
② ③
③ ④
④ 。则下列有关比较中正确的是
。则下列有关比较中正确的是| A.第一电离能:④>③>①>② | B.原子半径:④>③>②>① |
| C.电负性:④>③>①>② | D.最高正化合价:④>③=②>① |
您最近一年使用:0次
2021-02-01更新
|
1513次组卷
|
13卷引用:河北省石家庄市第二中学2022年高二寒假考试化学试题
河北省石家庄市第二中学2022年高二寒假考试化学试题(人教版2019)选择性必修2 阶段性综合评估测试卷(二)鲁科版2019选择性必修2阶段性综合评估测试卷(二)陕西省宝鸡市长岭中学2021-2022学年高二下学期期中考试化学试题重庆市朝阳中学2021-2022学年高二下学期期中考试化学试题湖北省武汉市钢城第四中学2021-2022学年高二下学期期中考试化学试题吉林省洮南市第一中学2022-2023学年高二下学期学习质量检测化学试卷新疆维吾尔自治区塔城地区2022-2023学年高二下学期5月期中化学试题广东省揭阳市三所中学联考2022-2023学年高二下学期4月期中考试化学试题陕西省西安市陕西师范大学附属中学渭北中学2022-2023学年高二下学期5月月考化学试题江西省丰城拖船中学2022-2023学年高二下学期6月期末考试化学试题吉林省长春市新解放学校2022-2023学年高二下学期7月期末考试化学试题安徽省安庆市怀宁县高河中学2023-2024学年高二下学期第一次月考化学试题
名校
10 . 回答下列问题:
(1)Pt的电子排布式为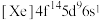 ,则Pt在元素周期表中的位置是
,则Pt在元素周期表中的位置是_______ ,处于_______ 区。
(2) 中阴离子的立体构型名称是
中阴离子的立体构型名称是_______ ,B、N、H的电负性由大到小的顺序为_______ 。
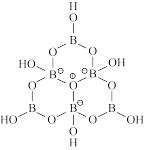
(3)科学家合成了一种含硼阴离子[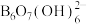 ],其结构如下图所示。其中硼原子的杂化方式为
],其结构如下图所示。其中硼原子的杂化方式为_______ ,该结构中共有_______ 种不同化学环境的氧原子。
(4)金属硼氢化物可用作储氢材料。如图是一种金属硼氢化物氨合物的晶体结构示意图。图中八面体的中心代表金属M原子,顶点代表氨分子;四面体的中心代表硼原子,顶点代表氢原子。该晶体属立方晶系,晶胞棱边夹角均为90,棱长为apm,密度为3 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 。
。

①该晶体的化学式为_______ 。
②金属M原子与硼原子间最短距离为_______ pm。
③金属M的相对原子质量为_______ (列出表达式)。
(1)Pt的电子排布式为
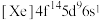 ,则Pt在元素周期表中的位置是
,则Pt在元素周期表中的位置是(2)
 中阴离子的立体构型名称是
中阴离子的立体构型名称是(3)科学家合成了一种含硼阴离子[
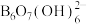 ],其结构如下图所示。其中硼原子的杂化方式为
],其结构如下图所示。其中硼原子的杂化方式为
(4)金属硼氢化物可用作储氢材料。如图是一种金属硼氢化物氨合物的晶体结构示意图。图中八面体的中心代表金属M原子,顶点代表氨分子;四面体的中心代表硼原子,顶点代表氢原子。该晶体属立方晶系,晶胞棱边夹角均为90,棱长为apm,密度为3
 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 。
。
①该晶体的化学式为
②金属M原子与硼原子间最短距离为
③金属M的相对原子质量为
您最近一年使用:0次
2022-04-01更新
|
492次组卷
|
5卷引用:河北省石家庄市第二中学2022届高三下学期5月模拟考试化学试题



