1 . 物质的结构决定其性质.下列事实与解释不相符的是
选项 | 事实 | 解释 |
A | 基态Cu原子价层电子排布式为3d104s1 | 3d能级电子为全充满状态,原子能量更低 |
B | 水的热稳定性强于氨 | 水分子间形成的氢键数目与强度均大于氨 |
C | 三氟乙酸的酸性强于乙酸 | 氟为吸电子基,导致羟基中O-H键极性变大 |
D | Na2O、MgO、Al2O3离子键成分的百分数依次减小 | Na、Mg、Al的电负性依次增大 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-06-01更新
|
202次组卷
|
2卷引用:河北省石家庄市2024届普通高中学校高三毕业年级教学质量检测(三)化学试卷
解题方法
2 . 已知X、Y、Z、W、Q、R六种元素中,原子序数依次增大,其结构或性质信息如表。
请根据信息回答有关问题:
(1)元素X原子核外共有___________ 种不同运动状态的电子。
(2)元素X、Y的第一电离能较大的是___________ (填元素符号)。
(3)元素X、Y、Z的电负性最小的是___________ (填元素符号)。
(4)元素W的基态原子核外电子排布式为___________ 。
(5)元素Q在周期表中位置为___________ ,元素R基态原子的价电子排布式为___________ 。
| 元素 | 结构或性质信息 |
| X | 基态原子的最外层电子排布式为 |
| Y | 基态原子的L层上有2个未成对的p电子 |
| Z | 基态原子的M层上s、p电子个数相等 |
| W | 位于第4周期VIB族 |
| Q | 元素的正三价离子的 能级半充满 能级半充满 |
| R | 元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子 |
(1)元素X原子核外共有
(2)元素X、Y的第一电离能较大的是
(3)元素X、Y、Z的电负性最小的是
(4)元素W的基态原子核外电子排布式为
(5)元素Q在周期表中位置为
您最近一年使用:0次
名校
3 . W、X、Z、Q、Y为原子序数依次增大的短周期主族元素,期内层电子数之和为18,最外层电子数之和为28,它们所形成的阴离子具有很高的亲水性,可以作为能源材料中的电解质,该离子结构如图所示。下列说法正确的是

| A.Y离子的VSEPR模型为四面体 | B.原子半径:Y>Z>W |
| C.电负性:X<Y<Q | D.阴离子中∠Y-X-Y为180° |
您最近一年使用:0次
2024-02-27更新
|
162次组卷
|
2卷引用:河北省石家庄二中教育集团2023-2024学年高二年级上学期期末考试化学试题
名校
4 . X、Y、Z、W、R为五种短周期元素,其原子半径和最外层电子数之间的关系如图所示。下列说法错误的是
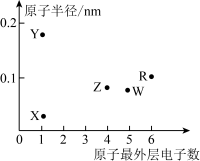

| A.X、Y、R三种元素可以形成离子化合物 |
| B.元素的电负性:Z>W |
| C.W2X4可以与H+形成配位键 |
| D.X与Z可以形成正四面体结构的分子 |
您最近一年使用:0次
2023-03-26更新
|
155次组卷
|
2卷引用:河北省石家庄市第十七中学2022-2023高二下学期第一次月考化学试题
5 . 工业上电解熔融Al2O3和冰晶石(Na3AlF6)的混合物可制得铝,下列说法正确的是
| A.半径大小:r(Al3+)<r(Na+) | B.电负性大小:F<O |
| C.电离能大小:I1(O)<I1(Na) | D.还原性:F->O2- |
您最近一年使用:0次
名校
解题方法
6 . 前20号不同主族元素 的原子序数依次增大,它们的原子序数之和等于35,分析试剂
的原子序数依次增大,它们的原子序数之和等于35,分析试剂 常用于稀土金属分离的载体、陶瓷上釉等。加热
常用于稀土金属分离的载体、陶瓷上釉等。加热 固体
固体 ,剩余固体质量(m)与温度(T)的关系如图所示。下列叙述正确的是
,剩余固体质量(m)与温度(T)的关系如图所示。下列叙述正确的是

 的原子序数依次增大,它们的原子序数之和等于35,分析试剂
的原子序数依次增大,它们的原子序数之和等于35,分析试剂 常用于稀土金属分离的载体、陶瓷上釉等。加热
常用于稀土金属分离的载体、陶瓷上釉等。加热 固体
固体 ,剩余固体质量(m)与温度(T)的关系如图所示。下列叙述正确的是
,剩余固体质量(m)与温度(T)的关系如图所示。下列叙述正确的是
A.电负性: | B.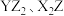 都是直线形分子 都是直线形分子 |
C. 段失去 段失去 分子 分子 | D. 生成的固体化合物为 生成的固体化合物为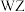 |
您最近一年使用:0次
2024-02-13更新
|
120次组卷
|
3卷引用:河北省石家庄市新乐市第一中学等校2023-2024学年高三上学期省级联测考试化学试卷
名校
解题方法
7 . 由于铁氮化合物具有非常优异的磁性能、机械性能和耐腐蚀性,受到研究人员的广泛关注。γˊ−Fe4N是一种性能优异的铁氮化合物,其可由氨气与羰基铁粉[Fe(CO)5]反应得到。
(1)Fe变为Fe2+时是失去___________ 轨道电子,Fe3+价层电子排布图为___________ 。
(2)氨气中N的杂化类型是___________ ,NH3中H−N−H的键角比NH4+中H−N−H的键角___________ (填“大”或“小”),理由是___________ 。
(3) 与CO中均存在化学键的类型有
与CO中均存在化学键的类型有___________ (填标号)。
A.离子键 B.氢键 C.配位键 D.共价键 E.金属键
(4)羰基铁粉[Fe(CO)5]中铁元素的配位数是___________ ,配位原子为___________ 。
(5)氨气与羰基铁粉的反应中涉及元素电负性由大到小的顺序为___________ 。
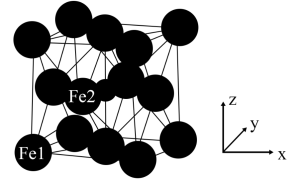
(6)γ−Fe4N的晶胞如图所示,设晶胞中Fe1点的原子坐标为(0,0,0),N点的原子坐标为( ,
, ,
, ),则Fe2点的原子坐标为
),则Fe2点的原子坐标为___________ 。已知该晶体的密度为dg/cm3,阿伏加德罗常数的值为NA,则晶胞参数a为___________ nm(用含d和NA的代数式表示)。
(1)Fe变为Fe2+时是失去
(2)氨气中N的杂化类型是
(3)
 与CO中均存在化学键的类型有
与CO中均存在化学键的类型有A.离子键 B.氢键 C.配位键 D.共价键 E.金属键
(4)羰基铁粉[Fe(CO)5]中铁元素的配位数是
(5)氨气与羰基铁粉的反应中涉及元素电负性由大到小的顺序为
(6)γ−Fe4N的晶胞如图所示,设晶胞中Fe1点的原子坐标为(0,0,0),N点的原子坐标为(
 ,
, ,
, ),则Fe2点的原子坐标为
),则Fe2点的原子坐标为
您最近一年使用:0次
2021-12-31更新
|
289次组卷
|
5卷引用:石家庄示范性高中2022届高三上学期调研考试化学试题
名校
8 . 由于钒的化合物颜色鲜艳而多彩,因此以神话中斯堪的纳维亚女神“Vanadis"的名字命名。钒有多种化合价,如:+2、+3、+4、+5等,其化合物具有广泛的用途。请回答下列问题:
(1)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用+ ,表示,与之相反的用 -
,表示,与之相反的用 - 表示,称为电子的自旋磁量子数,则基态V3+核外电子的自旋磁量子数之和为
表示,称为电子的自旋磁量子数,则基态V3+核外电子的自旋磁量子数之和为___________ 。
(2)钒的一种配合物的结构简式为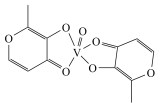 ,该配合物的组成元素的电负性由大到小的顺序是
,该配合物的组成元素的电负性由大到小的顺序是_______ (用元素符号表示),氧原子的杂化轨道类型为__________ ,该配合物分子中含有的化学键类型有________ (填标号)。
A.离子键 B.极性键 C.非极性键 D.配位键
(3)钒的含氧酸有正钒酸(H3VO4)、偏钒酸(HVO3)等,正钒酸、偏钒酸的酸性由强到弱的顺序是_____________ (用分子式表示),原因为________ 。
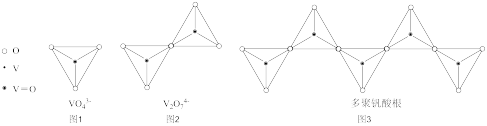
(4)钒的多种含氧酸根离子的结构如图所示,图3为一种无限长单链结构的多聚钒酸根,其化学式为__ 。
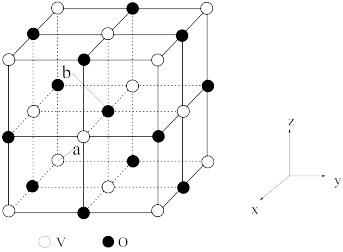
(5)钒的某种氧化物的立方晶胞如图所示,该氧化物的化学式为________________________ ;以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分数坐标,若a点原子的分数坐标为(0,0,0),则b点原子的分数坐标为____________________ ;钒原子构成的八面体空隙与氧原子构成的八 面体空隙的数量比为_________________________ ;已知该氧化物晶体的密度为ρg·cm-3。则晶胞中距离最近的两个氧原子的核间距为_________________ pm(用NA表示阿伏加德罗常数的值,列出计算式即可)。
(1)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用+
 ,表示,与之相反的用 -
,表示,与之相反的用 - 表示,称为电子的自旋磁量子数,则基态V3+核外电子的自旋磁量子数之和为
表示,称为电子的自旋磁量子数,则基态V3+核外电子的自旋磁量子数之和为(2)钒的一种配合物的结构简式为
 ,该配合物的组成元素的电负性由大到小的顺序是
,该配合物的组成元素的电负性由大到小的顺序是A.离子键 B.极性键 C.非极性键 D.配位键
(3)钒的含氧酸有正钒酸(H3VO4)、偏钒酸(HVO3)等,正钒酸、偏钒酸的酸性由强到弱的顺序是
(4)钒的多种含氧酸根离子的结构如图所示,图3为一种无限长单链结构的多聚钒酸根,其化学式为

(5)钒的某种氧化物的立方晶胞如图所示,该氧化物的化学式为

您最近一年使用:0次
名校
9 . 光学性能优良的高分子材料聚础酸异山梨醇酯可由如下反应制备。
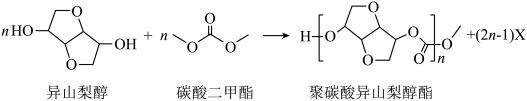
下列说法错误的是
| A.涉及元素的电负性:H<C<O | B.异山梨醇分子中有4个手性碳 |
| C.反应式中化合物X为甲醇 | D.异山梨醇中所有碳原子共平面 |
您最近一年使用:0次
名校
解题方法
10 . M、R、X、Y为原子序数依次增大的短周期主族元素,Z是一种过渡元素。M的基态原子L层p轨道电子数是s轨道电子数的2倍,R是同周期元素中最活泼的金属元素,X和M形成的一种化合物是引起酸雨的主要大气污染物,Y是一种重要的成盐元素,Z的基态原子4s和3d轨道均为半充满状态。回答下列问题:
(1)R的基态原子核外电子占据的最高能层符号为___________ ,占据最高能级的电子云轮廓图为___________ 形,核外电子运动状态共有___________ 种。
(2)X和Y相比较,电负性较大的是___________ (填元素符号),简单氢化物稳定性较强的是___________ (填化学式)。
(3)M、R形成的既含离子键又含非极性键的化合物的电子式为___________ 。
(4)Z的基态原子价层电子排布式为___________ ,与Z同周期且最外层电子数相同的元素有___________ 种。
(5)与X同周期且主族序数小1的元素的第一电离能___________ (填“>”或“<”)X元素的第一电离能,原因为___________ 。
(1)R的基态原子核外电子占据的最高能层符号为
(2)X和Y相比较,电负性较大的是
(3)M、R形成的既含离子键又含非极性键的化合物的电子式为
(4)Z的基态原子价层电子排布式为
(5)与X同周期且主族序数小1的元素的第一电离能
您最近一年使用:0次



