名校
1 . 回答下列问题:
(1)Pt的电子排布式为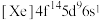 ,则Pt在元素周期表中的位置是
,则Pt在元素周期表中的位置是_______ ,处于_______ 区。
(2) 中阴离子的立体构型名称是
中阴离子的立体构型名称是_______ ,B、N、H的电负性由大到小的顺序为_______ 。
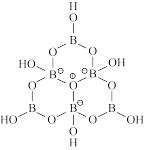
(3)科学家合成了一种含硼阴离子[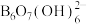 ],其结构如下图所示。其中硼原子的杂化方式为
],其结构如下图所示。其中硼原子的杂化方式为_______ ,该结构中共有_______ 种不同化学环境的氧原子。
(4)金属硼氢化物可用作储氢材料。如图是一种金属硼氢化物氨合物的晶体结构示意图。图中八面体的中心代表金属M原子,顶点代表氨分子;四面体的中心代表硼原子,顶点代表氢原子。该晶体属立方晶系,晶胞棱边夹角均为90,棱长为apm,密度为3 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 。
。

①该晶体的化学式为_______ 。
②金属M原子与硼原子间最短距离为_______ pm。
③金属M的相对原子质量为_______ (列出表达式)。
(1)Pt的电子排布式为
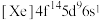 ,则Pt在元素周期表中的位置是
,则Pt在元素周期表中的位置是(2)
 中阴离子的立体构型名称是
中阴离子的立体构型名称是(3)科学家合成了一种含硼阴离子[
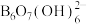 ],其结构如下图所示。其中硼原子的杂化方式为
],其结构如下图所示。其中硼原子的杂化方式为
(4)金属硼氢化物可用作储氢材料。如图是一种金属硼氢化物氨合物的晶体结构示意图。图中八面体的中心代表金属M原子,顶点代表氨分子;四面体的中心代表硼原子,顶点代表氢原子。该晶体属立方晶系,晶胞棱边夹角均为90,棱长为apm,密度为3
 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 。
。
①该晶体的化学式为
②金属M原子与硼原子间最短距离为
③金属M的相对原子质量为
您最近一年使用:0次
2022-04-01更新
|
495次组卷
|
5卷引用:河北省石家庄市第二中学2022届高三下学期5月模拟考试化学试题
解题方法
2 . 立方氮化硼硬度高,耐磨性好,在机械加工行业有广泛应用。制备立方氮化硼的一种方法为BCl3(g)+NH3(g)=BN(s)+3HCl(g),下列说法错误的是
| A.反应混合物中所有化学键均为共价键 |
| B.元素电负性大小为N>B |
| C.BCl3和BN均为共价晶体 |
D.形成BCl3时B原子先激发后杂化,其激发态价电子轨道表示式为: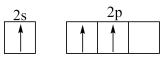 |
您最近一年使用:0次
3 . 为回收利用废镍催化剂(主要成分为NiO,另含Fe2O3、CaO、CuO、BaO等),科研人员研制了一种回收镍和硫酸铜晶体的新工艺。工艺流程如图所示:
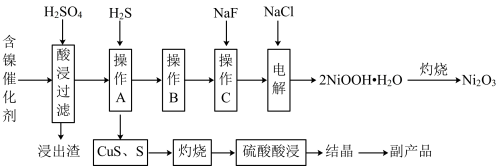
已知:常温下,有关氢氧化物开始沉淀和沉淀完全的pH如下表所示:
请回答下列问题:
(1)加快酸浸速率的常用措施有___________ (任写一条即可)。
(2)“浸出渣”主要成分为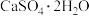 和
和___________ 两种物质。
(3)“操作B”的过程是:先在40~50℃温度下加入 ,其作用是
,其作用是___________ (用离子方程式表示);再调pH至___________ (填pH范围),操作B可除去溶液中的___________ 元素(填元素名称)。
(4)在碱性条件下,电解产生 的原理是:
的原理是: 在阳极被氧化为
在阳极被氧化为 ,
, 再被
再被 氧化产生
氧化产生 沉淀。请写出
沉淀。请写出 被
被 氧化得到
氧化得到 沉淀的离子方程式
沉淀的离子方程式___________ 。
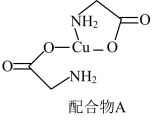
(5)配合物A常用于医药、电镀等方面,其结构如图所示。向硫酸铜溶液中滴入氨基乙酸钠(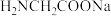 )即可得到它,配合物A中的配位原子的电负性由大到小的顺序是
)即可得到它,配合物A中的配位原子的电负性由大到小的顺序是___________ 。

已知:常温下,有关氢氧化物开始沉淀和沉淀完全的pH如下表所示:
| 氢氧化物 |  |  |  |
| 开始沉淀的pH | 1.5 | 6.5 | 7.7 |
| 沉淀完全的pH | 3.7 | 9.7 | 9.2 |
请回答下列问题:
(1)加快酸浸速率的常用措施有
(2)“浸出渣”主要成分为
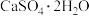 和
和(3)“操作B”的过程是:先在40~50℃温度下加入
 ,其作用是
,其作用是(4)在碱性条件下,电解产生
 的原理是:
的原理是: 在阳极被氧化为
在阳极被氧化为 ,
, 再被
再被 氧化产生
氧化产生 沉淀。请写出
沉淀。请写出 被
被 氧化得到
氧化得到 沉淀的离子方程式
沉淀的离子方程式(5)配合物A常用于医药、电镀等方面,其结构如图所示。向硫酸铜溶液中滴入氨基乙酸钠(
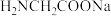 )即可得到它,配合物A中的配位原子的电负性由大到小的顺序是
)即可得到它,配合物A中的配位原子的电负性由大到小的顺序是
您最近一年使用:0次
2022-08-25更新
|
415次组卷
|
2卷引用:河北省石家庄市第九中学2022-2023高三上学期10月月考化学试题
名校
4 . 某科研团队经多次实验发现一种新型漂白剂的结构如图所示,其组成元素均为短周期元素,其中 与
与 同周期,
同周期, 与
与 对应的简单离子核外电子排布相同,且
对应的简单离子核外电子排布相同,且 、
、 、
、 的最外层电子数之和等于
的最外层电子数之和等于 的最外层电子数,下列说法错误的是
的最外层电子数,下列说法错误的是
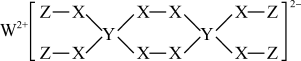
 与
与 同周期,
同周期, 与
与 对应的简单离子核外电子排布相同,且
对应的简单离子核外电子排布相同,且 、
、 、
、 的最外层电子数之和等于
的最外层电子数之和等于 的最外层电子数,下列说法错误的是
的最外层电子数,下列说法错误的是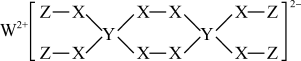
A.四种元素中 的电负性最大 的电负性最大 |
B. 该物质中含有 该物质中含有 配位键 配位键 |
C. 的最高价氧化物对应的水化物是一元弱酸 的最高价氧化物对应的水化物是一元弱酸 |
D.第一电离能介于 与 与 之间的同周期元素只有3种 之间的同周期元素只有3种 |
您最近一年使用:0次
2023-01-02更新
|
508次组卷
|
2卷引用:河北省石家庄实验中学2022-2023学年高二上学期期末考试化学试题
名校
解题方法
5 . 在碱性溶液中,Cu2+可以与缩二脲形成紫色配离子,其结构如图所示。下列说法错误的是
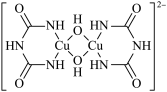

| A.该配离子与水分子形成氢键的原子只有N和O |
| B.该配离子中铜离子的配位数是4 |
| C.基态Cu原子的价电子排布式是 3d104s1 |
| D.该配离子中非金属元素的电负性大小顺序为O>N>C>H |
您最近一年使用:0次
2021-04-29更新
|
916次组卷
|
19卷引用:河北省石家庄市第二中学2021届高三3月学情考试化学试题
河北省石家庄市第二中学2021届高三3月学情考试化学试题河北省石家庄市第二十四中学2020-2021学年高二第二学期期中考试化学试题湖北省2021年普通高中学业水平选择考适应性测试化学试题(已下线)解密13 物质结构与性质(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练湖北武汉市蔡甸区汉阳一中2020-2021学年高二下学期3月月考化学试题辽宁省实验中学东戴河分校两校2020-2021学年高二4月联考化学试题四川省成都市树德中学2020-2021学年高二下学期4月月考化学试题(已下线)押山东卷第04题 物质结构与性质选择题-备战2021年高考化学临考题号押题(山东卷)山东省滨州市无棣县2020-2021学年高二下学期期中考试化学试题福建省连城县第一中学2021-2022学年高三上学期10月月考化学试题(已下线)卷14 物质结构与性质选择题-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)浙江金华第一中学2021-2022学年高二下学期期中考试化学试题第三章 本章达标检测2北京市海淀实验中学2022-2023学年高三上学期10月学科展示化学试题(已下线)专题十 物质结构与性质(选择性必修2)能力提升检测卷(测)-2023年高考化学一轮复习讲练测(新教材新高考)江西省景德镇一中2022-2023学年高二上学期期中考试化学试题山东省菏泽市单县二中2021-2022学年高二下学期开学考试 化学试题(已下线)专题33 物质结构与性质基础-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)第7讲 配合物与超分子
9-10高二下·吉林·期中
名校
解题方法
6 . 现有三种元素的基态原子的电子排布式如下:
①1s22s22p63s23p4;②1s22s22p63s23p3;③1s22s22p5。
则下列有关比较中正确的是
①1s22s22p63s23p4;②1s22s22p63s23p3;③1s22s22p5。
则下列有关比较中正确的是
| A.第一电离能:③>②>① |
| B.原子半径:③>②>① |
| C.电负性:③>②>① |
| D.最高正化合价:③>②>① |
您最近一年使用:0次
2021-12-04更新
|
1050次组卷
|
92卷引用:河北省石家庄市鹿泉一中2017-2018学年高二3月月考化学试题
河北省石家庄市鹿泉一中2017-2018学年高二3月月考化学试题河北省石家庄市启明中学2019-2020学年高二四月月考化学试题河北省石家庄市第一中学2019-2020学年高二下学期第一次月考化学试题(已下线)2009一2010年度吉林一中下学期高二期中考试化学卷(已下线)2010年厦门一中高二暑期水平测试(已下线)09-10年辽宁大连23中高二下学期期末考试化学卷(已下线)09~10年牡丹江一中高二下学期期末考试化学卷(已下线)2011-2012学年四川省南山中学高二上学期期末模拟考试化学试卷(已下线)2011--2012学年四川省成都二十中高二上学期期中考试化学试卷(已下线)2011-2012学年山西省忻州一中高二下学期第一次月考化学试卷(已下线)2011-2012学年黑龙江省鹤岗一中高二下学期期中考试化学试卷(已下线)2011-2012学年湖北省武汉市五校高二下学期期中统考化学试卷(已下线)2011-2012年黑龙江龙东地区高二下学期期末考试化学试卷(已下线)2011-2012学年辽宁省沈阳二中高二下学期期中考试化学试卷(已下线)2012-2013学年黑龙江省鹤岗一中高二下学期期中考试化学试卷(已下线)2012-2013学年辽宁葫芦岛第一高级中学高二下学期期中考试化学试卷(已下线)2012-2013学年山东省济南一中高二下学期期中考试理科化学试卷(已下线)2012-2013学年黑龙江省鹤岗一中高二下学期期末考试化学试卷(已下线)2013届浙江省台州中学高三第一次统练化学试卷(已下线)2013-2014广西桂林中学高二下学期期中考试化学试卷(已下线)2013-2014黑龙江省鹤岗一中高二下学期期末考试化学试卷2014-2015江苏省射阳县盘湾中学高二上学期期末考试化学试卷2013-2014山东省即墨市高二下学期期中考试化学试卷2014-2015学年辽宁省沈阳市沈阳二中高二下期中化学试卷2014-2015学年湖北省部分重点高中高二下期末考试化学试卷2016届浙江省慈溪中学高三上学期期中考试化学试卷2015-2016学年四川省雅安市天全中学高二上学期期中测试化学试卷2015-2016学年安徽省六安一中高二上学期期末化学试卷2015-2016学年福建省师大附中高二上学期期末化学试卷2015-2016学年吉林省汪清六中高二3月月考化学试卷2015-2016学年吉林省辽源市田家炳高中高二下期中化学试卷2015-2016学年吉林省扶余一中高二下学期期中考试化学试卷2015-2016学年云南省德宏州芒一中高二下学期期末化学试卷2015-2016学年吉林省汪清六中高二下学期期末化学试卷2016-2017学年河南省郑州市第一中学高二下学期入学测试理综化学试卷2016-2017学年黑龙江哈三中高二下学期4月月考(验收)考试化学试卷河南省郑州市八校2016-2017学年高二下学期期中联考化学试题江苏省泰州市姜堰区2016-2017学年高二下学期期中考试化学试题山西省大同市第一中学2016-2017学年高二5月月考化学试题河北省唐山市开滦第二中学2016-2017学年高二6月月考化学试题福建省三明市第一中学2016-2017学年高二下学期第二次月考化学试题河北省馆陶县第一中学2016-2017学年高二下学期期末考试化学试题新疆呼图壁县第一中学2016-2017学年高二下学期期末考试化学试题河南省焦作市博爱一中2016-2017学年高二下学期第一次月考化学试题辽宁省实验中学分校2016-2017学年高二6月月考化学试题2017-2018学年人教版高中化学选修三 模块综合质量检测【全国百强校】内蒙古集宁一中(东校区)2017-2018学年高二下学期期中考试化学试题【全国百强校】广东省佛山市第一中学2017-2018学年高二下学期期中考试(理)化学试题【全国百强校】广东省中山市第一中学2017-2018学年高二下学期第二次段考化学试题河南省济源第一中学2017-2018学年高二下期6月月考化学试题陕西省西安中学2017-2018学年高二(平行班)下学期期末考试化学试题山东省微山县第二中学2018-2019学年高二上学期第三学段教学质量监测化学试题吉林省吉林市第五十五中学2018-2019学年高二下学期3月月考化学试题【全国百强校】内蒙古自治区赤峰市第二中学2018-2019学年高二下学期4月月考化学试题山西省阳泉市第二中学2018-2019学年高二下学期期中考试化学试题福建省平和县第一中学2018-2019学年高二下学期第二次月考化学试题黑龙江省哈尔滨市阿城区第二中学2018-2019学年高二下学期期中考试化学试题陕西省西安中学2018-2019学年高二下学期期末考试化学试题甘肃省临泽县第一中学2018-2019学年高二下学期期末考试化学试题甘肃省张掖市临泽一中2018-2019学年高二下学期期末考试化学试题河北省秦皇岛市卢龙中学2018-2019学年高二下学期期末考试化学试题湖北省宜昌市第二中学2018-2019学年高二上学期期中考试化学试题辽宁省实验中学东戴河分校2019-2020学年高二12月月考化学试题吉林省辽源市东辽县第一高级中学2019-2020高二5月月考化学试题宁夏银川市长庆高级中学2019-2020学年高二下学期期中考试化学试题山西省晋中市平遥中学2019-2020高二下学期在线学习质量检测化学试题山西省忻州市第二中学2019-2020高二下学期3月考试化学试题陕西省西安市西北工业大学附属中学2019-2020学年高二下学期5月考试化学试题陕西省宝鸡市渭滨区2019-2020学年高二下学期期末考试化学试题宁夏青铜峡市高级中学(吴忠中学青铜峡分校)2019-2020学年高二下学期期末考试化学试题吉林省吉林地区普通高中友好学校联合体第三十届基础年段2019-2020学年高二下学期期末联考化学试题山西省晋中市祁县中学校2019-2020学年高二下学期6月月考化学试题陕西省咸阳市实验中学2020-2021学年高二上学期第一次月考化学试题天津市宝坻区宝坻九中2021届高三上学期第一次月考化学试题四川省内江市威远中学2020-2021学年高二上学期期中考试化学试题(鲁科版2019)选择性必修2 第1章 原子结构与元素性质 第3节 元素性质及其变化规律(已下线)第1章 原子结构与元素性质(基础过关)-2020-2021学年高二化学单元测试定心卷(鲁科版2019选择性必修2)新疆维吾尔自治区新源县第二中学2019-2020学年高二上学期第一次阶段测试化学试题吉林省吉化第一高级中学校2020-2021学年高二下学期3月月考化学试题新疆新源县第二中学2018-2019学年高二下学期期末考试化学试题吉林省通化县综合高级中学2020-2021学年高二下学期期中考试化学试题宁夏青铜峡市高级中学2020-2021学年高二下学期期中考试化学试题甘肃省兰州市第二十七中学2022届高三上学期8月月考化学试题(已下线)第30讲 原子结构与性质(讲) — 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)北京市第四中学2021-2022学年高二上学期期末考试化学试题吉林省长春市第八中学2021-2022学年高二下学期线上月考化学试题福建省福州市四校联盟2021-2022学年高二下学期期中联考化学试题福建省建瓯市芝华中学2021-2022学年高二下学期第一次阶段考化学试题四川省平昌县得胜中学2021-2022学年高二上学期10月月考化学试题宁夏吴忠市吴忠中学2022-2023学年高三上学期阶段性测试 化学试题辽宁省大石桥市第三高级中学2021-2022学年高二12月月考化学试题宁夏青铜峡市宁朔中学2022-2023学年高二下学期期中考试化学试题
名校
7 . Q、X、Y、Z、M、W是原子序数依次增大的短周期主族元素,其中X、Y、Z同周期,Y与M同主族,Z与W同主族。基态Y、Z原子核外电子均有5种空间运动状态,这六种元素形成的一种化合物结构如图所示。下列说法正确的是
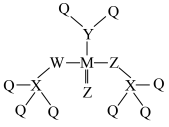

| A.第一电离能:Z>Y>X |
| B.电负性:Z>M>W |
| C.Q、X、Y三种元素组成的化合物既可能呈酸性,也可能呈碱性 |
| D.Y和Z的简单氢化物相比较:沸点Y>Z,稳定性Y>Z |
您最近一年使用:0次
13-14高二上·江苏泰州·期中
名校
解题方法
8 . 如图是第三周期11~17号元素某些性质变化趋势的柱形图,下列有关说法中正确的是
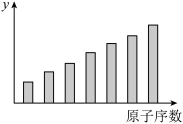
| A.y轴表示的可能是第一电离能 |
| B.y轴表示的可能是电负性 |
| C.y轴表示的可能是原子半径 |
| D.y轴表示的可能是形成基态离子转移的电子数 |
您最近一年使用:0次
2021-04-24更新
|
1003次组卷
|
51卷引用:河北省石家庄市第二十七中学2022-2023学年高三上学期九月月考化学试题
河北省石家庄市第二十七中学2022-2023学年高三上学期九月月考化学试题(已下线)2013-2014学年江苏省泰州市姜堰区高二上学期期中考试化学试卷2015-2016学年黑龙江省哈尔滨六中高二下期中化学试卷2016-2017学年河南省商丘市第一高级中学高二上学期期末考试化学试卷湖北省蕲春县2016-2017学年高二下学期期中考试化学试题2018版化学(苏教版)高考总复习专题十一课时跟踪训练--原子结构与元素的性质山东师范大学附属中学2017-2018学年高二下学期期中考试(理)化学试题山东省师范大学附属中学2017-2018学年高二下学期第七次学分认定考试(期中)(理)化学试题【全国百强校】黑龙江省实验中学2017-2018学年高二下学期期中考试(理)化学试题【全国百强校】山西省大同市第一中学2017-2018学年高二5月月考化学试题河南省兰考县第二高级中学2017-2018学年高二下学期期中考试化学试题吉林省辽源市田家炳高级中学2018-2019学年高二下学期期中考试化学试题山西省阳泉市第二中学2018-2019学年高二下学期期中考试化学试题鲁科版高中化学选修3模块综合测评卷黑龙江省哈尔滨市呼兰一中、阿城二中、宾县三中、尚志五中四校2018-2019学年高二下学期期中考试化学试题福建省平和县第一中学2018-2019学年高二下学期期末考试化学试题新疆阿勒泰地区第二高级中学2018-2019学年高二下学期期末(A卷)化学试题山东省济宁市2018-2019学年高二期末模块检测化学试题宁夏回族自治区石嘴山市平罗中学2019-2020学年高二上学期期中考试化学试题四川省南充市白塔中学2019-2020学年高二上学期期中考试化学试题人教化学选修3第一章第二节课时5福建省福州市格致中学2018-2019学年高二下学期期中考试化学试题天津市第二十中学2019-2020学年高二下学期阶段性检测化学试题第1章 原子结构——C挑战区 模拟高考(鲁科版选修3)福建省建瓯市芝华中学2019-2020学年高二下学期居家学习检测化学试题安徽省定远县育才学校2019-2020学年高一6月月考化学试题安徽省安庆市太湖县太湖中学2019-2020学年高二下学期3月线上考试化学试题安徽省安庆市太湖县2019-2020学年高二下学期期中质量调研考试化学试题福建省建瓯市芝华中学2019-2020学年高二下学期第一次阶段考试化学试题河南省洛阳市2019-2020学年高二下学期期末质量检测化学试题(已下线)第35讲 原子结构与性质(精练)-2021年高考化学一轮复习讲练测(已下线)第1章 原子结构与元素性质(基础过关)-2020-2021学年高二化学单元测试定心卷(鲁科版2019选择性必修2)新疆维吾尔自治区乌鲁木齐市第四中学2020-2021学年高二年级下学期期中考试化学试题吉林省长春市清蒲中学2020-2021学年高二下学期期中考试化学试题福建省漳州市正兴学校等三校2021-2022学年高二下学期期中联考化学试题甘肃省兰州第一中学2021-2022学年高二下学期期中考试化学试题福建省宁德市柘荣县第一中学2021-2022学年高二下学期月考八化学试题(已下线)专题13 原子结构与性质-2023年高考化学一轮复习小题多维练(全国通用)新疆乌鲁木齐高级中学2021-2022学年高二上学期期末考试化学试题湖南省长沙市长郡梅溪湖中学2021-2022学年高二下学期入学考试化学试题新疆疏勒县实验学校2021-2022学年高二下学期期末考试化学试题陕西省西安市阎良区关山中学2021-2022学年高二下学期期末质量检测化学试题重庆市缙云教育联盟2022-2023学年高二上学期期末联考化学试题黑龙江省大庆市大庆中学2022-2023学年高二下学期4月月考化学试题新疆维吾尔自治区皮山县高级中学2022-2023学年高二下学期4月期中化学试题福建省南平市浦城县2022-2023学年高二下学期期中考试化学试题重庆市2022-2023学年高二上学期期末考试化学试题(已下线)寒假作业10 原子结构与性质-【寒假分层作业】2024年高二化学寒假培优练(人教版2019)天津市九十六中学2023-2024学年高三上学期12月月考化学试题四川省阆中中学校2023-2024学年高二下学期4月期中化学试题(已下线)清单01 原子结构与性质(考点清单)(讲+练)-2023-2024学年高二化学下学期期末考点大串讲(人教版2019)
9 . 材料是入类进步的基石,深入认识物质的结构有助于进一步开发新的材料。回答下列问题。
(1)B和Ni均为新材料的主角。
①按照杂化轨道理论,基态B原子的价电子先激发,再杂化成键形成 。杂化前,处于激发态的B原子的价电子轨道表示式为
。杂化前,处于激发态的B原子的价电子轨道表示式为___________ (填编号)。
A.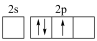 B.
B.  C.
C.  D.
D.
② 常温下呈液态,其分子空间构型为正四面体形。其易溶
常温下呈液态,其分子空间构型为正四面体形。其易溶 、苯等有机溶剂的原因是
、苯等有机溶剂的原因是___________ 。
(2)亚铁氰化钾具有防止食盐结块、保持食盐松散等作用,其化学式为 ,所含元素电负性由大到小的顺序为
,所含元素电负性由大到小的顺序为___________ ,1mol  含有σ键的物质的量为
含有σ键的物质的量为___________ 。
(3)铀氮化合物是核燃料循环系统中的重要物质。已知 。反应所得的气态产物中属于非极性分子的有
。反应所得的气态产物中属于非极性分子的有___________ (填化学式);反应中断裂的化学键有___________ 。(填编号)。
a.氢键 b.极性键 c.非极性键 d.离子键 e.配位键
(4)某锂电池的负极材料是锂原子嵌入石墨烯层间,其晶胞结构(底边为平行四边形)如图所示。

该晶体的化学式为___________ 。
(1)B和Ni均为新材料的主角。
①按照杂化轨道理论,基态B原子的价电子先激发,再杂化成键形成
 。杂化前,处于激发态的B原子的价电子轨道表示式为
。杂化前,处于激发态的B原子的价电子轨道表示式为A.
 B.
B.  C.
C.  D.
D.
②
 常温下呈液态,其分子空间构型为正四面体形。其易溶
常温下呈液态,其分子空间构型为正四面体形。其易溶 、苯等有机溶剂的原因是
、苯等有机溶剂的原因是(2)亚铁氰化钾具有防止食盐结块、保持食盐松散等作用,其化学式为
 ,所含元素电负性由大到小的顺序为
,所含元素电负性由大到小的顺序为 含有σ键的物质的量为
含有σ键的物质的量为(3)铀氮化合物是核燃料循环系统中的重要物质。已知
 。反应所得的气态产物中属于非极性分子的有
。反应所得的气态产物中属于非极性分子的有a.氢键 b.极性键 c.非极性键 d.离子键 e.配位键
(4)某锂电池的负极材料是锂原子嵌入石墨烯层间,其晶胞结构(底边为平行四边形)如图所示。

该晶体的化学式为
您最近一年使用:0次
2023-10-04更新
|
288次组卷
|
2卷引用:河北省石家庄实验中学2022-2023学年高二上学期期末考试化学试题
名校
10 . 钛硅分子筛是一种新型固体催化剂,可催化合成重要有机合成活性试剂甲乙酮肟(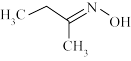 )。回答下列问题:
)。回答下列问题:
(1)基态硅原子的核外电子空间运动状态有____ 种。
(2)甲乙酮肟中同周期三种元素电负性由大到小的顺序为____ ,氮原子的杂化方式为____ ,C=N与C—C键夹角____ (填“<”“>”或“=”)C=N与N—O键夹角。
(3)TiO2和TiCl4均是制备钛硅分子筛的重要中间体。
①TiO2与光气COCl2反应可用于制取四氯化钛。COCl2中σ键和π键的数目比为____ ,其空间构型为____ 。
②TiCl4与金属Ti在高温条件下可反应生成TiCl3,TiCl3中Ti3+极易被氧化,还原性很强。试解释Ti3+还原性强的原因____ 。
(4)研究表明,在TiO2通过氮掺杂反应生成TiO2-mNn,能使TiO2对可见光具有活性,反应如图所示。

若TiO2晶体密度为ρg·cm-3,则阿伏加德罗常数的值NA=____ ,TiO2-mNn晶体中m=____ 。
 )。回答下列问题:
)。回答下列问题:(1)基态硅原子的核外电子空间运动状态有
(2)甲乙酮肟中同周期三种元素电负性由大到小的顺序为
(3)TiO2和TiCl4均是制备钛硅分子筛的重要中间体。
①TiO2与光气COCl2反应可用于制取四氯化钛。COCl2中σ键和π键的数目比为
②TiCl4与金属Ti在高温条件下可反应生成TiCl3,TiCl3中Ti3+极易被氧化,还原性很强。试解释Ti3+还原性强的原因
(4)研究表明,在TiO2通过氮掺杂反应生成TiO2-mNn,能使TiO2对可见光具有活性,反应如图所示。

若TiO2晶体密度为ρg·cm-3,则阿伏加德罗常数的值NA=
您最近一年使用:0次
2022-02-25更新
|
344次组卷
|
4卷引用:河北省石家庄市2022届高三毕业班教学质量检测二(一模)(结构与性质)
(已下线)河北省石家庄市2022届高三毕业班教学质量检测二(一模)(结构与性质)湖南省百师联盟2021-2022学年高三下学期开年摸底联考化学试题山西省吕梁市2021-2022学年高三下学期开学考试理综化学试题山东省烟台第二中学2021-2022学年高三下学期开年摸底联考化学试题



