名校
解题方法
1 . 元素X的基态原子中的电子共有7个能级,且最外层电子数为1,X原子的内层轨道全部排满电子.在气体分析中,常用XCl的盐酸溶液吸收并定量测定CO的含量,其化学反应如下:2XCl+2CO+2H2O═X2Cl2•2CO•2H2O
(1)X基态原子的电子排布式为______ .
(2)C、H、O三种原子的电负性由大到小的顺序为______ .
(3)X2Cl2•2CO•2H2O是一种配合物,其结构如图1所示:
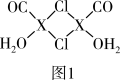
①与CO为互为等电子体的分子是______ .
②该配合物中氯原子的杂化方式为______ .
③在X2Cl2•2CO•2H2O中,每个X原子能与其他原子形成3个配位键,在图中用“→”标出相应的配位键______ .
(4)XCl的晶胞如2图所示,距离每个X+最近的Cl-的个数为______ .XCl的化学式__________

已知X的半径为apm,此晶胞的密度为dg/cm3,则阿伏加 德罗常数NA=_____________ (无需化简,列式即可)。
(1)X基态原子的电子排布式为
(2)C、H、O三种原子的电负性由大到小的顺序为
(3)X2Cl2•2CO•2H2O是一种配合物,其结构如图1所示:

①与CO为互为等电子体的分子是
②该配合物中氯原子的杂化方式为
③在X2Cl2•2CO•2H2O中,每个X原子能与其他原子形成3个配位键,在图中用“→”标出相应的配位键
(4)XCl的晶胞如2图所示,距离每个X+最近的Cl-的个数为

已知X的半径为apm,此晶胞的密度为dg/cm3,则阿伏加 德罗常数NA=
您最近一年使用:0次
2 . 已知A、B、D、E、G、X、Y、Z八种元素的原子序数依次增大。其中,A原子核外电子只有1种运动状态;基态B、E原子的2p轨道均含2个未成对电子;G是周期表中电负性最大的元素;Y和G同主族,X和Y同周期,且X离子是同周期元素简单离子中半径最小的;Z是八种元素中唯一的第四周期元素位于ds区,且基态原子核外只有1个未成对电子其余均为成对电子。推断出元素符号及相应化学式,并回答下列问题:
(1)基态Z原子的简化核外电子排布式:_______ ,基态E原子价层电子轨道表达式:_______ ,基态X原子的核外电子排布共有_______ 个能级。
(2)键能:G-G_______ Y-Y(填“>或<”,后同);B和D的第三电离能:B_______ D。
(3)A2E分子的VSEPR理想模型为_______ ;已知DA3溶于A2E溶液呈碱性,试在方框内画出DA3与A2E的分子间形成的氢键_______ 。

(4)B2A2分子中σ键和π键的比例_______ ;B2A2、E2在NaOH溶液中可构建燃料电池,试写出该燃料电池负极的电极反应式:_______ 。
(1)基态Z原子的简化核外电子排布式:
(2)键能:G-G
(3)A2E分子的VSEPR理想模型为

(4)B2A2分子中σ键和π键的比例
您最近一年使用:0次
3 . 图一是Na、Cu、Si、H、C、N等元素单质的熔点高低顺序,其中c、d均为热和电的良导体。
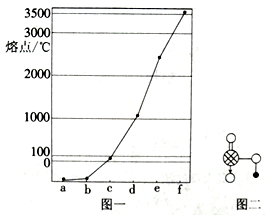
(1)单质d对应元素的基态原子M层电子排布式为_____ ,该元素位于元素周期表的____ 区。
(2)单质a、f对应的元素以原子个数比1 : 1形成的分子(相同条件下对H2的相对密度为13)中含σ键和π键的个数比为____ ,该分子中心原子的杂化轨道类型为________ 。
(3)单质b对应元素原子的最高能级电子云轮廓图形状为____ 形,将b的简单氢化 物溶于水后的溶液滴加到AgNO3溶液中至过量,所得络离子的结构可用示意图表示为_______ 。
(4)图二是上述六种元素中的一种元素形成的含氧酸的结构,请简要说明该物质易溶于水的两个原因_____________ 。

(1)单质d对应元素的基态原子M层电子排布式为
(2)单质a、f对应的元素以原子个数比1 : 1形成的分子(相同条件下对H2的相对密度为13)中含σ键和π键的个数比为
(3)单质b对应元素原子的最高能级电子云轮廓图形状为
(4)图二是上述六种元素中的一种元素形成的含氧酸的结构,请简要说明该物质易溶于水的两个原因
您最近一年使用:0次
名校
解题方法
4 . 硼(B)及其化合物是结构化学的重要研究对象。请回答下列问题:
(1)和B同主族电负性最小的元素[放射性元素(周期表中84号及其后的元素)除外]的价电子排布式为___________ ,Be、B、C的第一电离能由大到小的顺序是___________________ (用元素符号表示)
(2)无机苯(B3N3H6)与苯结构相似,其中B的杂化方式为______________ ,1mol B3N3H6中σ键的数目为______________________ 。
(3)Al和B同主族,其化合物氟化铝的熔沸点远远高于氯化铝,试解释其原因________________ 。
(4)将硼砂(NaB4O7)和NH4C1共热可得白色固体BN和B2O3、方程式_________________________ 。
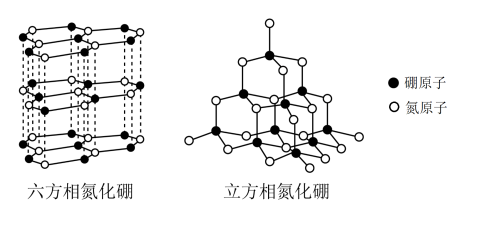
氮化硼有两种晶型结构,一种是六方氮化硼,其结构与石墨相似却不导电,原因是__________________ ;另一种是类似于金刚石结构的立方氮化硼,已知晶胞边长为361.5pm,N原子半径为a pm,则B原子半径为___________ pm(只要求列算式)。
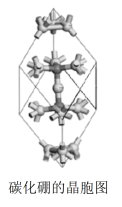
(5)碳化硼是除金刚石和氮化硼外最硬的固体,下图是碳化硼的晶胞简图,该图给出了晶胞中的所有原子,除“三原子”(中心原子和其相连的2个原子)外,晶胞的其余原子都是B12多面体中的1个原子,B12多面体的其他原子都不在晶胞内,均未画出。图中原子旁的短棍表示该原子与其他原子相连,若上述三原子都是碳原子,写出碳化硼的化学式_____________________ 。
(1)和B同主族电负性最小的元素[放射性元素(周期表中84号及其后的元素)除外]的价电子排布式为
(2)无机苯(B3N3H6)与苯结构相似,其中B的杂化方式为
(3)Al和B同主族,其化合物氟化铝的熔沸点远远高于氯化铝,试解释其原因
(4)将硼砂(NaB4O7)和NH4C1共热可得白色固体BN和B2O3、方程式
氮化硼有两种晶型结构,一种是六方氮化硼,其结构与石墨相似却不导电,原因是

(5)碳化硼是除金刚石和氮化硼外最硬的固体,下图是碳化硼的晶胞简图,该图给出了晶胞中的所有原子,除“三原子”(中心原子和其相连的2个原子)外,晶胞的其余原子都是B12多面体中的1个原子,B12多面体的其他原子都不在晶胞内,均未画出。图中原子旁的短棍表示该原子与其他原子相连,若上述三原子都是碳原子,写出碳化硼的化学式

您最近一年使用:0次
5 . “嫦娥石”是中国首次在月球上发现的新矿物,其主要由Ca、Fe、P、O和Y(钇,原子序数比Fe大13)组成,下列说法正确的是
| A.Y位于元素周期表的第ⅢB族 |
| B.基态Ca原子的核外电子填充在6个轨道中 |
| C.Fe2+和 Fe3+中未成对电子个数之比为4:5 |
| D.5种元素中,电负性最大的是P |
您最近一年使用:0次
名校
解题方法
6 . 砷的一些化合物常用作半导体、除草剂、杀鼠药等。回答下列问题:
(1)基态As原子的核外电子排布式为[Ar]__________ ,有___________ 个未成对电子。
(2)镓氮砷合金材料的太阳能电池效率达40%。Ga、N、As电负性由大至小的顺序是_____________ 。
(3)As4O6的分子结构如图所示,其中As原子的杂化方式为____________ ,1mol 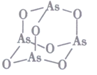 As4O6含有σ键的物质的量为
As4O6含有σ键的物质的量为________ mol。
(4)晶胞有两个基本要素:
①原子坐标参数,表示晶胞内部各原子的相对位置,LiZnAs基稀磁半导体的晶胞如图所示,其中原子
坐标参数A处Li为(0,0, );B处As为(
);B处As为( ,
, ,
, );C处Li的坐标参数为
);C处Li的坐标参数为_____________ 。
②晶胞参数,描述晶胞的大小和形状,已知LiZnAs单晶的晶胞参数α=594 pm,NA表示阿伏伽德罗常数的数值,其密度为____________ g·cm-3(列出计算式即可)。
(1)基态As原子的核外电子排布式为[Ar]
(2)镓氮砷合金材料的太阳能电池效率达40%。Ga、N、As电负性由大至小的顺序是
(3)As4O6的分子结构如图所示,其中As原子的杂化方式为
 As4O6含有σ键的物质的量为
As4O6含有σ键的物质的量为(4)晶胞有两个基本要素:
①原子坐标参数,表示晶胞内部各原子的相对位置,LiZnAs基稀磁半导体的晶胞如图所示,其中原子
坐标参数A处Li为(0,0,
 );B处As为(
);B处As为( ,
, ,
, );C处Li的坐标参数为
);C处Li的坐标参数为②晶胞参数,描述晶胞的大小和形状,已知LiZnAs单晶的晶胞参数α=594 pm,NA表示阿伏伽德罗常数的数值,其密度为
您最近一年使用:0次
名校
解题方法
7 . 化合物XYZ4ME4可作肥料,所含的5种元素位于主族,在每个短周期均有分布,仅有Y和M同族。Y的基态原子价层p轨道半充满,X的基态原子价层电子排布式为nsn-1,X与M同周期,E在地壳中含量最多。下列说法正确的是
| A.元素电负性:E>Y>Z | B.1mol M中含有共价键数目为4NA |
| C.半径:X2+>E2- | D.YZ3和YE 的空间结构均为三角锥形 的空间结构均为三角锥形 |
您最近一年使用:0次
名校
解题方法
8 . 蓝铜矿的主要成分为2CuCO3·Ca(OH)2,将它与焦炭一起加热可以生成Cu、CO2和H2O。下列说法正确的是
| A.Cu是第四周期第ⅦB族元素 |
| B.0.1mol[Cu(H2O)4]2+中所含配位键的物质的量为0.8mol |
| C.电负性:O>C>H |
| D.将0.1L0.1mol/L[Cu(NH3)4](OH)2加入足量的MgCl2溶液中,理论上可得到0.2molMg(OH)2 |
您最近一年使用:0次
名校
解题方法
9 . 物质W常用作漂白剂和氧化剂,其构成元素均为短周期主族元素,各元素原子半径与原子序数关系如下图所示,实验室常用 洗涤残留在试管壁上的Q单质。下列说法正确的是
洗涤残留在试管壁上的Q单质。下列说法正确的是
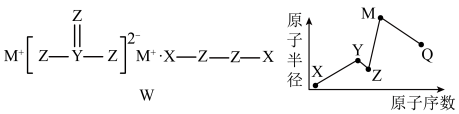
 洗涤残留在试管壁上的Q单质。下列说法正确的是
洗涤残留在试管壁上的Q单质。下列说法正确的是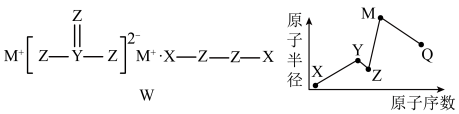
A.X可分别与Y、Z、Q形成 微粒 微粒 |
| B.Z分别与X、M形成的化合物所含化学键类型相同 |
| C.氢化物的沸点:Z>Y |
| D.电负性:M<Y<X<Z |
您最近一年使用:0次
解题方法
10 . 卢瑟福发现质子的核反应为 ;卢瑟福的学生查德威克发现中子的核反应为
;卢瑟福的学生查德威克发现中子的核反应为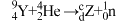 。下列说法错误的是
。下列说法错误的是
 ;卢瑟福的学生查德威克发现中子的核反应为
;卢瑟福的学生查德威克发现中子的核反应为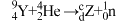 。下列说法错误的是
。下列说法错误的是| A.Y元素的第一电离能高于同周期相邻元素的 |
B.元素的电负性: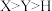 |
C. 和 和 的简单氢化物中中心原子的价层电子对数目相同 的简单氢化物中中心原子的价层电子对数目相同 |
D. 的空间结构为直线形 的空间结构为直线形 |
您最近一年使用:0次



