名校
解题方法
1 . 某锂盐的结构如图所示,其阴离子是由原子序数依次增大的短周期主族元素X、Y,Z、W形成,X,Y与Z同一周期,Y与W同族。下列说法正确的是( )
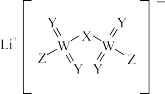
A.元素的电负性: | B.第一电离能: |
C.简单气态氢化物的热稳定性: | D.简单离子的半径: |
您最近一年使用:0次
2022-05-05更新
|
2589次组卷
|
16卷引用:河北省沧州市泊头市第一中学2023-2024学年高二上学期12月月考化学试题
河北省沧州市泊头市第一中学2023-2024学年高二上学期12月月考化学试题山东省济南市2022届高三第二次模拟化学试题安徽省怀宁中学2021-2022学年高二下学期5月阶段考试化学试题山东省济南第一中学2023届高三上学期开学考试化学试题辽宁省沈阳市第十中学2022-2023学年高二上学期期末综合测评化学试题新疆乌鲁木齐市第八中学2022-2023学年高二上学期期末考试化学试题贵州省江口中学2022-2023学年高二下学期3月份月考化学试题第一章 原子结构与性质(B卷·能力提升练)-2022-2023学年高二化学分层训练AB卷(人教版2019选择性必修2)云南省楚雄彝族自治州民族中学2022-2023学年高二下学期5月月考化学试题(已下线)2023年湖南卷高考真题变式题(选择题6-10)(已下线)选择题1-5湖南省邵阳市武冈市2023-2024学年高三上学期期中考试化学试题河南省驻马店市确山县第一高级中学2023~2024学年高二上学期第二次月考化学试题黑龙江省大兴安岭实验中学2023-2024学年高二下学期开学考试化学试卷宁夏石嘴山市第三中学2023-2024学年高二下学期3月月考化学试题山东省临沂市平邑县第一中学西校区2023-2024学年高二上学期1月份阶段性考试化学试题
名校
2 . 部分短周期元素原子半径的相对大小、最高正价或最低负价随原子序数的变化关系如图所示,下列说法正确的是


| A.离子半径的大小顺序:e>f>g>h | B.与x形成简单化合物的沸点:y>z>d |
| C.y、z、d三种元素第一电离能和电负性的大小顺序不一致 | D.e、f、g、h四种元素对应最高价氧化物的水化物相互之间均能发生反应 |
您最近一年使用:0次
2021-01-09更新
|
2094次组卷
|
8卷引用:河北省沧州市东光县等3地河北省盐山中学等2校2022-2023学年高二下学期3月月考化学试题
名校
3 . 三苯胺及其衍生物可用于新型电致发光材料、特种染料和医药的合成,一种三苯胺单醛的修饰路线如图所示,下列说法错误的是

| A.电负性:H<C<O | B.甲中所有碳原子一定在同一平面 |
| C.乙的核磁共振氢谱有7组峰 | D.该反应发生了 键的断裂 键的断裂 |
您最近一年使用:0次
名校
解题方法
4 . 基于所学内容回答问题
(1)基态铜原子的价电子排布式为_________ ,其核外电子的空间运动状态有________ 种;As原子的价电子排布图为________________ 。
(2) 与
与 同周期,
同周期,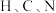 三种元素的电负性从小到大的顺序为
三种元素的电负性从小到大的顺序为________ ; 、
、 、
、 的第一电离能从大到小的顺序为
的第一电离能从大到小的顺序为________________ 。
(3) 的电子式
的电子式_________ , 的沸点高于
的沸点高于 的原因是
的原因是_________ 。
(4)已知 的熔点高于
的熔点高于 的熔点,其原因是
的熔点,其原因是__________________ 。
(5)铜的某种氧化物的晶胞结构如图所示,若该晶胞中 原子与
原子与 原子之间的最近距离为apm,设阿伏加德罗常数的值为
原子之间的最近距离为apm,设阿伏加德罗常数的值为 ,则该晶胞的密度为
,则该晶胞的密度为_________  (填含
(填含 的表达式)。
的表达式)。
(1)基态铜原子的价电子排布式为
(2)
 与
与 同周期,
同周期,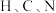 三种元素的电负性从小到大的顺序为
三种元素的电负性从小到大的顺序为 、
、 、
、 的第一电离能从大到小的顺序为
的第一电离能从大到小的顺序为(3)
 的电子式
的电子式 的沸点高于
的沸点高于 的原因是
的原因是(4)已知
 的熔点高于
的熔点高于 的熔点,其原因是
的熔点,其原因是(5)铜的某种氧化物的晶胞结构如图所示,若该晶胞中
 原子与
原子与 原子之间的最近距离为apm,设阿伏加德罗常数的值为
原子之间的最近距离为apm,设阿伏加德罗常数的值为 ,则该晶胞的密度为
,则该晶胞的密度为 (填含
(填含 的表达式)。
的表达式)。 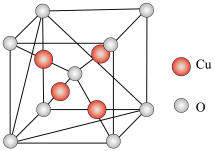
您最近一年使用:0次
2024-01-23更新
|
389次组卷
|
2卷引用:河北省沧州市泊头市第一中学2023-2024学年高二上学期12月月考化学试题
名校
5 . X、Y、Z、J、Q是原子序数依次增大,且分布在三个短周期的主族元素,Y元素原子的核外未成对电子数在同周期中最多,Y、Z同周期,Z、J同主族.下列说法错误的是
| A.电负性:Q>J;第一电离能:Y>Z | B.最高价含氧酸的酸性:Q>J |
C. 、 、 的中心原子杂化方式相同 的中心原子杂化方式相同 | D.简单离子半径:Y>Z、J>Q |
您最近一年使用:0次
2023-06-21更新
|
562次组卷
|
5卷引用:河北省泊头市第一中学2023-2024学年高三上学期开学考试化学试题
河北省泊头市第一中学2023-2024学年高三上学期开学考试化学试题河北省衡水市第二中学2023届高三下学期三模化学试题(已下线)第19讲元素周期律与元素周期表(已下线)开学摸底考试卷-2024年高考化学一轮复习考点通关卷(新高考通用)(已下线)考点18 元素周期律与元素周期表(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)
名校
6 . 某物质的结构如图所示。短周期元素X、Y、Z、W、M、Q的原子序数依次增大,已知X和W同周期,W和Q同主族。下列说法错误的是
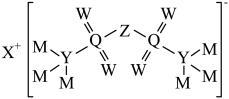

| A.电负性:M>W>Z>Y |
| B.Y、Z、W的简单氢化物的键角依次减小 |
| C.常温下,M的单质可以在水溶液中置换出W的单质 |
| D.W的单质一定为非极性分子 |
您最近一年使用:0次
7 . 甲基氯硅烷(CH3SiH2Cl)、乙二胺(NH2CH2CH2NH2)和乙二醇(HOCH2CH2OH)常用于制备硅橡胶和聚合物树脂。下列说法错误的是
| A.上述物质中硅和氮的杂化方式相同 |
| B.上述物质所含元素中,电负性的大小顺序为O>N>C>Si |
| C.乙二胺中氢键(N-H…N)的键能高于乙二醇中氢键(O-H…O)的键能 |
| D.上述物质所含元素中,第一电离能的大小顺序为N>O>C>Si |
您最近一年使用:0次
2024-03-27更新
|
252次组卷
|
2卷引用:河北省沧州市2024届高三下学期一模化学试卷
名校
8 . 2022年诺贝尔化学奖授予了点击化学领域的三位科学家。一价铜催化的叠氮化物-炔烃环加成反应可谓点击化学中的第一个经典之作,催化剂CuCl的晶体结构如图所示,下列说法错误的是
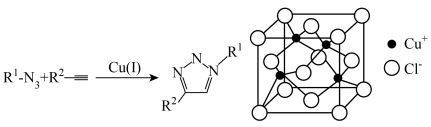

| A.N、O、Cu的电负性从大到小的顺序是N>O>Cu |
B.基态 的简化电子排布式为 的简化电子排布式为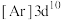 |
C.晶胞结构中, 的配位数为4 的配位数为4 |
D.若晶体的密度为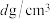 ,则晶胞参数 ,则晶胞参数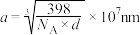 |
您最近一年使用:0次
名校
解题方法
9 . 硫酸铈铵[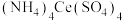 ,
,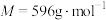 ]是分析化学中常用的滴定剂。以氟碳铈矿(含
]是分析化学中常用的滴定剂。以氟碳铈矿(含 、
、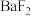 、
、 等)为原料制备硫酸铈铵的工艺流程如图所示。
等)为原料制备硫酸铈铵的工艺流程如图所示。
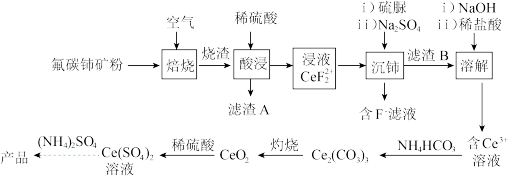
已知部分信息如下:
① 在空气中易被氧化为
在空气中易被氧化为 。
。
②“沉铈”时发生的反应之一: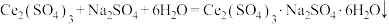 。
。
回答下列问题:
(1) 中非金属元素的电负性由大到小的顺序为
中非金属元素的电负性由大到小的顺序为___________ ; 的空间结构为
的空间结构为___________ 。
(2)“焙烧”时,为提高效率,可采用的措施为___________ (答两条)。
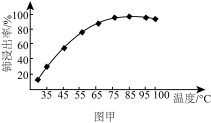
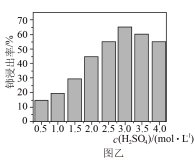
(3)“酸浸”中,铈浸出率与温度的关系如图甲所示,铈浸出率与硫酸浓度的关系如图乙所示。工业生产应选择的适宜条件是___________(填标号)。
(4)“沉铈”时,硫脲作___________ (填“还原剂”或“氧化剂”)。
(5)含 溶液转化为
溶液转化为 沉淀的离子方程式为
沉淀的离子方程式为___________ 。灼烧 时发生反应的化学方程式为
时发生反应的化学方程式为___________ 。
(6)测定产品纯度。称取 产品溶于水,配制成250mL溶液,准确量取25.00mL溶液于锥形瓶中,滴加
产品溶于水,配制成250mL溶液,准确量取25.00mL溶液于锥形瓶中,滴加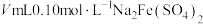 溶液时,恰好完全反应。已知:滴定反应为
溶液时,恰好完全反应。已知:滴定反应为 ,杂质不参与反应,该产品纯度为
,杂质不参与反应,该产品纯度为___________ %。
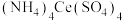 ,
,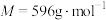 ]是分析化学中常用的滴定剂。以氟碳铈矿(含
]是分析化学中常用的滴定剂。以氟碳铈矿(含 、
、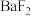 、
、 等)为原料制备硫酸铈铵的工艺流程如图所示。
等)为原料制备硫酸铈铵的工艺流程如图所示。
已知部分信息如下:
①
 在空气中易被氧化为
在空气中易被氧化为 。
。②“沉铈”时发生的反应之一:
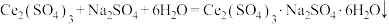 。
。回答下列问题:
(1)
 中非金属元素的电负性由大到小的顺序为
中非金属元素的电负性由大到小的顺序为 的空间结构为
的空间结构为(2)“焙烧”时,为提高效率,可采用的措施为
(3)“酸浸”中,铈浸出率与温度的关系如图甲所示,铈浸出率与硫酸浓度的关系如图乙所示。工业生产应选择的适宜条件是___________(填标号)。


A.65℃、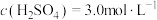 | B.85℃、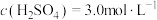 |
C.95℃、 | D.85℃、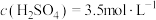 |
(4)“沉铈”时,硫脲作
(5)含
 溶液转化为
溶液转化为 沉淀的离子方程式为
沉淀的离子方程式为 时发生反应的化学方程式为
时发生反应的化学方程式为(6)测定产品纯度。称取
 产品溶于水,配制成250mL溶液,准确量取25.00mL溶液于锥形瓶中,滴加
产品溶于水,配制成250mL溶液,准确量取25.00mL溶液于锥形瓶中,滴加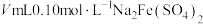 溶液时,恰好完全反应。已知:滴定反应为
溶液时,恰好完全反应。已知:滴定反应为 ,杂质不参与反应,该产品纯度为
,杂质不参与反应,该产品纯度为
您最近一年使用:0次
2024-01-15更新
|
242次组卷
|
2卷引用:河北省沧州市部分学校2023-2024学年高三上学期12月联考化学试题
名校
解题方法
10 . 完成下列问题
(1)C、N、Mg、Al、Si、Cu 是常见的六种元素,按要求回答下列问题:
①Cu位于元素周期表第_______ 周期第_______ 族。
②基态C原子核外电子排布式为_______ ;基态N原子核外有_______ 种运动状态的电子。
③基态Si原子核外电子占据的最高能级的电子云轮廓图为_______ 形。
④Mg、Al 两种元素中第一电离能较大的是_______ (填元素符号),原因为_______ 。
(2)几种元素的电负性数据如下表:
①AlF3的熔点_______ AlBr3的熔点(填“大于”、“小于”或“等于”),原因是_______ 。
②根据同一主族元素电负性递变规律,预测碘元素的电负性数值范围为_______ 。
③卤族元素之间可以形成化合物,则氯元素与碘元素形成的化合物ICl中,碘元素的化合价为_______ 。
(1)C、N、Mg、Al、Si、Cu 是常见的六种元素,按要求回答下列问题:
①Cu位于元素周期表第
②基态C原子核外电子排布式为
③基态Si原子核外电子占据的最高能级的电子云轮廓图为
④Mg、Al 两种元素中第一电离能较大的是
(2)几种元素的电负性数据如下表:
| O | F | Al | Br | …… |
| 3.5 | 4.0 | 1.5 | 2.8 | …… |
②根据同一主族元素电负性递变规律,预测碘元素的电负性数值范围为
③卤族元素之间可以形成化合物,则氯元素与碘元素形成的化合物ICl中,碘元素的化合价为
您最近一年使用:0次



