名校
解题方法
1 . 下列有关微拉性质的比较中,正确的是
A.原子半径: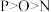 | B.最高正价: |
C.第一电离能: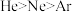 | D.电负性: |
您最近一年使用:0次
2021-09-22更新
|
465次组卷
|
5卷引用:福建泉州市第六中学2020-2021学年高二下学期期中考试化学试题
福建泉州市第六中学2020-2021学年高二下学期期中考试化学试题(已下线)第1章 原子结构与性质(章末检测)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修2)陕西省宝鸡市金台区2021-2022学年高二下学期期中考试化学试题吉林省吉林市田家炳高级中学2022-2023学年高二上学期期末线上考试化学试题四川省南充市阆中中学校2023-2024学年高二下学期3月月考化学试卷
名校
解题方法
2 . 咔唑(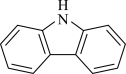 )是一种新型有机液体储氢介质。下列说法错误的是
)是一种新型有机液体储氢介质。下列说法错误的是
 )是一种新型有机液体储氢介质。下列说法错误的是
)是一种新型有机液体储氢介质。下列说法错误的是| A.电负性:N>C>H |
| B.同周期元素中第一电离能小于N的有4种 |
C.咔唑的沸点比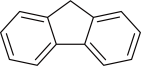 的沸点高 的沸点高 |
D.基态氮原子的外围电子轨道表示式不能写为 ,因为违背了洪特规则原理 ,因为违背了洪特规则原理 |
您最近一年使用:0次
2023-09-22更新
|
194次组卷
|
4卷引用:福建省泉州市部分中学2022-2023学年高二下学期期末联考化学试题
名校
解题方法
3 . 短周期主族元素X、Y、Z、W的原子序数依次增加,K、L、M均是由这些元素组成的氧化物,甲、乙分别是元素Y、W的单质,甲是常见的固体,乙是常见的气体。K是红棕色气体,丙的浓溶液具有强氧化性,上述物质的转化关系如图所示。下列说法不正确的是( )


| A.Y、Z、W三种元素电负性:W>Z>Y |
| B.Y、Z、W三种元素第一电离能:Z>W>Y |
| C.L的沸点一定比X、Y组成的化合物沸点高 |
| D.由X、Y、Z、W构成的化合物中只能含有共价键 |
您最近一年使用:0次
2020-06-24更新
|
556次组卷
|
6卷引用:福建省建瓯市芝华中学2019-2020学年高二下学期居家学习检测化学试题
4 . 短周期元素W、X、Y、Z原子序数依次递增,X、Z同主族,W、Y同主族。由上述元素组成的物质甲~已转化关系如图,乙、丙、丁、戊都是二元化合物,丁的焰色反应为黄色,己为淡黄色单质。下列说法错误的是
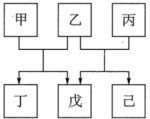

| A.只有甲的水溶液为碱性 | B.键角:丙>戊 |
| C.沸点:己>乙 | D.电负性: |
您最近一年使用:0次
解题方法
5 . 钛及其化合物在生产、生活中有着广泛的用途。回答下列问题:
(1)Ti(BH4)3是一种储氢材料。BH 中B原子的杂化轨道类型为
中B原子的杂化轨道类型为___ ;Ti、B、H元素的电负性由大到小排列顺序为_____ 。
(2)已知Ti3+易形成多种配合物,[TiCl(H2O)5]Cl2·H2O是其中的一种。
①1mol该配合物中含有_______ molσ键。
②Ti3+具有较强还原性的原因是___________ 。
(3)研究表明,TiO2通过氮掺杂反应可生成TiO2-xNy,能使TiO2对可见光具有活性,反应如图所示。
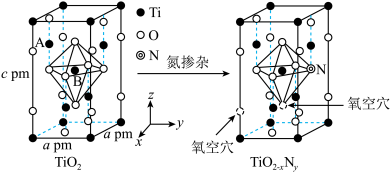
①上图TiO2晶胞中钛原子占据___________ 个氧原子围成的八面体空隙。
②已知所有的Ti-O键键长为rpm,B点原子的分数坐标为( ,
, ,
, ),则A点原子的分数坐标为(
),则A点原子的分数坐标为( ,0,
,0,___________ )。
③TiO2-xNy晶体中x=___________ 。
(1)Ti(BH4)3是一种储氢材料。BH
 中B原子的杂化轨道类型为
中B原子的杂化轨道类型为(2)已知Ti3+易形成多种配合物,[TiCl(H2O)5]Cl2·H2O是其中的一种。
①1mol该配合物中含有
②Ti3+具有较强还原性的原因是
(3)研究表明,TiO2通过氮掺杂反应可生成TiO2-xNy,能使TiO2对可见光具有活性,反应如图所示。

①上图TiO2晶胞中钛原子占据
②已知所有的Ti-O键键长为rpm,B点原子的分数坐标为(
 ,
, ,
, ),则A点原子的分数坐标为(
),则A点原子的分数坐标为( ,0,
,0,③TiO2-xNy晶体中x=
您最近一年使用:0次
名校
解题方法
6 . 中国科学家首次在月球上发现新矿物,将其命名为“嫦娥石”,“嫦娥石”中包含了Fe、Cu、Ti、Cr、Ni、Mo、N、O等多种元素。
(1)鉴定月球土壤的元素组成,可采用的方法是___________ 。
A.光谱分析 B.X-射线衍射分析
(2)在第二周期中,第一电离能比N高的主族元素是___________ 。氮原子的电子排布图表示的状态中,能量由低到高的顺序是___________ (填序号)。
A.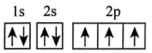 B.
B.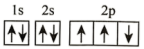
C.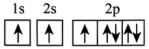 D.
D.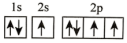
(3)已知有关氮、磷的单键和三键的键能( )如下表:
)如下表:
从能量角度看,氮以 、而白磷以
、而白磷以 (结构式可表示为
(结构式可表示为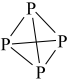 )形式存在的原因是
)形式存在的原因是___________ 。
(4)已知 分子的键角约为107°,而同主族磷的氢化物
分子的键角约为107°,而同主族磷的氢化物 分子的键角约为94°,试用价层电子对互斥模型解释
分子的键角约为94°,试用价层电子对互斥模型解释 的键角比
的键角比 的键角大的原因:
的键角大的原因:___________
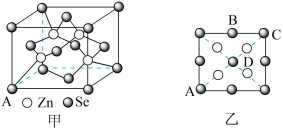
(5)硒化锌(ZnSe)是一种重要的半导体材料,其晶胞结构如图甲所示,已知晶胞边长为apm,乙图为甲图的俯视图,若原子坐标A为(0,0,0),B为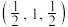 ,则D原子坐标为
,则D原子坐标为___________ ;若该晶胞密度为 ,则阿伏加德罗常数
,则阿伏加德罗常数 为
为_________________ 。
(1)鉴定月球土壤的元素组成,可采用的方法是
A.光谱分析 B.X-射线衍射分析
(2)在第二周期中,第一电离能比N高的主族元素是
A.
 B.
B.
C.
 D.
D.
(3)已知有关氮、磷的单键和三键的键能(
 )如下表:
)如下表:| N-N |  | P-P |  |
| 193 | 946 | 197 | 489 |
从能量角度看,氮以
 、而白磷以
、而白磷以 (结构式可表示为
(结构式可表示为 )形式存在的原因是
)形式存在的原因是(4)已知
 分子的键角约为107°,而同主族磷的氢化物
分子的键角约为107°,而同主族磷的氢化物 分子的键角约为94°,试用价层电子对互斥模型解释
分子的键角约为94°,试用价层电子对互斥模型解释 的键角比
的键角比 的键角大的原因:
的键角大的原因:(5)硒化锌(ZnSe)是一种重要的半导体材料,其晶胞结构如图甲所示,已知晶胞边长为apm,乙图为甲图的俯视图,若原子坐标A为(0,0,0),B为
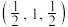 ,则D原子坐标为
,则D原子坐标为 ,则阿伏加德罗常数
,则阿伏加德罗常数 为
为
您最近一年使用:0次
7 . 锗(Ge)是典型的半导体元素,在电子、材料等领域应用广泛。回答下列问题:
(1)基态Ge原子的核外电子排布式为_______ ,最高能级电子的电子云轮廓形状为_______ 。
(2)比较下列锗卤化物的熔点和沸点,分析其变化的原因_______ 。
(3)光催化还原CO2制备CH4反应中,带状纳米Zn2GeO4是该反应的良好催化剂。Zn、Ge、O电负性由大至小的顺序是_______ 。
(4)Ge单晶具有金刚石型结构,其中Ge原子的杂化方式为_______ ,微粒之间存在的作用力是_______ 。
(5)晶胞有两个基本要素:
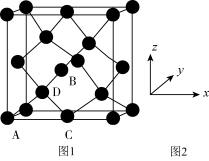
①原子坐标参数,表示晶胞内部各原子的相对位置,下图为Ge单晶的晶胞,其中原子坐标参数A为(0,0,0);B为( ,0,
,0, );C为(
);C为(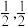 ,0)。则D原子的坐标参数为
,0)。则D原子的坐标参数为_______ 。
②晶胞参数,描述晶胞的大小和形状。已知Ge单晶的晶胞参数a=565.76pm,其密度为_______ g·cm-3(列出计算式即可)。
(1)基态Ge原子的核外电子排布式为
(2)比较下列锗卤化物的熔点和沸点,分析其变化的原因
| GeCl4 | GeBr4 | GeI4 | |
| 熔点/℃ | −49.5 | 26 | 146 |
| 沸点/℃ | 83.1 | 186 | 约400 |
(4)Ge单晶具有金刚石型结构,其中Ge原子的杂化方式为
(5)晶胞有两个基本要素:
①原子坐标参数,表示晶胞内部各原子的相对位置,下图为Ge单晶的晶胞,其中原子坐标参数A为(0,0,0);B为(
 ,0,
,0, );C为(
);C为(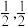 ,0)。则D原子的坐标参数为
,0)。则D原子的坐标参数为
②晶胞参数,描述晶胞的大小和形状。已知Ge单晶的晶胞参数a=565.76pm,其密度为
您最近一年使用:0次
解题方法
8 . 建盏由建阳坯土、天然矿物釉烧制,含有SiO2、Al2O3、Fe2O3、FeO、CaO、TiO2等化学成分。
(1)现代化学可利用_______ 特征谱线来鉴定建盏中的元素。
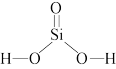
(2)建盏胎釉中含SiO2是硅酸的酸酐。硅酸结构式如图所示,硅原子的杂化方式_______ 。
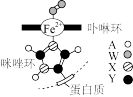
(3)Fe2+与蛋白质链上咪唑环通过配位键连接形成的物质结构如图所示。A、W、X、Y为短周期前10号主族元素。四种元素的电负性由大到小的顺序为_______ (用元素符号表示)。
(4)元素Fe在周期表中的位置为_______ ;其第三电离能(I3)为2957 KJ· mol-1、第四电离能(I4)为5290 KJ· mol-1,I4远大于I3的原因为_______ 。
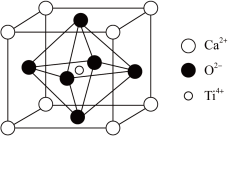
(5)建盏胎釉矿石中的钙钛矿晶胞如图所示,Ti4+处于6个O2-组成的_______ 空隙中,在钙钛矿晶胞结构的另一种表示中,Ti4+处于各顶角位置,则O2-处于_______ 位置(选填“面心”“体心”或“棱心”)。已知晶胞密度为 ρ g∙cm-3,则两个O2-离子间的最短距离为_______ nm(阿伏加德罗常数的值为NA,列出表达式)。
(1)现代化学可利用
(2)建盏胎釉中含SiO2是硅酸的酸酐。硅酸结构式如图所示,硅原子的杂化方式

(3)Fe2+与蛋白质链上咪唑环通过配位键连接形成的物质结构如图所示。A、W、X、Y为短周期前10号主族元素。四种元素的电负性由大到小的顺序为

(4)元素Fe在周期表中的位置为
(5)建盏胎釉矿石中的钙钛矿晶胞如图所示,Ti4+处于6个O2-组成的

您最近一年使用:0次
9 . 已知X、Y、Z、W是短周期元素。X元素原子的2p能级处于半充满状态;Y元素原子L电子层上s电子数和p电子数相等;Z元素的+2价阳离子的核外电子排布与氖原子相同;W元素原子的M电子层有1个未成对的p电子。下列说法一定正确的是
| A.含有X元素的化合物一定是共价化合物 |
| B.Y元素的电负性大于X元素的电负性 |
| C.W元素的单质能与NaOH溶液反应放出氢气 |
| D.X元素的单质与Z元素的单质在一定条件下能发生化合反应 |
您最近一年使用:0次
2020-05-14更新
|
612次组卷
|
11卷引用:福建省仙游第一中学2022-2023学年高二下学期第一次月考化学试题
福建省仙游第一中学2022-2023学年高二下学期第一次月考化学试题人教化学选修3第一章第二节课时5第1章 原子结构——B拓展区综合拓展(鲁科版选修3)江苏省南通中学2019-2020学年高二下学期期中考试化学试题新疆昌吉回族自治州第二中学2019-2020学年高二下学期期中考试化学试题(人教版2019)选择性必修2 第一章 原子结构与性质 C高考挑战区宁夏吴忠市吴忠中学2020-2021学年高二3月月考化学试题新疆乌鲁木齐市第八中学2021-2022学年高二下学期期中考试化学试题江苏省苏州市相城区陆慕高级中学2021-2022学年高二下学期第一次月考化学试题安徽省合肥市第一中学2022-2023学年高二下学期第一次质量检测化学试题河南省焦作市2022-2023学年第四中学高二下学期3月月考 化学试卷
10 . 科学家正在研究温室气体CH4和CO2的转化和利用。
(1)CH4和CO2所含的三种元素电负性从小到大的顺序为______ 。
(2)下列关于CH4和CO2的说法正确的是______ (填序号)。
a.固态CO2属于分子晶体
b. CH4分子中含有极性共价键,是极性分子
c.因为碳氢键键能小于碳氧键,所以CH4熔点低于CO2
d. CH4和CO2分子中碳原子的杂化类型分别是sp3和sp
(3)在Ni基催化剂作用下,CH4和CO2反应可获得化工原料CO和H2。
①基态Ni原子的电子排布式为____________ ,Ni该元素位于元素周期表的第___ 族。
②Ni能与CO形成正四面体形的配合物Ni(CO)4,1mol Ni(CO)4中含有_____ molσ键。
(4)一定条件下,CH4和CO2都能与H2O形成笼状结构(如图所示)的水合物晶体,其相关参数见下表.CH4与H2O形成的水合物俗称“可燃冰”。


①“可燃冰”中分子间存在的2种作用力是______ 。
②为开采深海海底的“可燃冰”,有科学家提出用CO2置换CH4的设想.已知图中笼状结构的空腔直径为0.586nm,根据上述图表,从物质结构及性质的角度分析,该设想的依据是___________________________ 。
(1)CH4和CO2所含的三种元素电负性从小到大的顺序为
(2)下列关于CH4和CO2的说法正确的是
a.固态CO2属于分子晶体
b. CH4分子中含有极性共价键,是极性分子
c.因为碳氢键键能小于碳氧键,所以CH4熔点低于CO2
d. CH4和CO2分子中碳原子的杂化类型分别是sp3和sp
(3)在Ni基催化剂作用下,CH4和CO2反应可获得化工原料CO和H2。
①基态Ni原子的电子排布式为
②Ni能与CO形成正四面体形的配合物Ni(CO)4,1mol Ni(CO)4中含有
(4)一定条件下,CH4和CO2都能与H2O形成笼状结构(如图所示)的水合物晶体,其相关参数见下表.CH4与H2O形成的水合物俗称“可燃冰”。


①“可燃冰”中分子间存在的2种作用力是
②为开采深海海底的“可燃冰”,有科学家提出用CO2置换CH4的设想.已知图中笼状结构的空腔直径为0.586nm,根据上述图表,从物质结构及性质的角度分析,该设想的依据是
您最近一年使用:0次
2016-12-09更新
|
1726次组卷
|
3卷引用:2015年全国普通高等学校招生统一考试化学(福建卷)



