1 . 钛硅分子筛是一种新型固体催化剂,可催化合成重要有机合成活性试剂甲乙酮肟(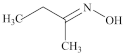 )。回答下列问题:
)。回答下列问题:
(1)基态硅原子的核外电子空间运动状态有___________ 种。
(2)甲乙酮肟中同周期三种元素电负性由大到小的顺序为___________ ,氮原子的杂化方式为___________ ,C=N与C-C键夹角___________ (填“<”“>”或“=”)C=N与N-O键夹角。
(3) 和
和 均是制备钛硅分子筛的重要中间体。
均是制备钛硅分子筛的重要中间体。
① 与光气
与光气 反应可用于制取四氯化钛。
反应可用于制取四氯化钛。 中σ键和π键的数目比为
中σ键和π键的数目比为___________ ,其空间构型为___________ 。
② 与金属
与金属 在高温条件下可反应生成
在高温条件下可反应生成 ,
, 中
中 极易被氧化,还原性很强。试解释
极易被氧化,还原性很强。试解释 还原性强的原因
还原性强的原因___________ 。
 )。回答下列问题:
)。回答下列问题:(1)基态硅原子的核外电子空间运动状态有
(2)甲乙酮肟中同周期三种元素电负性由大到小的顺序为
(3)
 和
和 均是制备钛硅分子筛的重要中间体。
均是制备钛硅分子筛的重要中间体。①
 与光气
与光气 反应可用于制取四氯化钛。
反应可用于制取四氯化钛。 中σ键和π键的数目比为
中σ键和π键的数目比为②
 与金属
与金属 在高温条件下可反应生成
在高温条件下可反应生成 ,
, 中
中 极易被氧化,还原性很强。试解释
极易被氧化,还原性很强。试解释 还原性强的原因
还原性强的原因
您最近一年使用:0次
名校
解题方法
2 . 运用物质结构与性质的相关知识,回答下列问题:
(1) 分子中,与
分子中,与 原子相连的
原子相连的 呈正电性
呈正电性 ,与
,与 原子相连的
原子相连的 呈负电性
呈负电性 电负性大小顺序是
电负性大小顺序是_______ 。基态 原子中能量最高的电子所在的原子轨道的电子云在空间上有
原子中能量最高的电子所在的原子轨道的电子云在空间上有_____ 个伸展方向,原子轨道呈______ 形。
(2) 的价层电子排布式为
的价层电子排布式为 在周期表中的位置为
在周期表中的位置为________ , 价电子轨道表示式为
价电子轨道表示式为________ 。
(3) 是离子晶体,其晶格能可通过Born-Haber循环计算得到。
是离子晶体,其晶格能可通过Born-Haber循环计算得到。
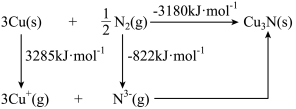
通过图中数据________ (填“能”或“不能”)计算出 原子的第一电离能,
原子的第一电离能, 的晶格能为
的晶格能为________  。
。
(4)GaAs的晶胞结构如图甲。将Mn掺杂到GaAs的晶体中得到稀磁性半导体材料(图乙)。
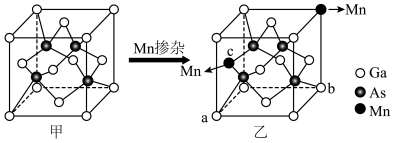
①GaAs晶胞中距离Ga原子最近As原子的个数为________ 。
②掺杂 之后,晶体中
之后,晶体中 的原子个数比为
的原子个数比为________ (化为最简整数比)。
(1)
 分子中,与
分子中,与 原子相连的
原子相连的 呈正电性
呈正电性 ,与
,与 原子相连的
原子相连的 呈负电性
呈负电性 电负性大小顺序是
电负性大小顺序是 原子中能量最高的电子所在的原子轨道的电子云在空间上有
原子中能量最高的电子所在的原子轨道的电子云在空间上有(2)
 的价层电子排布式为
的价层电子排布式为 在周期表中的位置为
在周期表中的位置为 价电子轨道表示式为
价电子轨道表示式为(3)
 是离子晶体,其晶格能可通过Born-Haber循环计算得到。
是离子晶体,其晶格能可通过Born-Haber循环计算得到。
通过图中数据
 原子的第一电离能,
原子的第一电离能, 的晶格能为
的晶格能为 。
。(4)GaAs的晶胞结构如图甲。将Mn掺杂到GaAs的晶体中得到稀磁性半导体材料(图乙)。

①GaAs晶胞中距离Ga原子最近As原子的个数为
②掺杂
 之后,晶体中
之后,晶体中 的原子个数比为
的原子个数比为
您最近一年使用:0次
名校
解题方法
3 . 据《科学》报道,中国科学家首次实现超导体(Bi2Te3/NBSe2)中分段费米面。回答下列问题:
(1)Bi与P位于同主族,基态P原子的价层电子排布式为___________ 。基态Se原子核外电子云轮廓图呈哑铃形的能级上共有___________ 个电子。
(2)二氯二茂铌的组成为(C5H5)2NbCl2.环戊二烯阴离子( )的平面结构简式如图所示:
)的平面结构简式如图所示:
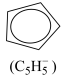
①C、H、Cl的电负性由大到小的顺序为___________ 。
② 中C原子的杂化类型是
中C原子的杂化类型是___________ 。
③已知分子中的大π键可以用 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,则
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,则 中大π键可以表示为
中大π键可以表示为___________ 。
(3) 的空间构型为
的空间构型为___________ 。
(4)四氟化铌(NbF4)的熔点为72℃,它的晶体类型为___________ 。
(1)Bi与P位于同主族,基态P原子的价层电子排布式为
(2)二氯二茂铌的组成为(C5H5)2NbCl2.环戊二烯阴离子(
 )的平面结构简式如图所示:
)的平面结构简式如图所示:
①C、H、Cl的电负性由大到小的顺序为
②
 中C原子的杂化类型是
中C原子的杂化类型是③已知分子中的大π键可以用
 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,则
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,则 中大π键可以表示为
中大π键可以表示为(3)
 的空间构型为
的空间构型为(4)四氟化铌(NbF4)的熔点为72℃,它的晶体类型为
您最近一年使用:0次
2022-03-25更新
|
233次组卷
|
2卷引用:福建省漳州市第三中学2022-2023学年高二下学期3月质量检测化学试题
4 . Ⅰ.已知A、B、C、D、E、F、G、H8种短周期元素的原子半径和某些化合价如下表所示:
(1)将D、F两种元素的元素符号填入如图所示元素周期表中的相应位置_______ 。
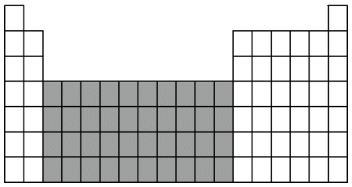
(2)上图中阴影部分所示区域的元素称为_______ 元素,下列元素属于该区域的是_______ 。
A.Ba B.Fe C.Br D.Rb
Ⅱ.现有A、B、C、D、E、F、G、H元素,均为前四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答有关问题。
(3)G2D2的电子式为_______ 。(D、G为字母代号,请将字母代号用元素符号表示,下同)。
(4)某同学推断E元素基态原子的核外电子轨道表示式为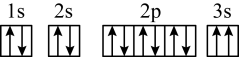 。该同学所画的电子轨道表示式违背了
。该同学所画的电子轨道表示式违背了_______ ,该元素的I3远远大于I2,其原因是_______ 。
(5)D、E、F三种元素的简单离子半径由大到小的顺序是_______ 。
(6)H位于元素周期表中_______ 区(按电子排布分区),其基态原子的价电子排布式为_______ 。与元素H位于同一周期,其原子基态时未成对电子数在同周期中最多的元素是_______ (填元素符号)。
(7)写出一种由A、B、C、D四种元素组成离子化合物_______ 。
(8)GeO2不能形成类似CO2分子中的π键,原因是_______ 。
| 元素 | A | B | C | D | E | F | G | H |
| 化合价 | -2 | +5、-3 | +4、-4 | +6、-2 | +2 | +1 | +7、-1 | +4、-4 |
| 原子半径/nm | 0.073 | 0.075 | 0 077 077 | 0.102 | 0 130 130 | 0.154 | 0 099 099 | 0.111 |

(2)上图中阴影部分所示区域的元素称为
A.Ba B.Fe C.Br D.Rb
Ⅱ.现有A、B、C、D、E、F、G、H元素,均为前四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答有关问题。
| A元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B元素是形成化合物种类最多的元素 |
| C元素基态原子的核外p能级电子数比s能级电子数少1 |
| D元素基态原子的核外p轨道中有两个未成对电子 |
| E元素的气态基态原子的第一至第四电离能分别是I1=738kJ/mol,I2=1451kJ/mol,I3=7733kJ/mol,I4=10540kJ/mol |
| F元素的主族序数与周期数的差为4 |
| G元素是前四周期中电负性最小的元素 |
| H元素位于元素周期表中的第8列 |
(4)某同学推断E元素基态原子的核外电子轨道表示式为
 。该同学所画的电子轨道表示式违背了
。该同学所画的电子轨道表示式违背了(5)D、E、F三种元素的简单离子半径由大到小的顺序是
(6)H位于元素周期表中
(7)写出一种由A、B、C、D四种元素组成离子化合物
(8)GeO2不能形成类似CO2分子中的π键,原因是
您最近一年使用:0次
名校
解题方法
5 . 据媒体报道,法国一家公司Tiamat日前研发出比当前广泛使用的锂电池成本更低、寿命更长、充电速度更快的钠离子电池,预计从2020年开始实现工业生产。该电池的负极材料为Na2Co2TeO6(制备原料为Na2CO3、Co3O4和TeO2),电解液为NaClO4的碳酸丙烯酯溶液。回答下列问题:
(1)Co 属于元素周期表中___________ 区元素,其基态原子的价电子排布式为___________ 。
(2)基态Na原子中,核外电子占据的原子轨道总数为___________ ,最高能层电子云轮廓图形状为___________
(3)结合题中信息判断:C、O、Cl的电负性由小到大的顺序为___________ (用元素符号表示)。
(4) 的几何构型为
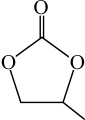
的几何构型为___________ ;碳酸丙烯酯的结构简式如图所示,则其中碳原子的杂化轨道类型为___________ ,1mol碳酸丙烯酯中 键的数目为
键的数目为___________ 。
(5)[Co(H2O)6]3+的几何构型为正八面体形,配体是___________ ,该配离子包含的作用力为___________ (填选项字母)。
A.离子键 B.金属键 C.配位键 D.氢键 E.极性键
(1)Co 属于元素周期表中
(2)基态Na原子中,核外电子占据的原子轨道总数为
(3)结合题中信息判断:C、O、Cl的电负性由小到大的顺序为
(4)
 的几何构型为
的几何构型为 键的数目为
键的数目为
(5)[Co(H2O)6]3+的几何构型为正八面体形,配体是
A.离子键 B.金属键 C.配位键 D.氢键 E.极性键
您最近一年使用:0次
名校
6 . 下列比较中,正确的是
| A.第一电离能:Na<Mg<Al | B.电负性:Cl>S>As |
| C.原子半径:O>F>Na | D.最高正化合价:F>S>N |
您最近一年使用:0次
2024-03-01更新
|
153次组卷
|
3卷引用:福建省漳州市华安县第一中学2023-2024学年高二下学期3月月考化学试题
名校
解题方法
7 . 2022年12月,首架国产大飞机C919正式交付,国之重器,世界瞩目。铼( )是生产飞机发动机叶片必不可少的材料。X、Y、Z、Q、W是原子序数依次增大且位于不同主族的短周期元素,其中X、Y、Z三种元素可与铼元素组成一种化合物(结构如图),该化合物与X的单质反应可得到铼。Q是地壳中含量最丰富的金属元素,Z与W形成的化合物为共价晶体。下列说法正确的是
)是生产飞机发动机叶片必不可少的材料。X、Y、Z、Q、W是原子序数依次增大且位于不同主族的短周期元素,其中X、Y、Z三种元素可与铼元素组成一种化合物(结构如图),该化合物与X的单质反应可得到铼。Q是地壳中含量最丰富的金属元素,Z与W形成的化合物为共价晶体。下列说法正确的是
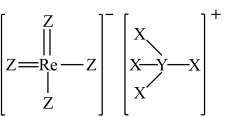
 )是生产飞机发动机叶片必不可少的材料。X、Y、Z、Q、W是原子序数依次增大且位于不同主族的短周期元素,其中X、Y、Z三种元素可与铼元素组成一种化合物(结构如图),该化合物与X的单质反应可得到铼。Q是地壳中含量最丰富的金属元素,Z与W形成的化合物为共价晶体。下列说法正确的是
)是生产飞机发动机叶片必不可少的材料。X、Y、Z、Q、W是原子序数依次增大且位于不同主族的短周期元素,其中X、Y、Z三种元素可与铼元素组成一种化合物(结构如图),该化合物与X的单质反应可得到铼。Q是地壳中含量最丰富的金属元素,Z与W形成的化合物为共价晶体。下列说法正确的是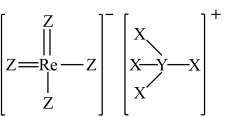
| A.电负性:Z>Y>Q>W |
| B.图中的阳离子存在三个共价键和一个配位键,四个键的性质不同 |
| C.熔点:W晶体小于W、Y形成的晶体 |
| D.Q的氧化物可以和氨水反应 |
您最近一年使用:0次
名校
8 . 碳、硫、氧、氮是中学常见元素,下列说法不正确的是
A. 、 、 、 、 都是直线形分子 都是直线形分子 |
B. 、 、 、 、 的键角依次减小 的键角依次减小 |
C. 、 、 分子的中心原子都是 分子的中心原子都是 化 化 |
| D.C、N、F元素的电负性依次增大 |
您最近一年使用:0次
2023-06-08更新
|
155次组卷
|
5卷引用:福建省三明市四地四校2021-2022学年高二下学期期中联考化学试题
名校
9 . 纯碱( )是重要的基础化工原料,我国化学家侯德榜在1943年提出了著名侯氏制碱法。原理为:将
)是重要的基础化工原料,我国化学家侯德榜在1943年提出了著名侯氏制碱法。原理为:将 通入氨化的饱和食盐水中析出
通入氨化的饱和食盐水中析出 晶体,将得到的
晶体,将得到的 晶体加热分解生成
晶体加热分解生成 。下列有关
。下列有关 、
、 、
、 和
和 的说法正确的是
的说法正确的是
 )是重要的基础化工原料,我国化学家侯德榜在1943年提出了著名侯氏制碱法。原理为:将
)是重要的基础化工原料,我国化学家侯德榜在1943年提出了著名侯氏制碱法。原理为:将 通入氨化的饱和食盐水中析出
通入氨化的饱和食盐水中析出 晶体,将得到的
晶体,将得到的 晶体加热分解生成
晶体加热分解生成 。下列有关
。下列有关 、
、 、
、 和
和 的说法正确的是
的说法正确的是A.电负性: | B.沸点: |
C.键角: | D. 为极性分子,CO2为非极性分子 为极性分子,CO2为非极性分子 |
您最近一年使用:0次
2022-07-07更新
|
302次组卷
|
3卷引用:福建省福州屏东中学2023-2024学年高二下学期期中考试化学试题
名校
10 . Zn2+、三乙撑二胺和对苯二甲酸根离子可形成晶体M,其晶胞示意图如图。
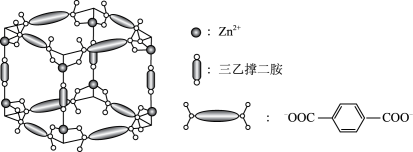
(1)Zn2+的价层电子排布式是_____ 。
(2)C、N、O的电负性从大到小 的顺序是_____ ;C、N、O的第一电离能从大到小 的顺序是_____ 。
(3)三乙撑二胺(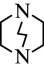 )与
)与 能形成配位键的原因是
能形成配位键的原因是_____ 。
(4)下列事实可用“水分子间存在氢键”解释的是_____ (填字母序号 )。
a.常压下,4℃时水的密度最大
b.水的沸点比硫化氢的沸点高160℃
c.水的热稳定性比硫化氢强
(5)对苯二甲酸(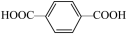 )中苯环上的碳原子的杂化方式为
)中苯环上的碳原子的杂化方式为_____ ,羧基上碳原子的杂化方式为____ ,对苯二甲酸中最多有_____ 个原子共平面。

(1)Zn2+的价层电子排布式是
(2)C、N、O的电负性
(3)三乙撑二胺(
 )与
)与 能形成配位键的原因是
能形成配位键的原因是(4)下列事实可用“水分子间存在氢键”解释的是
a.常压下,4℃时水的密度最大
b.水的沸点比硫化氢的沸点高160℃
c.水的热稳定性比硫化氢强
(5)对苯二甲酸(
 )中苯环上的碳原子的杂化方式为
)中苯环上的碳原子的杂化方式为
您最近一年使用:0次



