1 . 下表是元素周期表前四周期的一部分,X、Y、Z、R、Q、W、J是7种元素的代号。回答下列问题时,涉及元素书写的请用相应的元素符号。

(1)J基态原子的核外电子排布式为________ 。基态Q2+中未成对电子数为________ ;R和Y的简单离子与Na+半径大小顺序为________ 。
(2)X、Y、Z三种元素电负性由大到小的排序是________ ;X与Y的第一电离能:X________ (填“>”“<”或“=”)Y,其理由是________ 。
(3)检验某溶液中是否含有Q3+的方法是_____________________________ 。
(4)已知WX3是一种引爆剂,受撞击时分解为两种单质,则其化学方程式为________________ 。

(1)J基态原子的核外电子排布式为
(2)X、Y、Z三种元素电负性由大到小的排序是
(3)检验某溶液中是否含有Q3+的方法是
(4)已知WX3是一种引爆剂,受撞击时分解为两种单质,则其化学方程式为
您最近一年使用:0次
2018-02-11更新
|
153次组卷
|
2卷引用:河北省邢台市第二中学2017-2018学年高二化学选修三课时训练:1.2 原子结构与元素的性质 第2课时
名校
解题方法
2 . 四种元素X、Y、Z、W位于元素周期表的前四周期,已知它们的核电荷数依次增加,且核电荷数之和为51;Y原子的L层p轨道中有2个电子;Z与Y原子的价层电子数相同;W原子的L层电子数与最外层电子数之比为4∶1,其d轨道中的电子数与最外层电子数之比为5∶1。
(1)Y、Z可分别与X形成只含一个中心原子的共价化合物a、b,它们的分子式分别是________ 、________ ;杂化轨道分别是________ 、________ ;a分子的立体结构是________ 。
(2)Y的最高价氧化物和Z的最高价氧化物的晶体类型分别是________ 晶体、________ 晶体。
(3)Y与Z比较,电负性较大的是________ ,W2+离子的核外电子排布式是________ 。
(1)Y、Z可分别与X形成只含一个中心原子的共价化合物a、b,它们的分子式分别是
(2)Y的最高价氧化物和Z的最高价氧化物的晶体类型分别是
(3)Y与Z比较,电负性较大的是
您最近一年使用:0次
名校
3 . 下列各元素电负性大小顺序正确的是( )
| A.K>Na>Li | B.F>O>S | C.As>P>N | D.C>N>O |
您最近一年使用:0次
名校
解题方法
4 . 砷的一些化合物常用作半导体、除草剂、杀鼠药等。回答下列问题:
(1)基态As原子的核外电子排布式为[Ar]__________ ,有___________ 个未成对电子。
(2)镓氮砷合金材料的太阳能电池效率达40%。Ga、N、As电负性由大至小的顺序是_____________ 。
(3)As4O6的分子结构如图所示,其中As原子的杂化方式为____________ ,1mol 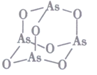 As4O6含有σ键的物质的量为
As4O6含有σ键的物质的量为________ mol。
(4)晶胞有两个基本要素:
①原子坐标参数,表示晶胞内部各原子的相对位置,LiZnAs基稀磁半导体的晶胞如图所示,其中原子
坐标参数A处Li为(0,0, );B处As为(
);B处As为( ,
, ,
, );C处Li的坐标参数为
);C处Li的坐标参数为_____________ 。
②晶胞参数,描述晶胞的大小和形状,已知LiZnAs单晶的晶胞参数α=594 pm,NA表示阿伏伽德罗常数的数值,其密度为____________ g·cm-3(列出计算式即可)。
(1)基态As原子的核外电子排布式为[Ar]
(2)镓氮砷合金材料的太阳能电池效率达40%。Ga、N、As电负性由大至小的顺序是
(3)As4O6的分子结构如图所示,其中As原子的杂化方式为
 As4O6含有σ键的物质的量为
As4O6含有σ键的物质的量为(4)晶胞有两个基本要素:
①原子坐标参数,表示晶胞内部各原子的相对位置,LiZnAs基稀磁半导体的晶胞如图所示,其中原子
坐标参数A处Li为(0,0,
 );B处As为(
);B处As为( ,
, ,
, );C处Li的坐标参数为
);C处Li的坐标参数为②晶胞参数,描述晶胞的大小和形状,已知LiZnAs单晶的晶胞参数α=594 pm,NA表示阿伏伽德罗常数的数值,其密度为
您最近一年使用:0次
名校
5 . 利用电负性数值可以预测
| A.分子的极性 | B.分子的对称性 |
| C.分子的空间构型 | D.化学键的极性 |
您最近一年使用:0次
2016-12-09更新
|
180次组卷
|
5卷引用:河北省唐山市开滦第二中学2017-2018学年高二4月月考化学试题
名校
解题方法
6 . 化合物XYZ4ME4可作肥料,所含的5种元素位于主族,在每个短周期均有分布,仅有Y和M同族。Y的基态原子价层p轨道半充满,X的基态原子价层电子排布式为nsn-1,X与M同周期,E在地壳中含量最多。下列说法正确的是
| A.元素电负性:E>Y>Z | B.1mol M中含有共价键数目为4NA |
| C.半径:X2+>E2- | D.YZ3和YE 的空间结构均为三角锥形 的空间结构均为三角锥形 |
您最近一年使用:0次
7 . 下列说法正确的是
A. 的空间结构与其VSEPR模型相同 的空间结构与其VSEPR模型相同 |
B.氢键 中的三原子均在一条直线上 中的三原子均在一条直线上 |
| C.基态O原子核外电子的运动状态有8种 |
| D.第一电离能和电负性的大小可分别作为判断元素金属性和非金属性强弱的依据 |
您最近一年使用:0次
8 . 在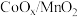 催化下醇的氧化氰化反应如图所示。下列叙述正确的是
催化下醇的氧化氰化反应如图所示。下列叙述正确的是
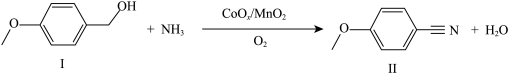
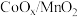 催化下醇的氧化氰化反应如图所示。下列叙述正确的是
催化下醇的氧化氰化反应如图所示。下列叙述正确的是
| A.熔点:Ⅰ>Ⅱ | B.Ⅰ所属类别为酚类 |
| C.Ⅰ和Ⅱ分子中σ键数目相同 | D.Ⅱ含有的元素中 的电负性最大 的电负性最大 |
您最近一年使用:0次



