名校
1 . F、Cl、Br元素的某种性质Y随核电荷数的变化趋势如图所示,则坐标轴Y不可以代表的是
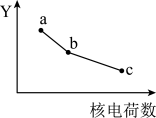

| A.元素的电负性 | B.元素的第一电离能 |
| C.氢化物的稳定性 | D.简单离子的还原性 |
您最近一年使用:0次
解题方法
2 . 硅与碳同主族,是构成地壳的主要元素之一,下列说法正确的是
| A.键能:Si-Si<C-C |
B. 和 和 中C、Si化合价均为-4价 中C、Si化合价均为-4价 |
| C.硅酸盐与碳酸盐中Si、C原子的杂化方式相同 |
D.相比较碳原子,硅与硅之间更易形成 键 键 |
您最近一年使用:0次
2023-04-29更新
|
216次组卷
|
2卷引用:河北省部分学校2023届高三下学期大数据应用调研联合测评化学试题
3 . 下列有关性质的比较错误的是
| A.热稳定性:H2S<HCl | B.电负性:Cl>Br |
| C.第一电离能:S<P | D.离子半径:K+>Cl- |
您最近一年使用:0次
名校
4 . 下列各组元素中,电负性依次减小的是
| A.F、N、O | B.Cl、C、F | C.As、N、H | D.Cl、S、As |
您最近一年使用:0次
2022-01-21更新
|
374次组卷
|
6卷引用:河北省石家庄市元氏县第四中学2021-2022学年高二下学期6月月考化学试题
5 . 第四周期的元素形成的化合物在生产生活中有着重要的用途。
(1)镍铬钢抗腐蚀性能强,基态铬原子的价电子排布式为___________ ,按照电子排布式,镍元素在周期表中位于___________ 区。
(2)“玉兔二号”月球车通过砷化镓(GaAs)太阳能电池提供能量进行工作。基态砷原子的电子占据最高能级的电子云轮廓图为___________ 形。砷的电负性比镓___________ (填“大”或“小”)。
(3)基态Fe3+、Fe2+离子中未成对的电子数之比为___________ 。
(1)镍铬钢抗腐蚀性能强,基态铬原子的价电子排布式为
(2)“玉兔二号”月球车通过砷化镓(GaAs)太阳能电池提供能量进行工作。基态砷原子的电子占据最高能级的电子云轮廓图为
(3)基态Fe3+、Fe2+离子中未成对的电子数之比为
您最近一年使用:0次
2023-11-01更新
|
143次组卷
|
2卷引用:河北省衡水市安平中学2023-2024学年高二下学期开学考试化学试题
名校
解题方法
6 . 下列叙述正确的是
| A.铬原子的电子排布式:ls22s22p63s23p63d44s2 |
| B.Na、Mg、Al的第一电离能逐渐增大 |
C.碳原子的电子排布图: |
| D.N、O、F的电负性逐渐增大 |
您最近一年使用:0次
2019-06-28更新
|
849次组卷
|
15卷引用:【全国百强校】河北省武邑中学2017-2018学年高二下学期期中考试化学试题
【全国百强校】河北省武邑中学2017-2018学年高二下学期期中考试化学试题福建省泉州市泉港区第一中学2017-2018学年高二下学期第一次(4月)月考化学试题黑龙江省牡丹江市第三高级中学2018-2019学年高二下学期期中考试化学试题黑龙江省齐齐哈尔市第八中学2018-2019学年高二下学期期中考试化学试题人教化学选修3第一章第二节课时5山东省济南外国语学校2019-2020学年高二下学期3月份“空中课堂”阶段性测试化学试题四川省越西中学2019-2020学年高二5月月考化学试题辽宁省锦州市黑山县黑山中学2019-2020学年高二下学期线上教学检测化学试题安徽省亳州市涡阳县第九中学2019-2020学年高二7月月考化学试题河南省驻马店市2018-2019学年高二上学期期末考试化学试题江苏省镇江市吕叔湘中学2019-2020学年高二下学期4月诊断考试化学试题福建省南安市柳城中学2020-2021学年高二下学期期中考试化学试题黑龙江省黑河市第九中学2022-2023学年高三上学期摸底考试化学试题新疆疏勒县实验学校2021-2022学年高二下学期期中考试化学试题黑龙江省大庆市大庆中学2022-2023学年高三第二次模拟考试化学试题
名校
7 . 甲醇(CH3OH)空气氧化法是生产工业甲醛(HCHO)的常用方法。发生的反应为2CH3OH+O2 2
2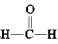 +2H2O
+2H2O
(1)C、H、O 三种元素的电负性由大到小的顺序为___________ 。
(2)H2O的中心原子上的孤电子对数为___________ 。
(3)HCHO分子内σ键与π键个数之比为___________ ,HCHO的空间结构为___________ 。
(4)CH3OH和HCHO分子中碳原子的杂化轨道类型分别为___________ 和___________ 。
(5)甲醇氧化生成HCHO时,会产生CO、CO2、CH3OCH3等副产物。相同条件下,CO2的沸点比O2的高,主要原因为___________ 。
(6)工业上利用甲醛易溶于水的性质吸收产品,解释甲醛易溶于水的原因:___________ 。
 2
2 +2H2O
+2H2O(1)C、H、O 三种元素的电负性由大到小的顺序为
(2)H2O的中心原子上的孤电子对数为
(3)HCHO分子内σ键与π键个数之比为
(4)CH3OH和HCHO分子中碳原子的杂化轨道类型分别为
(5)甲醇氧化生成HCHO时,会产生CO、CO2、CH3OCH3等副产物。相同条件下,CO2的沸点比O2的高,主要原因为
(6)工业上利用甲醛易溶于水的性质吸收产品,解释甲醛易溶于水的原因:
您最近一年使用:0次
2021-07-11更新
|
458次组卷
|
5卷引用:河北省张家口市张北县第一中学2022-2023学年高二下学期4月月考化学试题
名校
解题方法
8 . 由于铁氮化合物具有非常优异的磁性能、机械性能和耐腐蚀性,受到研究人员的广泛关注。γˊ−Fe4N是一种性能优异的铁氮化合物,其可由氨气与羰基铁粉[Fe(CO)5]反应得到。
(1)Fe变为Fe2+时是失去___________ 轨道电子,Fe3+价层电子排布图为___________ 。
(2)氨气中N的杂化类型是___________ ,NH3中H−N−H的键角比NH4+中H−N−H的键角___________ (填“大”或“小”),理由是___________ 。
(3) 与CO中均存在化学键的类型有
与CO中均存在化学键的类型有___________ (填标号)。
A.离子键 B.氢键 C.配位键 D.共价键 E.金属键
(4)羰基铁粉[Fe(CO)5]中铁元素的配位数是___________ ,配位原子为___________ 。
(5)氨气与羰基铁粉的反应中涉及元素电负性由大到小的顺序为___________ 。
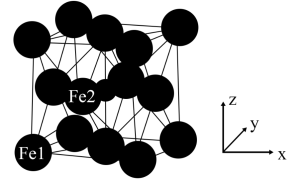
(6)γ−Fe4N的晶胞如图所示,设晶胞中Fe1点的原子坐标为(0,0,0),N点的原子坐标为( ,
, ,
, ),则Fe2点的原子坐标为
),则Fe2点的原子坐标为___________ 。已知该晶体的密度为dg/cm3,阿伏加德罗常数的值为NA,则晶胞参数a为___________ nm(用含d和NA的代数式表示)。
(1)Fe变为Fe2+时是失去
(2)氨气中N的杂化类型是
(3)
 与CO中均存在化学键的类型有
与CO中均存在化学键的类型有A.离子键 B.氢键 C.配位键 D.共价键 E.金属键
(4)羰基铁粉[Fe(CO)5]中铁元素的配位数是
(5)氨气与羰基铁粉的反应中涉及元素电负性由大到小的顺序为
(6)γ−Fe4N的晶胞如图所示,设晶胞中Fe1点的原子坐标为(0,0,0),N点的原子坐标为(
 ,
, ,
, ),则Fe2点的原子坐标为
),则Fe2点的原子坐标为
您最近一年使用:0次
2021-12-31更新
|
289次组卷
|
5卷引用:石家庄示范性高中2022届高三上学期调研考试化学试题
名校
解题方法
9 . 对 Na 、Mg 、Al 的有关性质的叙述不正确的是
| A.第一电离能:Na<Mg<Al |
| B.电负性:Na<Mg<Al |
| C.还原性:Na>Mg>Al |
| D.最高价氧化物的水化物碱性:NaOH>Mg(OH)2>Al(OH)3 |
您最近一年使用:0次
2022-11-02更新
|
142次组卷
|
2卷引用:河北省保定高碑店市崇德实验中学2022-2023学年高三上学期10月月考化学试题
名校
10 . 现有三种元素基态原子的电子排布式:①1s22s22p63s23p4;②1s22s22p63s23p3;③1s22s22p5。下列有关比较正确的是
| A.第一电离能:③>②>① | B.原子半径:①>②>③ |
| C.电负性:③>①>② | D.最高正化合价:③>②>① |
您最近一年使用:0次



