1 . 下列关于物质结构与性质的叙述错误的是
A. 键的极性大于 键的极性大于 ,因此 ,因此 分子的极性大于 分子的极性大于 |
B. 的电负性大于 的电负性大于 ,因此 ,因此 的键角小于 的键角小于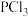 |
C. 键的键能大于 键的键能大于 ,因此 ,因此 的稳定性高于 的稳定性高于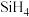 |
D.甲基是推电子基团,羟基是吸电子基团,因此 的碱性强于 的碱性强于 |
您最近一年使用:0次
2 . 高纯硅可以采用下列方法制备.下列说法正确的是

| A.晶体Si导电性介于导体和绝缘体之间,常用于制造光导纤维 |
B.可以通过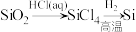 实现粗硅的制备 实现粗硅的制备 |
C.步骤①的反应为 ,不能说明碳的非金属性比硅强 ,不能说明碳的非金属性比硅强 |
D.已知电负性: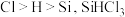 遇水会剧烈反应,化学方程式为 遇水会剧烈反应,化学方程式为 |
您最近一年使用:0次
2024-03-01更新
|
373次组卷
|
2卷引用:山东省部分学校2023-2024学年高三下学期2月份大联考(开学)质量检测化学试题
3 . 铬元素是哺乳类代谢过程中必须的微量元素,目前六氟代乙酰丙酮铬(Ⅲ)螯合物(其结构如图)的检出极限已达到 。回答下列问题:
。回答下列问题:
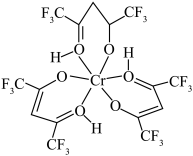
(1)基态铬原子的价电子排布式为___________ ,H、C、O、F的电负性由大到小的顺序为___________ 。
(2)与 具有相同未成对电子数的同周期基态原子的元素有
具有相同未成对电子数的同周期基态原子的元素有___________ 种,其中原子序数最大的元素在周期表中的位置是___________ 。
(3)六氟代乙酰丙酮铬(Ⅲ)螯合物中含有的化学键有___________ 。
a.极性共价键 b.非极性共价键 c.离子键 d.配位键
(4)六氟代乙酰丙酮(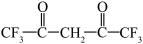 )中
)中 键有
键有___________ 个。
(5)分子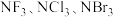 中键角由小到大的顺序是
中键角由小到大的顺序是___________ ,其原因是___________ 。
 。回答下列问题:
。回答下列问题:
(1)基态铬原子的价电子排布式为
(2)与
 具有相同未成对电子数的同周期基态原子的元素有
具有相同未成对电子数的同周期基态原子的元素有(3)六氟代乙酰丙酮铬(Ⅲ)螯合物中含有的化学键有
a.极性共价键 b.非极性共价键 c.离子键 d.配位键
(4)六氟代乙酰丙酮(
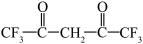 )中
)中 键有
键有(5)分子
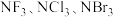 中键角由小到大的顺序是
中键角由小到大的顺序是
您最近一年使用:0次
解题方法
4 . 填空。
(1)N、Al、Si、Zn四种元素中,有一种元素的电离能数据如下,则该元素是___________ (填写元素符号)。
(2)请解释 的热稳定性高于
的热稳定性高于 的原因
的原因___________ 。
(3)基态氮原子核外电子的空间运动状态有___________ 种, 的键角约为107°,推测
的键角约为107°,推测 的键角
的键角___________ 107°(填“>,<或=”)。
(4)基态硅原子价层电子轨道表示式为___________ ; 与N-甲基咪唑(分子式为:
与N-甲基咪唑(分子式为: ,结构为
,结构为 )反应可以得到一种功能性螯合物。则:C、N、H三种非金属元素的电负性由大到小的顺序是
)反应可以得到一种功能性螯合物。则:C、N、H三种非金属元素的电负性由大到小的顺序是___________ ,1个N-甲基咪唑分子中含有___________ 个 键。
键。
(5)已知周期表中存在对角相似规则,如Be与Al在周期表中处于对角线位置则化学性质相似,Be的氧化物、氢氧化物也有两性,写出Be的氢氧化物与氢氧化钠反应的化学方程式___________ 。
(1)N、Al、Si、Zn四种元素中,有一种元素的电离能数据如下,则该元素是
| 电离能 |  |  |  |  | …… |
 | 578 | 1817 | 2745 | 11575 | …… |
 的热稳定性高于
的热稳定性高于 的原因
的原因(3)基态氮原子核外电子的空间运动状态有
 的键角约为107°,推测
的键角约为107°,推测 的键角
的键角(4)基态硅原子价层电子轨道表示式为
 与N-甲基咪唑(分子式为:
与N-甲基咪唑(分子式为: ,结构为
,结构为 )反应可以得到一种功能性螯合物。则:C、N、H三种非金属元素的电负性由大到小的顺序是
)反应可以得到一种功能性螯合物。则:C、N、H三种非金属元素的电负性由大到小的顺序是 键。
键。(5)已知周期表中存在对角相似规则,如Be与Al在周期表中处于对角线位置则化学性质相似,Be的氧化物、氢氧化物也有两性,写出Be的氢氧化物与氢氧化钠反应的化学方程式
您最近一年使用:0次
2023-03-28更新
|
687次组卷
|
3卷引用:山东省济宁市微山县第二中学2023-2024学年高三上学期第三次月考化学试题
解题方法
5 . 立方氮化硼硬度高,耐磨性好,在机械加工行业有广泛应用。制备立方氮化硼的一种方法为BCl3(g)+NH3(g)=BN(s)+3HCl(g),下列说法错误的是
| A.反应混合物中所有化学键均为共价键 |
| B.元素电负性大小为N>B |
| C.BCl3和BN均为共价晶体 |
D.形成BCl3时B原子先激发后杂化,其激发态价电子轨道表示式为: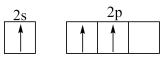 |
您最近一年使用:0次
名校
6 . 下列说法错误的是
A. 、 、 均是由极性键构成的非极性分子 均是由极性键构成的非极性分子 |
B. 与 与 的键角相等 的键角相等 |
C.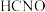 中元素的电负性:O>N>C>H 中元素的电负性:O>N>C>H |
D.如图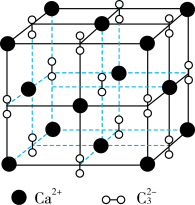 所示的 所示的 立方晶胞中, 立方晶胞中, 的配位数为6 的配位数为6 |
您最近一年使用:0次
2023-01-09更新
|
348次组卷
|
3卷引用:山东省济宁市第一中学2022-2023学年高二下学期期中考试化学试题
名校
解题方法
7 . Fe2(SO4)3溶液可与黄芩素发生显色反应。下列有关说法正确的是
| A.电负性由强到弱的顺序为O>H>C |
| B.Fe3+的基态价电子排布式为3d6 |
| C.黄岑素晶体熔点高、硬度大 |
D.SO 的空间构型为正四面体 的空间构型为正四面体 |
您最近一年使用:0次
名校
解题方法
8 . 二氯异氰尿酸钠是中国疾控中心研发的“-18℃低温消毒剂”主要成分之一,其合成方法如下图。下列说法错误的是
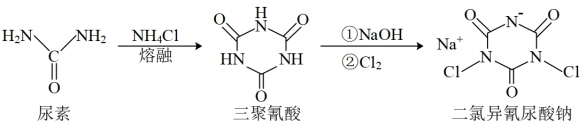

| A.尿素和氯化铵中N原子杂化方式相同 |
| B.二氯异氰尿酸钠所含元素中电负性最大的是氧 |
| C.二氯异氰尿酸钠晶体中存在离子键、共价键和配位键 |
D.三聚氰酸具有与苯环类似的结构,可推知三聚氰酸分子中存在大 键 键 |
您最近一年使用:0次
2022-04-08更新
|
673次组卷
|
5卷引用:山东省青岛市2022高考一模化学试题
名校
9 . 石墨烯具有优异的光学、电学、力学特性,在材料学、微纳加工、能源和生物医学等方面具有广阔的应用前景,石墨烯可采用化学方法制备,如以六氯苯、六溴苯为原料可制备石墨烯。下表是六氯苯、六溴苯、苯六酸的熔点和水溶性:
下列说法正确的是
| 物质 | 六氯苯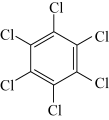 | 六溴苯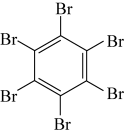 | 苯六酸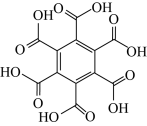 |
| 熔点/℃ | 231 | 325 | 287 |
| 水溶性 | 不溶 | 不溶 | 易溶 |
| A.苯六酸所含元素的电负性:C>O>H |
| B.从结构上看,六氯苯、六溴苯和苯六酸均为极性分子 |
| C.六氯苯、六溴苯和苯六酸分子中C的杂化方式均为sp2杂化 |
| D.苯六酸与六氯苯、六溴苯的水溶性存在明显的差异是因为其分子结构庞大 |
您最近一年使用:0次
2022-03-20更新
|
442次组卷
|
9卷引用:山东省名校联盟2021-2022学年高二下学期质量检测联合调考化学试题
山东省名校联盟2021-2022学年高二下学期质量检测联合调考化学试题山东省名校联盟2021-2022学年高二下学期质量检测联合调考化学(B2)试题湖南省2021-2022学年高二下学期3月大联考化学试题河北省邢台市四校联考2021-2022学年高二下学期第二次月考化学试题吉林省吉林市第一中学2021-2022学年高二下学期第一次质量检测化学试题广东省名校联盟2021-2022学年高二下学期4月大联考化学试题内蒙古额尔古纳市第一中学2021-2022学年高二下学期阶段性考试化学试题福建省名校联盟2021-2022学年高二下学期期中考试化学试题.辽宁省抚顺市第一中学2022届高三下学期5月模拟考试化学试题
名校
解题方法
10 . 下列对有关事实的原因分析错误的是
| 事实 | 原因 | |
| A | 白磷(P4)为正四面体分子 | 白磷分子中P−P键间的夹角是109°28′ |
| B | 分子内不同化学键之间存在一定的夹角 | 共价键具有方向性 |
| C | 键的极性H−O键>H−S键 | O的电负性大于S的电负性 |
| D | 通常状况下,1体积水溶解700体积氨气 | 氨是极性分子且有氢键的影响 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-01-24更新
|
1066次组卷
|
9卷引用:山东省烟台市2021-2022学年高二上学期期末考试化学试题
山东省烟台市2021-2022学年高二上学期期末考试化学试题山东省枣庄市第三中学2021-2022学年高二3月质量检测化学试题山东省沂南第一中学2021-2022学年高二4月月考化学试题(已下线)第二章 分子结构与性质 章节过关检测-2021-2022学年高二化学链接教材精准变式练(人教版2019选择性必修2)湖北省新高考联考协作体2021-2022学年高二3月考试化学试题广东省佛山市顺德区第一中学 2021-2022学年高二下学期期中考试化学试题福建省连城县第一中学2021-2022学年高二下学期第一次月考化学试题(已下线)专题33 物质结构与性质基础-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)广东省深圳市盐田高级中学2022-2023学年高二下学期第一次月考化学试题



