名校
1 .  氰基丙烯酸甲酯(俗称501)因其聚合速度过快、聚合放热,对人体组织的刺激性和毒性较大,被用作普通的瞬干胶。而对
氰基丙烯酸甲酯(俗称501)因其聚合速度过快、聚合放热,对人体组织的刺激性和毒性较大,被用作普通的瞬干胶。而对 氰基丙烯酸甲酯进行结构修饰(如图所示)制得的
氰基丙烯酸甲酯进行结构修饰(如图所示)制得的 氰基丙烯酸正丁酯(俗称504)既有较快的聚合速度,又对人体细胞几乎无毒性,同时还能与比较潮湿的人体组织强烈结合且柔韧性较好,被用作医用胶。已知氰基
氰基丙烯酸正丁酯(俗称504)既有较快的聚合速度,又对人体细胞几乎无毒性,同时还能与比较潮湿的人体组织强烈结合且柔韧性较好,被用作医用胶。已知氰基 具有较强的极性,对邻近化学键具有活化作用。下列说法错误的是
具有较强的极性,对邻近化学键具有活化作用。下列说法错误的是
 氰基丙烯酸甲酯(俗称501)因其聚合速度过快、聚合放热,对人体组织的刺激性和毒性较大,被用作普通的瞬干胶。而对
氰基丙烯酸甲酯(俗称501)因其聚合速度过快、聚合放热,对人体组织的刺激性和毒性较大,被用作普通的瞬干胶。而对 氰基丙烯酸甲酯进行结构修饰(如图所示)制得的
氰基丙烯酸甲酯进行结构修饰(如图所示)制得的 氰基丙烯酸正丁酯(俗称504)既有较快的聚合速度,又对人体细胞几乎无毒性,同时还能与比较潮湿的人体组织强烈结合且柔韧性较好,被用作医用胶。已知氰基
氰基丙烯酸正丁酯(俗称504)既有较快的聚合速度,又对人体细胞几乎无毒性,同时还能与比较潮湿的人体组织强烈结合且柔韧性较好,被用作医用胶。已知氰基 具有较强的极性,对邻近化学键具有活化作用。下列说法错误的是
具有较强的极性,对邻近化学键具有活化作用。下列说法错误的是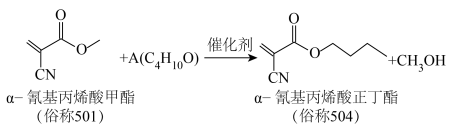
| A.上述反应的反应类型为取代反应 |
| B.504分子中碳原子的杂化轨道类型有3种 |
| C.对501进行结构修饰制得504,是通过增长酯基碳链,使性能得到改良 |
D.由于氰基对邻近酯基的活化作用,使 氰基丙烯酸酯在常温下就能发生加聚反应而固化 氰基丙烯酸酯在常温下就能发生加聚反应而固化 |
您最近一年使用:0次
名校
解题方法
2 . 科研人员利用高压 气流将水微滴喷射到涂覆催化剂的石墨网上,研究常温制氨,其反应历程中微粒转化关系如图1,相对能量变化关系如图2,图中“*”表示催化剂表面吸附位,下列说法正确的是
气流将水微滴喷射到涂覆催化剂的石墨网上,研究常温制氨,其反应历程中微粒转化关系如图1,相对能量变化关系如图2,图中“*”表示催化剂表面吸附位,下列说法正确的是
 气流将水微滴喷射到涂覆催化剂的石墨网上,研究常温制氨,其反应历程中微粒转化关系如图1,相对能量变化关系如图2,图中“*”表示催化剂表面吸附位,下列说法正确的是
气流将水微滴喷射到涂覆催化剂的石墨网上,研究常温制氨,其反应历程中微粒转化关系如图1,相对能量变化关系如图2,图中“*”表示催化剂表面吸附位,下列说法正确的是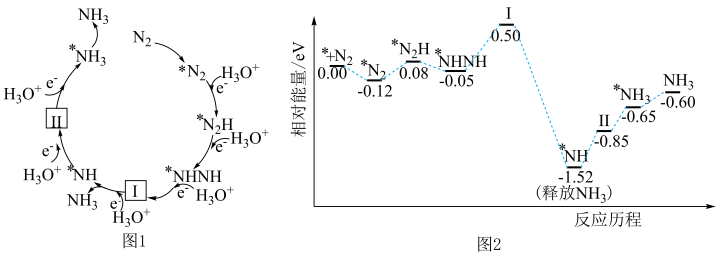
A. 与 与 的 的 模型不相同 模型不相同 |
B. 过程中存在极性键和非极性键的断裂与形成 过程中存在极性键和非极性键的断裂与形成 |
C.反应历程中放热最多的反应是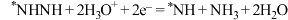 |
D.总反应为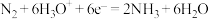 |
您最近一年使用:0次
名校
解题方法
3 . 物质的结构决定物质的性质,下列性质差异与结构因素匹配正确的是
| 性质差异 | 结构因素 | |
| A | 溶解度(20℃):Na2CO3(29g)大于NaHCO3(9g) | 阴离子电荷数 |
| B | 沸点: | 分子间氢键 |
| C | 键角:CH4( )大于NH3( )大于NH3( ) ) | 中心原子的杂化方式 |
| D | 熔点: | 晶体类型 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
4 . 化合物甲是一种常见无机物,其结构如下图所示(图中的“—”为单键或双键),其中W、X、Y、Z为元素周期表中的短周期主族元素,且原子序数依次增大,W和Y、X和Z分别为同主族元素,其四种元素原子的最外层电子数之和为14。下列叙述正确的是
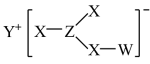
| A.W分别与X、Z形成的简单分子均为10电子微粒 |
| B.X、Y形成的离子化合物只含离子键 |
| C.ZX2的键角小于ZX3的键角 |
| D.等物质的量Y和Z的最高价氧化物对应的水化物反应生成甲 |
您最近一年使用:0次
5 . 下列选项正确的是:
| A.K3[Fe(CN)6]溶液滴入FeCl2溶液中:K++Fe2++[Fe(CN)6]3-=KFe[Fe(CN)6]↓,则1molFe2+的配位数是6NA |
B.反应:CH3CO18OH+C2H5OH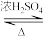 CH3COOC2H5+H218O中, CH3COOC2H5+H218O中,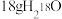 含有的中子数为10 NA 含有的中子数为10 NA |
| C.铅酸蓄电池充电时的阳极反应:Pb2++2H2O-2e-=PbO2+4H+,当线路中通过2NA个电子时,阳极减重64g |
D.将H2S气体通入NaClO溶液出现浑浊的离子方程式:H2S + ClO- = S↓ + Cl- + H2O,若产生的S为S8(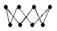 ),则32gS8中含有2NA个孤电子对 ),则32gS8中含有2NA个孤电子对 |
您最近一年使用:0次
名校
解题方法
6 . 硫代硫酸钠( )是一种具有应用前景的浸金试剂,浸金时
)是一种具有应用前景的浸金试剂,浸金时 与
与 配位形成
配位形成 。下列说法错误的是
。下列说法错误的是
 )是一种具有应用前景的浸金试剂,浸金时
)是一种具有应用前景的浸金试剂,浸金时 与
与 配位形成
配位形成 。下列说法错误的是
。下列说法错误的是A.第一电离能: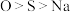 |
B. 和 和 的中心S原子均采用 的中心S原子均采用 杂化 杂化 |
C.与 配位时, 配位时, 中两个S原子都可作配位原子 中两个S原子都可作配位原子 |
D.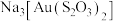 晶体中微粒间存在的相互作用有离子键、共价键和配位键 晶体中微粒间存在的相互作用有离子键、共价键和配位键 |
您最近一年使用:0次
7 . 我国科学家开发绿色工艺合成高能材料PVAA和PNBAA,结构如图所示。下列叙述正确的是

| A.PVAA和PNBAA所含官能团种类相同 |
| B.PVAA、PNBAA的单体中碳原子杂化类型相同 |
| C.PVAA和PNBAA是绿色炸药且能自然降解 |
D. PNBAA含 PNBAA含 手性碳原子 手性碳原子 |
您最近一年使用:0次
名校
8 . 反应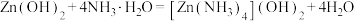 中的有关物质的说法不正确的是
中的有关物质的说法不正确的是
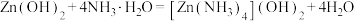 中的有关物质的说法不正确的是
中的有关物质的说法不正确的是A.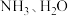 固态时均属于分子晶体 固态时均属于分子晶体 |
B.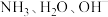 均为 均为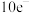 微粒 微粒 |
C. 分子中的键角 分子中的键角 比 比 中的键角 中的键角 大 大 |
D. 中存在离子键、配位键、极性键 中存在离子键、配位键、极性键 |
您最近一年使用:0次
名校
解题方法
9 . 下列符号表征或说法错误的是
A. 的电离: 的电离: |
B.基态Fe原子的价层电子排布式: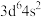 |
C. 的结构示意图: 的结构示意图: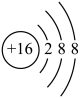 |
D. 分子的空间结构:三角锥形 分子的空间结构:三角锥形 |
您最近一年使用:0次
10 . 某种化合物的结构如图所示,其中X、Y、Z、Q、W为原子序数依次增大的五种短周期主族元素,基态Q原子s轨道上的电子数和p轨道上的电子数相等,Y是形成化合物种类最多的元素,X的原子半径是元素周期表中最小的.下列叙述正确的是
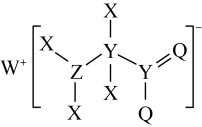
| A.X、Y两元素组成的分子的空间结构均为正四面体形 |
| B.X、W分别与Q形成的化合物可能具有强氧化性 |
C.第一电离能: |
| D.该化合物中有极性键、非极性键、配位键和离子键 |
您最近一年使用:0次

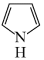 (131℃)>
(131℃)>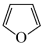 (31.36℃)
(31.36℃) 低于
低于


