名校
解题方法
1 . 某化合物具漂白性,主要用于染色工艺,其结构如图所示,其中W、X、Y、M、Z是原子序数依次递增的短周期主族元素,且Y和 同主族,下列说法错误的是
同主族,下列说法错误的是
 同主族,下列说法错误的是
同主族,下列说法错误的是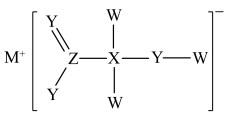
A.电负性: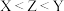 | B. 和 和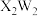 均为极性分子 均为极性分子 |
| C.MW与水反应后的溶液呈碱性 | D. 利 利 的VSEPR模型名称均为平面三角形 的VSEPR模型名称均为平面三角形 |
您最近一年使用:0次
今日更新
|
265次组卷
|
3卷引用:湖北省武汉市2024届高三毕业生四月调研考试(二模)化学试题
2 . 奥司他韦(Oseltamivir)是一种作用于神经氨酸酶的特异性抑制剂,其对神经氨酸酶的抑制能起到治疗流行性感冒的作用,结构简式如图所示,下列说法正确的是
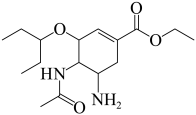
| A.奥司他韦分子中有3个手性碳原子 |
B.奥司他韦中C原子的杂化方式有两种,N原子的杂化方式只有 |
C.分子式为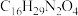 |
| D.该分子可发生取代、加成、消去、氧化反应 |
您最近一年使用:0次
3 . 以水钴矿(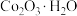 ,含
,含 、MgO、CaO)和辉铜矿(
、MgO、CaO)和辉铜矿( ,含
,含 、
、 )为原料制取胆矾和单质钴。
)为原料制取胆矾和单质钴。 ,
,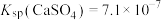 ,
,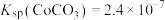 ;
;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
③萃取 的反应原理;
的反应原理; ;
;
④Mg、Ca、Fe、Co均能与强酸反应产生 。
。
回答下列问题:
(1)基态Co原子的简化电子排布式为___________ 。
(2)“酸浸”过程硫元素价态变为 价,写出“酸浸”过程中主要反应的化学方程式:
价,写出“酸浸”过程中主要反应的化学方程式:___________ 。
(3)“滤渣1”的主要成分为___________ 。
(4)常温下,若“滤液2”中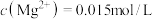 (忽略溶液中极少量的
(忽略溶液中极少量的 ),除去2L“滤液2”中的
),除去2L“滤液2”中的 ,至少需加入NaF固体的质量为
,至少需加入NaF固体的质量为___________ g(忽略溶液体积的变化)。
(5)“反萃取”步骤中加入的“试剂a”为___________ 。
(6)采用惰性电极电解 溶液﹑在无离子交换膜的条件下,不能用
溶液﹑在无离子交换膜的条件下,不能用 溶液代替
溶液代替 溶液的理由是
溶液的理由是___________ 。
(7)将制得的胆矾配成溶液,先加入足量氨水,得到深蓝色溶液,再通入 至弱酸性,生成白色沉淀和硫酸铵。经仪器分析:白色沉淀含H、N、O、S、Cu五种元素;所含Cu离子中无单电子;晶体的部分组成微粒的空间构型分别为一种三角锥形和一种正四面体形。则白色沉淀的化学式为
至弱酸性,生成白色沉淀和硫酸铵。经仪器分析:白色沉淀含H、N、O、S、Cu五种元素;所含Cu离子中无单电子;晶体的部分组成微粒的空间构型分别为一种三角锥形和一种正四面体形。则白色沉淀的化学式为___________ 。
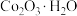 ,含
,含 、MgO、CaO)和辉铜矿(
、MgO、CaO)和辉铜矿( ,含
,含 、
、 )为原料制取胆矾和单质钴。
)为原料制取胆矾和单质钴。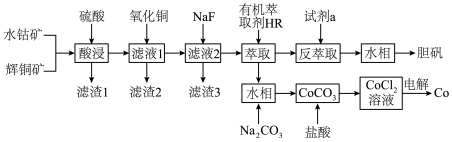
 ,
,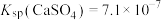 ,
,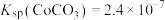 ;
;②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 金属离子 |  |  |  |  |
开始沉淀时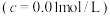 的pH 的pH | 2.7 | 7.5 | 7.6 | 4.7 |
完全沉淀时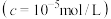 的pH 的pH | 3.7 | 9.0 | 9.1 | 6.2 |
 的反应原理;
的反应原理; ;
;④Mg、Ca、Fe、Co均能与强酸反应产生
 。
。回答下列问题:
(1)基态Co原子的简化电子排布式为
(2)“酸浸”过程硫元素价态变为
 价,写出“酸浸”过程中主要反应的化学方程式:
价,写出“酸浸”过程中主要反应的化学方程式:(3)“滤渣1”的主要成分为
(4)常温下,若“滤液2”中
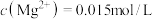 (忽略溶液中极少量的
(忽略溶液中极少量的 ),除去2L“滤液2”中的
),除去2L“滤液2”中的 ,至少需加入NaF固体的质量为
,至少需加入NaF固体的质量为(5)“反萃取”步骤中加入的“试剂a”为
(6)采用惰性电极电解
 溶液﹑在无离子交换膜的条件下,不能用
溶液﹑在无离子交换膜的条件下,不能用 溶液代替
溶液代替 溶液的理由是
溶液的理由是(7)将制得的胆矾配成溶液,先加入足量氨水,得到深蓝色溶液,再通入
 至弱酸性,生成白色沉淀和硫酸铵。经仪器分析:白色沉淀含H、N、O、S、Cu五种元素;所含Cu离子中无单电子;晶体的部分组成微粒的空间构型分别为一种三角锥形和一种正四面体形。则白色沉淀的化学式为
至弱酸性,生成白色沉淀和硫酸铵。经仪器分析:白色沉淀含H、N、O、S、Cu五种元素;所含Cu离子中无单电子;晶体的部分组成微粒的空间构型分别为一种三角锥形和一种正四面体形。则白色沉淀的化学式为
您最近一年使用:0次
4 . 设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.标准状况下,22.4L HF的原子数为 |
B. 和 和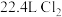 (均为标准状况)在光照下充分反应后的分子数目为 (均为标准状况)在光照下充分反应后的分子数目为 |
C. 水解能力弱于 水解能力弱于 , ,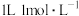 的 的 溶液中HF和 溶液中HF和 的总数大于 的总数大于 |
D.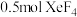 中氙的价层电子对数为 中氙的价层电子对数为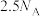 |
您最近一年使用:0次
5 . 下列关于超分子和配合物的叙述错误的是
A.配合物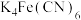 配离子的中心离子配位数是6 配离子的中心离子配位数是6 |
B.配合物 中存在离子键、共价键、配位键,若加入足量 中存在离子键、共价键、配位键,若加入足量 溶液,所有 溶液,所有 均被完全沉淀 均被完全沉淀 |
C.超分子“杯酚”具有分子识别的特性,利用此特性可分离 和 和 |
| D.人体细胞和细胞器的双分子膜体现了超分子的自组装特征 |
您最近一年使用:0次
解题方法
6 . 稀有气体化合物在化学、照明、医疗等众多领域有广泛应用,含Xe化合物的种类较多,氙的氟化物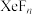 与NaOH溶液反应剧烈,与水反应则较为温和,反应方程式如下:
与NaOH溶液反应剧烈,与水反应则较为温和,反应方程式如下:
与水反应:ⅰ.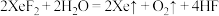 ⅲ.
ⅲ.
与NaOH溶液反应:ⅱ.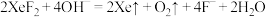 ⅳ.
ⅳ.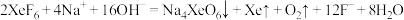
下列关说法错误的是
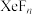 与NaOH溶液反应剧烈,与水反应则较为温和,反应方程式如下:
与NaOH溶液反应剧烈,与水反应则较为温和,反应方程式如下:与水反应:ⅰ.
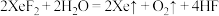 ⅲ.
ⅲ.
与NaOH溶液反应:ⅱ.
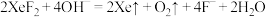 ⅳ.
ⅳ.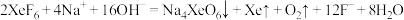
下列关说法错误的是
A. 中氙的价层电子对数为6 中氙的价层电子对数为6 |
B. 的键角小于 的键角小于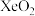 |
| C.较He、Ne、Ar、Kr原子,Xe原子半径大,电离能小,所以含Xe的化合物种类更多 |
| D.反应ⅰ~ⅳ中有3个氧化还原反应 |
您最近一年使用:0次
7 . 设 为阿伏加德罗常数的值。钛镍记忆合金用于制造神舟十四号飞船的天线。钛酸亚铁高温(FeTiO3)通过以下反应转化为Ti,用于冶炼钛:
为阿伏加德罗常数的值。钛镍记忆合金用于制造神舟十四号飞船的天线。钛酸亚铁高温(FeTiO3)通过以下反应转化为Ti,用于冶炼钛: 。下列说法错误的是
。下列说法错误的是
 为阿伏加德罗常数的值。钛镍记忆合金用于制造神舟十四号飞船的天线。钛酸亚铁高温(FeTiO3)通过以下反应转化为Ti,用于冶炼钛:
为阿伏加德罗常数的值。钛镍记忆合金用于制造神舟十四号飞船的天线。钛酸亚铁高温(FeTiO3)通过以下反应转化为Ti,用于冶炼钛: 。下列说法错误的是
。下列说法错误的是A.每生成1mol 转移电子数为7 转移电子数为7 | B.1mol基态Ti原子中未成对电子数为2 |
C.1mol 中含5 中含5 配位键 配位键 | D.2L1mol/L的 溶液中,阳离子数目大于2 溶液中,阳离子数目大于2 |
您最近一年使用:0次
8 . 下列方案设计、现象和结论都正确的是
| 选项 | 目的 | 方案设计 | 现象和结论 |
| A | 检验丙烯醛中含有碳碳双键 | 向丙烯醛中加入足量新制氢氧化铜悬浊液,加热至不再生成砖红色沉淀,静置,向上层清液中滴加溴水 | 若溴水褪色,则丙烯醛中含有碳碳双键 |
| B | 探究不同价态硫元素的转化 | 向 与 与 的混合液中加入硝酸 的混合液中加入硝酸 | 溶液变浑浊,证明 与 与 在酸性条件下发生了归中反应 在酸性条件下发生了归中反应 |
| C | 探究压强对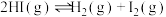 的影响 的影响 | 压缩体积,增大反应容器压强 | 气体颜色加深,则说明增大压强,该化学平衡正向移动 |
| D | 验证 与 与 在配合物形成过程中存在相互竞争 在配合物形成过程中存在相互竞争 | 向 溶液中加入少量NaCl固体 溶液中加入少量NaCl固体 | 溶液由蓝色变为黄绿色,说明发生了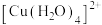 到 到 的转化 的转化 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
9 . X、Y、Z为短周期主族元素,X的原子序数是Y的8倍,X与Z同周期,且基态X、Z原子的未成对电子数相同。M是人体的必需微量元素之一,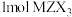 含有
含有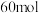 质子。下列说法一定正确的是
质子。下列说法一定正确的是
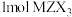 含有
含有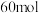 质子。下列说法一定正确的是
质子。下列说法一定正确的是| A.M在元素周期表中位于d区 | B. 中Z原子采用 中Z原子采用 杂化 杂化 |
| C.X、Z分别与Y形成化合物的沸点:X>Z | D.同周期元素中第一电离能比X大的有3种 |
您最近一年使用:0次
名校
解题方法
10 . 用NA表示阿伏加德罗常数的值。下列说法正确的是
A.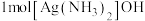 中 中 键的数目为6NA 键的数目为6NA |
B.92g甘油中 杂化的原子数目为3NA 杂化的原子数目为3NA |
C.标况下 甲醇完全燃烧,消耗 甲醇完全燃烧,消耗 分子的数目为1.5NA 分子的数目为1.5NA |
D.向 乙酸溶液中通入氨气至中性, 乙酸溶液中通入氨气至中性, 的数目小于0.1NA 的数目小于0.1NA |
您最近一年使用:0次



