1 . 一水合硫酸四氨合铜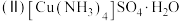 为蓝色正交晶体,在工业上用途广泛,主要用于印染、电镀、纤维、杀虫剂的制备和制备某些含铜的化合物。常温下,一水合硫酸四氨合铜(Ⅱ)易与空气中的二氧化碳、水反应生成铜的碱式盐,使晶体变成绿色粉末。其制备方法如下:
为蓝色正交晶体,在工业上用途广泛,主要用于印染、电镀、纤维、杀虫剂的制备和制备某些含铜的化合物。常温下,一水合硫酸四氨合铜(Ⅱ)易与空气中的二氧化碳、水反应生成铜的碱式盐,使晶体变成绿色粉末。其制备方法如下:
①向一只锥形瓶中加入约50mL水,放置于磁力搅拌器上,速度调节为中速。
②将16g无水硫酸铜晶体缓慢地加入锥形瓶中,同时加入3~5mL稀硫酸。当硫酸铜晶体在常温下不再溶解时即可停止加入硫酸铜,如仍有部分硫酸铜晶体未溶就微热促使硫酸铜溶解。此时溶液呈淡蓝色。关闭磁力搅拌器,取下锥形瓶。
③向上一步的溶液中缓慢加入1:1氨水。可观察到先出现淡蓝色沉淀,随着氨水的增多,上层出现一深蓝色液层,沉淀部分溶解。滴加氨水直到之前的蓝色沉淀完全溶解,再加氨水稍过量3~5mL即可。此时溶液呈深蓝色,较为不透光。
④摇匀后抽滤使溶液中不含不溶物,得到的溶液倒入烧杯。
⑤向上一步的溶液中缓慢加入乙醇,观察到开始有部分深蓝色晶体沉积在杯壁上。加乙醇直到晶体完全沉降。盖上表面血静置15min。此时杯壁上沉积着大量 晶体。倾析法除去大部分乙醇。进行抽滤。
晶体。倾析法除去大部分乙醇。进行抽滤。
⑥用氨水:乙醇=1:2的溶液洗涤所得产品,之后再一次用95%乙醇清洗产品。抽滤至干燥,得产品20g。
(1)步骤②中,溶解 固体的过程中,加入稀硫酸的目的是
固体的过程中,加入稀硫酸的目的是_______ 。
(2)步骤③中,加入1:1氨水产生深蓝色溶液的过程,发生反应的化学方程式为_______ 。说明H2O与Cu2+结合的稳定程度小于NH3,试从结构的角度进行解释:_______ 。
(3)步骤⑤中,加乙醇析出深蓝色溶液的原因是_______ 。
(4)抽滤所得母液中, 受热易分解,从中回收乙醇可采取的方式是
受热易分解,从中回收乙醇可采取的方式是_______ 。
(5)若将生成的四氨合铜离子中的两个NH3换成Cl-,则存在顺式和反式两种不同的立体异构体,则四氨合铜离子的空间结构应为_______ 形。
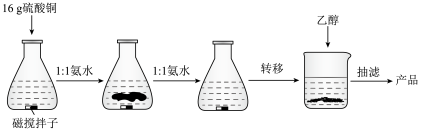
(6)过滤操作的主要目的是将固液混合物进行分离。中学化学中常见的用于固液混合物分离的操作有“普通过滤”和“减压过滤”等,操作示意图如下:
(7)该实验过程的产率为_______ (保留三位有效数字)。
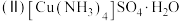 为蓝色正交晶体,在工业上用途广泛,主要用于印染、电镀、纤维、杀虫剂的制备和制备某些含铜的化合物。常温下,一水合硫酸四氨合铜(Ⅱ)易与空气中的二氧化碳、水反应生成铜的碱式盐,使晶体变成绿色粉末。其制备方法如下:
为蓝色正交晶体,在工业上用途广泛,主要用于印染、电镀、纤维、杀虫剂的制备和制备某些含铜的化合物。常温下,一水合硫酸四氨合铜(Ⅱ)易与空气中的二氧化碳、水反应生成铜的碱式盐,使晶体变成绿色粉末。其制备方法如下:①向一只锥形瓶中加入约50mL水,放置于磁力搅拌器上,速度调节为中速。
②将16g无水硫酸铜晶体缓慢地加入锥形瓶中,同时加入3~5mL稀硫酸。当硫酸铜晶体在常温下不再溶解时即可停止加入硫酸铜,如仍有部分硫酸铜晶体未溶就微热促使硫酸铜溶解。此时溶液呈淡蓝色。关闭磁力搅拌器,取下锥形瓶。
③向上一步的溶液中缓慢加入1:1氨水。可观察到先出现淡蓝色沉淀,随着氨水的增多,上层出现一深蓝色液层,沉淀部分溶解。滴加氨水直到之前的蓝色沉淀完全溶解,再加氨水稍过量3~5mL即可。此时溶液呈深蓝色,较为不透光。
④摇匀后抽滤使溶液中不含不溶物,得到的溶液倒入烧杯。
⑤向上一步的溶液中缓慢加入乙醇,观察到开始有部分深蓝色晶体沉积在杯壁上。加乙醇直到晶体完全沉降。盖上表面血静置15min。此时杯壁上沉积着大量
 晶体。倾析法除去大部分乙醇。进行抽滤。
晶体。倾析法除去大部分乙醇。进行抽滤。⑥用氨水:乙醇=1:2的溶液洗涤所得产品,之后再一次用95%乙醇清洗产品。抽滤至干燥,得产品20g。
(1)步骤②中,溶解
 固体的过程中,加入稀硫酸的目的是
固体的过程中,加入稀硫酸的目的是(2)步骤③中,加入1:1氨水产生深蓝色溶液的过程,发生反应的化学方程式为
(3)步骤⑤中,加乙醇析出深蓝色溶液的原因是
(4)抽滤所得母液中,
 受热易分解,从中回收乙醇可采取的方式是
受热易分解,从中回收乙醇可采取的方式是(5)若将生成的四氨合铜离子中的两个NH3换成Cl-,则存在顺式和反式两种不同的立体异构体,则四氨合铜离子的空间结构应为
(6)过滤操作的主要目的是将固液混合物进行分离。中学化学中常见的用于固液混合物分离的操作有“普通过滤”和“减压过滤”等,操作示意图如下:

| A.过滤速度相对较快 | B.能过滤胶状混合物 |
| C.得到的固体物质相对比较干燥 | D.可使沉淀中的杂质减少 |
(7)该实验过程的产率为
您最近一年使用:0次
2 . 叶绿素是高等植物和其他所有能进行光合作用的生物体含有的一类绿色色素。叶绿素a结构如图所示,下列说法正确的是
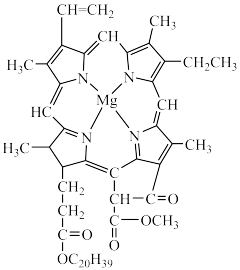
| A.叶绿素a是高分子化合物 |
B.叶绿素a中, 的配位数为2 的配位数为2 |
| C.叶绿素a中,C、N原子的杂化方式相同 |
| D.叶绿素a不能发生消去反应 |
您最近一年使用:0次
3 . 羰基硫(COS)是一种粮食熏蒸剂,能防止某些害虫和真菌的危害,工业上用于合成除草剂、杀草丹、燕麦敌、杀虫剂巴丹等。其结构与 类似。工业上一般通过
类似。工业上一般通过 或者CO与
或者CO与 反应制取COS,发生的相关反应如下:
反应制取COS,发生的相关反应如下:
i.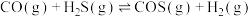
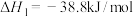
ii.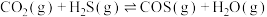
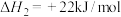
iii.

(1)
_______ 。
(2)COS的中心原子的杂化方式为_______ 。
(3)在一定温度下,将4molCO和 通入一固定容积的密闭容器中发生上述反应i。
通入一固定容积的密闭容器中发生上述反应i。
①能证明上述反应达到平衡的标志是_______ (填字母)。
A.CO和 的转化率相等 B.
的转化率相等 B. 的体积分数不再变化
的体积分数不再变化
C.混合气体的密度不再变化 D.CO、 、COS、
、COS、 浓度之比为1:1:1:1
浓度之比为1:1:1:1
②上述反应达到平衡后, 所占的体积分数为12.5%,则该反应的平衡常数为
所占的体积分数为12.5%,则该反应的平衡常数为_______ (保留两位有效数字)。若此时再向体系中加入0.5molCO和 ,平衡将
,平衡将_______ (填“向正反应方向”“向逆反应方向”或“不”)移动;理由是_______ 。
(4)将4molCO和 通入一固定容积的密闭容器中发生上述反应i,反应5分钟,CO的转化率随温度的变化关系如图所示。a点
通入一固定容积的密闭容器中发生上述反应i,反应5分钟,CO的转化率随温度的变化关系如图所示。a点_______ (填“是”或“不是”)平衡状态,判断的理由是_______ 。 、1molCO和
、1molCO和 通入一固定容积的密闭容器中发生上述反应i、ii和iii,CO、
通入一固定容积的密闭容器中发生上述反应i、ii和iii,CO、 和
和 平衡时的转化率如图所示,
平衡时的转化率如图所示, 转化率先减小后增大的原因是
转化率先减小后增大的原因是_______ 。
 类似。工业上一般通过
类似。工业上一般通过 或者CO与
或者CO与 反应制取COS,发生的相关反应如下:
反应制取COS,发生的相关反应如下:i.
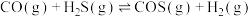
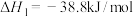
ii.
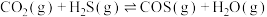
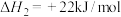
iii.


(1)

(2)COS的中心原子的杂化方式为
(3)在一定温度下,将4molCO和
 通入一固定容积的密闭容器中发生上述反应i。
通入一固定容积的密闭容器中发生上述反应i。①能证明上述反应达到平衡的标志是
A.CO和
 的转化率相等 B.
的转化率相等 B. 的体积分数不再变化
的体积分数不再变化C.混合气体的密度不再变化 D.CO、
 、COS、
、COS、 浓度之比为1:1:1:1
浓度之比为1:1:1:1②上述反应达到平衡后,
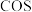 所占的体积分数为12.5%,则该反应的平衡常数为
所占的体积分数为12.5%,则该反应的平衡常数为 ,平衡将
,平衡将(4)将4molCO和
 通入一固定容积的密闭容器中发生上述反应i,反应5分钟,CO的转化率随温度的变化关系如图所示。a点
通入一固定容积的密闭容器中发生上述反应i,反应5分钟,CO的转化率随温度的变化关系如图所示。a点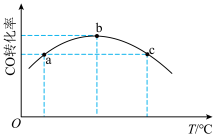
 、1molCO和
、1molCO和 通入一固定容积的密闭容器中发生上述反应i、ii和iii,CO、
通入一固定容积的密闭容器中发生上述反应i、ii和iii,CO、 和
和 平衡时的转化率如图所示,
平衡时的转化率如图所示, 转化率先减小后增大的原因是
转化率先减小后增大的原因是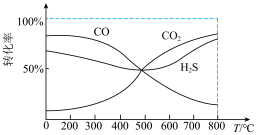
您最近一年使用:0次
4 . 化合物a的结构如图,X、Y、Z、M、N是原子序数依次增大的短周期主族元素,其中Z和N位于同一主族。下列说法错误的是
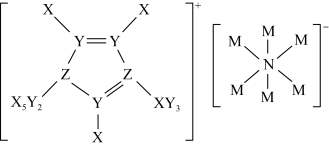
A.第一电离能: | B.化合物a在常温下可能呈液态 |
C.氢化物的沸点: | D.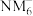 中心原子的杂化方式为 中心原子的杂化方式为 |
您最近一年使用:0次
解题方法
5 . 化学用语是化学学习的基础,下列化学用语表述错误的是
A. 的电子式: 的电子式: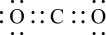 | B.次氯酸分子的结构式: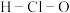 |
C.HCl中 键电子云: 键电子云: | D. 的VSEPR模型: 的VSEPR模型: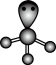 |
您最近一年使用:0次
6 . 实验装置为实验提供必要条件和测量手段。如图装置不能达到实验目的的是
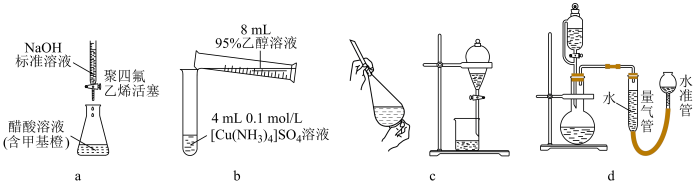
| A.图a测定醋酸溶液的浓度 |
| B.图b制备[Cu(NH3)4]SO4•H2O晶体 |
| C.图c用NaOH溶液除去溴苯中的溴单质 |
| D.图d测定一定质量的Na2O2和Na2O混合物中Na2O2的含量 |
您最近一年使用:0次
昨日更新
|
370次组卷
|
2卷引用:湖南省长沙市雅礼中学2024届高三下学期模拟考卷(二)化学试题
名校
7 . 一种利用废铜渣(主要成分为 ,及少量的
,及少量的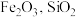 等杂质)制备超细铜粉的流程如下:
等杂质)制备超细铜粉的流程如下:
 ,及少量的
,及少量的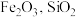 等杂质)制备超细铜粉的流程如下:
等杂质)制备超细铜粉的流程如下:
A.“酸浸”所得滤渣的主要成分为 |
B.向“沉铁”后的滤液中加入乙醇,析出的深蓝色晶体为 |
C.“沉铜”过程中发生了氧化还原反应, 是还原剂 是还原剂 |
D.“转化”后的滤液中含有的阳离子为 和 和 |
您最近一年使用:0次
昨日更新
|
478次组卷
|
4卷引用:2024届湖南省益阳市安化县第二中学高三下学期三模化学试题
解题方法
8 . 橄榄石是自然界存在最古老的宝石之一,某橄榄石的成分可以表示为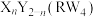 。已知:W、X、R、Y是原子序数依次增大的前四周期元素,基态W、X原子s轨道上的电子数和p轨道上的电子数都相等,基态R原子核外有14种不同运动状态的电子,Y的原子序数为X与R的原子序数之和。下列说法错误的是
。已知:W、X、R、Y是原子序数依次增大的前四周期元素,基态W、X原子s轨道上的电子数和p轨道上的电子数都相等,基态R原子核外有14种不同运动状态的电子,Y的原子序数为X与R的原子序数之和。下列说法错误的是
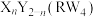 。已知:W、X、R、Y是原子序数依次增大的前四周期元素,基态W、X原子s轨道上的电子数和p轨道上的电子数都相等,基态R原子核外有14种不同运动状态的电子,Y的原子序数为X与R的原子序数之和。下列说法错误的是
。已知:W、X、R、Y是原子序数依次增大的前四周期元素,基态W、X原子s轨道上的电子数和p轨道上的电子数都相等,基态R原子核外有14种不同运动状态的电子,Y的原子序数为X与R的原子序数之和。下列说法错误的是A.第一电离能: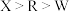 | B.简单氢化物的键角: |
| C.工业上冶炼X、Y单质的方法不同 | D.该橄榄石晶体中存在R、W形成的四面体结构 |
您最近一年使用:0次
9 . 工业上处理含铬( )酸性废水有多种方法,其中两种方法如下:
)酸性废水有多种方法,其中两种方法如下:
Ⅰ. 还原法:含铬酸性废水
还原法:含铬酸性废水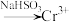 (含
(含 等)
等)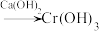 沉淀(含
沉淀(含 等沉淀)
等沉淀)
Ⅱ.电解法:含铬酸性废水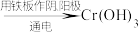 沉淀[含
沉淀[含 等沉淀]
等沉淀]
下列说法错误的是
 )酸性废水有多种方法,其中两种方法如下:
)酸性废水有多种方法,其中两种方法如下:Ⅰ.
 还原法:含铬酸性废水
还原法:含铬酸性废水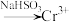 (含
(含 等)
等)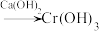 沉淀(含
沉淀(含 等沉淀)
等沉淀)Ⅱ.电解法:含铬酸性废水
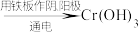 沉淀[含
沉淀[含 等沉淀]
等沉淀]下列说法错误的是
A. 和 和 中的S原子都采用 中的S原子都采用 杂化 杂化 |
B.Ⅰ和Ⅱ中,等量的 发生还原反应时消耗的 发生还原反应时消耗的 的量不同 的量不同 |
C.Ⅰ中参加反应的 |
D.Ⅱ中处理含 的废水转移6mol电子 的废水转移6mol电子 |
您最近一年使用:0次

 在水中的溶解度比
在水中的溶解度比 的小
的小 可形成二聚体
可形成二聚体


