名校
解题方法
1 . 下列物质中,分子的立体结构与水分子相似的是 ( )
| A.CO2 | B.H2S | C.PCl3 | D.SiCl4 |
您最近一年使用:0次
2020-05-23更新
|
753次组卷
|
11卷引用:重庆市荣昌永荣中学校2021-2022学年高二下学期期末考试化学试题
重庆市荣昌永荣中学校2021-2022学年高二下学期期末考试化学试题2016-2017学年河北省张家口一中高二12月月考化学卷广西靖西市第二中学2019-2020学年高二下学期开学考试化学试题山东省淄博市般阳中学2020-2021学年高二上学期期中考试化学试题(人教版2019)选择性必修2 第二章 分子结构与性质 第二节 分子的空间结构(人教版2019)选择性必修2 第二章 分子结构与性质 章末综合检测卷(鲁科版2019)选择性必修2 第2章 微粒间相互作用与物质性质 第2节 共价键与分子的空间结构(已下线)2.2.1 分子空间结构的理论分析-2020-2021学年高二化学课时同步练(鲁科2019选择性必修2)宁夏海原第一中学2020-2021学年高二下学期期末考试化学试题吉林地区普通高中友好学校联合体2021-2022学年高二下学期期末考试化学试题第二节 分子的空间结构 第1课时 分子结构的测定 多样的分子空间结构 价层电子对互斥模型
名校
2 . X、Y、Z、W是四种原子序数依次增大的短周期元素,W的最外层电子数比X的最外层电子数少1个,X、Y、Z为同一周期元素,X、Y、Z组成一种化合物(ZXY)2的结构式如图所示。下列叙述不正确的是( )
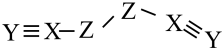
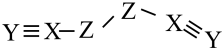
| A.化合物(ZXY)2中Z元素的化合价为-2价 |
| B.Y的氧化物对应的水化物可能是弱酸 |
| C.(ZXY)2分子中X原子的杂化方式为sp杂化 |
| D.X、Y、Z、W四种元素电负性的大小顺序为:Z>Y>X>W |
您最近一年使用:0次
2020-05-20更新
|
134次组卷
|
3卷引用:重庆市第八中学2020-2021学年高二下学期期中考试化学试题
3 . 铁及其化合物在生产生活中有着广泛的应用。回答下列问题:
(1)基态Fe原子的外围电子排布图为____ ,基态Fe2+中,核外电子占据最高能层的符号是____ ,Fe2+和Fe3+是铁的两种常见离子,Fe3+的稳定性强于Fe2+,原因是____ 。
(2)Fe3+可以与SCN—形成一系列不同配位数的红色配合物,所以常用KSCN溶液检验Fe3+的存在,KSCN中四种元素的电负性由小到大的顺序为_______ ,SCN—的几何构型为______ ,中心原子的杂化类型为_______ 。
(3)实验中常用K3[Fe(CN)6]检验Fe2+, K3[Fe(CN)6]晶体中的化学键有_________ (填写选项字母)
a.离子键. b.共价键 c,氢键 d .配位键 e.金属键
1mol K3[Fe(CN)6]中含有σ键与π键的数目比为_____________ 。
(4)FexO为氯化钠型结构,在实际晶体中,由于存在缺陷,x<1。 测得Fe0.92O晶体的晶胞参数a=428.0pm,则该晶体的密度ρ=__________ g/cm3 (列出计算式),晶体中最近的两个铁离子间的距离为_______ pm。
(1)基态Fe原子的外围电子排布图为
(2)Fe3+可以与SCN—形成一系列不同配位数的红色配合物,所以常用KSCN溶液检验Fe3+的存在,KSCN中四种元素的电负性由小到大的顺序为
(3)实验中常用K3[Fe(CN)6]检验Fe2+, K3[Fe(CN)6]晶体中的化学键有
a.离子键. b.共价键 c,氢键 d .配位键 e.金属键
1mol K3[Fe(CN)6]中含有σ键与π键的数目比为
(4)FexO为氯化钠型结构,在实际晶体中,由于存在缺陷,x<1。 测得Fe0.92O晶体的晶胞参数a=428.0pm,则该晶体的密度ρ=
您最近一年使用:0次
2020-05-20更新
|
386次组卷
|
3卷引用:重庆市第八中学2020届高三高考模拟试卷化学试题(三)
名校
解题方法
4 . 元素A、B、C、D、E的原子序数依次增大,且均小于36。A的基态原子2p能级有3个单电子;C的基态原子2p能级有1个单电子;D的价电子数为2且与E同周期;E的基态原子的内部各能层均排满,且4s能级有1个单电子。回答下列问题:
(1)基态E原子的价电子排布式为____________________
(2)A、B、C三种元素第一电离能由大到小的顺序为___________ (用元素符号表示)。
(3)与A的单质分子互为等电子体的分子和离子分别是________ (用分子和离子符号表示)。AB2的空间构型为___________ ,其中A原子的杂化类型是_______________
(4)B元素简单氢化物的沸点是同族元素中最高的,原因是_____________
(5)向含E元素的硫酸盐溶液中加入过量氨水,可得到深蓝色透明溶液。向溶液中加入乙醇,将析出深蓝色晶体。该晶体的化学式为[Cu(NH3)4]SO4∙H2O晶体中阳离子的结构式为____________
(6)C和D形成化合物的晶胞结构如图所示,已知晶体的密度为ρg/cm,阿伏加 德罗常数为NA,则晶胞边长a=______________ cm(用含ρ、NA的计算式表示)。

(1)基态E原子的价电子排布式为
(2)A、B、C三种元素第一电离能由大到小的顺序为
(3)与A的单质分子互为等电子体的分子和离子分别是
(4)B元素简单氢化物的沸点是同族元素中最高的,原因是
(5)向含E元素的硫酸盐溶液中加入过量氨水,可得到深蓝色透明溶液。向溶液中加入乙醇,将析出深蓝色晶体。该晶体的化学式为[Cu(NH3)4]SO4∙H2O晶体中阳离子的结构式为
(6)C和D形成化合物的晶胞结构如图所示,已知晶体的密度为ρg/cm,阿伏加 德罗常数为NA,则晶胞边长a=

您最近一年使用:0次
2020-05-09更新
|
105次组卷
|
2卷引用:重庆市凤鸣山中学2020届高三6月月考理综化学试题
名校
解题方法
5 . 储氢材料是一类能可逆地吸收和释放氢气的材料。LaNi5合金、NaBH4、H3B-NH3、Mg2NiH4等都是潜在储氢材料。回答下列问题:
(1)基态Ni原子的核外电子排布式为____ ,有___________ 个未成对的电子;
(2)NaBH4中H为-1价,Na、B、H电负性由大到小的顺序是_________ 。BH4-离子的立体构型为________ ,其中B的杂化轨道类型为_____ 。
(3)B2H6和NH3化合可以生成H3B-NH3,H3B-NH3加热时发生反应:H3B-NH3=BN+3H2,缓慢释放出H2。BN有类似于石墨的结构,B2H6、NH3和BN的沸点由高到低的顺序为_________ , 原因是___ 。
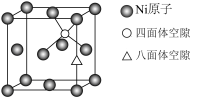
(4)X-射线衍射分析表明,Mg2NiH4 的立方晶胞的面心和顶点均被Ni原子占据,所有Mg原子的Ni配位数都相等。则Mg原子填入由Ni原子形成的_____ 空隙中(填“四面体”或“八面体”),其空隙占有百分率为_____ 。
(5)已知Mg2NiH4 晶体的晶胞参数为646.5 pm,液氢的密度为0.0708 g·cm-3。若以材料中氢的密度与液态氢密度之比定义储氢材料的储氢能力,则Mg2NiH4 的储氢能力是液氢的___ 倍(列出计算式即可)。
(1)基态Ni原子的核外电子排布式为
(2)NaBH4中H为-1价,Na、B、H电负性由大到小的顺序是
(3)B2H6和NH3化合可以生成H3B-NH3,H3B-NH3加热时发生反应:H3B-NH3=BN+3H2,缓慢释放出H2。BN有类似于石墨的结构,B2H6、NH3和BN的沸点由高到低的顺序为
(4)X-射线衍射分析表明,Mg2NiH4 的立方晶胞的面心和顶点均被Ni原子占据,所有Mg原子的Ni配位数都相等。则Mg原子填入由Ni原子形成的
(5)已知Mg2NiH4 晶体的晶胞参数为646.5 pm,液氢的密度为0.0708 g·cm-3。若以材料中氢的密度与液态氢密度之比定义储氢材料的储氢能力,则Mg2NiH4 的储氢能力是液氢的

您最近一年使用:0次
名校
解题方法
6 . 硼及其化合物在新材料、工农业生产等方面用途很广。请回答下列问题:
(1)写出与B元素同主族的Ga元素的基态原子核外电子排布式:________ 。
(2)立方氮化硼(BN)可利用人工方法在高温高压条件下合成,属于超硬材料。同属原子晶体的氮化硼比晶体硅具有更高的硬度和耐热性的原因是__________ 。
(3)BF3分子中中心原子的杂化轨道类型是____ 。又知若有d轨道参与杂化,能大大提高中心原子的成键能力,分析BF3、SiF4水解的产物中, 除了相应的酸外,前者生成BF4-而后者生成SiF62-的原因:_______________ 。
(4)NaBH4被认为是有机化学中的“万能还原剂”,NaBH4的电子式为_________ ,其中三种元素的电负性由大到小的顺序是_______________ 。
(5)自然界中含硼元素的钠盐是一种天然矿藏,其化学式写作 Na2B4O7•10H2O,实际上它的结构单元是由两个H3BO3和两个B(OH)4]-(合而成的双六元环,应该写成 Na2[B4O5(OH)4]•8H2O,其结构如图所示,它的阴离子可形成链状结构,则该晶体中不存在的作用力是______________ (填字母)。

A.离子键 B.共价键 C.氢键 D.金属键 E.范德华力
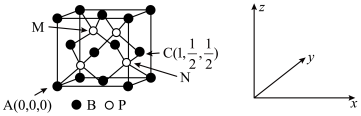
(6)磷化硼(BP)可作为金属表面的保护薄膜,其晶胞如图所示,在BP晶胞中P占据的是硼原子堆积的_____ (填“立方体”“正四面体”或“正八面体”)空隙。建立如图所示坐标系,可得晶胞中A、C处原子的分数坐标,则N处的P原子分数坐标为______ 。若晶胞中硼原子和磷原子之间的最近核间距为a pm,则晶胞边长为____________ cm。
(1)写出与B元素同主族的Ga元素的基态原子核外电子排布式:
(2)立方氮化硼(BN)可利用人工方法在高温高压条件下合成,属于超硬材料。同属原子晶体的氮化硼比晶体硅具有更高的硬度和耐热性的原因是
(3)BF3分子中中心原子的杂化轨道类型是
(4)NaBH4被认为是有机化学中的“万能还原剂”,NaBH4的电子式为
(5)自然界中含硼元素的钠盐是一种天然矿藏,其化学式写作 Na2B4O7•10H2O,实际上它的结构单元是由两个H3BO3和两个B(OH)4]-(合而成的双六元环,应该写成 Na2[B4O5(OH)4]•8H2O,其结构如图所示,它的阴离子可形成链状结构,则该晶体中不存在的作用力是

A.离子键 B.共价键 C.氢键 D.金属键 E.范德华力
(6)磷化硼(BP)可作为金属表面的保护薄膜,其晶胞如图所示,在BP晶胞中P占据的是硼原子堆积的

您最近一年使用:0次
2020-04-09更新
|
197次组卷
|
2卷引用:重庆巴蜀中学高2020届高三下学期3月月月考理综化学试题
解题方法
7 . 化学作为一门基础自然科学,在材料科学、生命科学、能源科学等诸多领域发挥着重要作用,其中铁和铜是两种应用广泛的元素。
(1)基态铁原子的价电子轨道表达式为_____ 。
(2)磁性材料铁氧体在制备时常加入 CH3COONa、尿素[CO(NH2)2]等碱性物质。尿素分子中所含元素的电负性由小到大的顺序是_____ ,1mol 尿素分子中含有的 σ 键数目为_____ 。 CH3COONa 中碳原子的杂化类型为_________ 。
(3)Fe(CO)5又名羰基铁,常温下为黄色油状液体,则 Fe(CO)5的晶体类型是_____ ,写出与CO互为等电子体的分子的电子式_____ (任写一种)。
(4)CuO在高温时分解为 O2和 Cu2O,请从阳离子的结构来说明在高温时,Cu2O比 CuO更稳定的原因_____ 。
(5)磷青铜是含少量锡、磷的铜合金,某磷青铜晶胞结构如图所示:
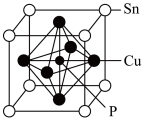
①其化学式为_____ 。
②若晶体密度为 8.82g/cm3,则最近的 Cu原子核间距为_____ pm(用含 NA的代数式表示)。
(1)基态铁原子的价电子轨道表达式为
(2)磁性材料铁氧体在制备时常加入 CH3COONa、尿素[CO(NH2)2]等碱性物质。尿素分子中所含元素的电负性由小到大的顺序是
(3)Fe(CO)5又名羰基铁,常温下为黄色油状液体,则 Fe(CO)5的晶体类型是
(4)CuO在高温时分解为 O2和 Cu2O,请从阳离子的结构来说明在高温时,Cu2O比 CuO更稳定的原因
(5)磷青铜是含少量锡、磷的铜合金,某磷青铜晶胞结构如图所示:

①其化学式为
②若晶体密度为 8.82g/cm3,则最近的 Cu原子核间距为
您最近一年使用:0次
名校
解题方法
8 . 碳和硫是高中化学学习的两种重要非金属元素
(1)下列C原子的电子排布式表达的状态中能量最高的是_____ 。
A 1s22s22p2 B.1s22s22px12py1 C.1s22s22px12pz1 D.1s22s12px12py12pz1_____ 。
(4)已知CS2晶体结构类似于干冰。CS2晶体中与每个CS2分子距离最近且等距的CS2分子有_____ 个。推测CS2晶体密度与冰的晶体密度较大的为_____ 。可能的原因是_____ 。又知CS2晶体中晶胞参数是apm,NA表示阿伏加德罗常数的值,晶体密度为_____ g/cm3(用含a、NA等符号的表达式表示)。
(5)Na2S是高子晶体,其晶格能可通过图的Born﹣Haber循环计算得到。_____ kJ/mol,Na2S的晶格能为_____ kJ/mol。(用图中给出的符号作答)
(1)下列C原子的电子排布式表达的状态中能量最高的是
A 1s22s22p2 B.1s22s22px12py1 C.1s22s22px12pz1 D.1s22s12px12py12pz1
(2)硫有一种结构为 的分子(灰球代表硫原子)。其中硫原子杂化方式为
的分子(灰球代表硫原子)。其中硫原子杂化方式为
(4)已知CS2晶体结构类似于干冰。CS2晶体中与每个CS2分子距离最近且等距的CS2分子有
(5)Na2S是高子晶体,其晶格能可通过图的Born﹣Haber循环计算得到。

您最近一年使用:0次
2020-03-08更新
|
167次组卷
|
3卷引用:重庆市乌江新高考协作体2023-2024学年高二下学期5月期中考试化学试题
重庆市乌江新高考协作体2023-2024学年高二下学期5月期中考试化学试题辽宁省实验中学、大连八中、大连二十四中、鞍山一中、东北育才学校2018-2019学年高三上学期末考试化学试题(已下线)考点14 物质结构与性质(选考)-2020年高考化学命题预测与模拟试题分类精编
名校
解题方法
9 . 本题涉及部分铜及其化合物的相关结构问题的考查,请回答下列问题。
(1)写出基态Cu2+的核外电子排布式:________ 。Cu的同周期元素中,与铜原子最外层电子数相等的元素原子还有___________ (用元素符号表示)。
(2)从原子结构角度分析高温Cu2O比CuO稳定的原因是___________ 。
(3)[Cu(NH3)2]Ac可用于合成氨工业中的铜洗工序,除去进入合成塔前混合气中的CO(CO能使催化剂中毒)。
①Ac表示CH3COO-,Ac中碳原子的杂化方式为________ 。
②[Cu(NH3)2]Ac能够结合CO的原因是________ 。
(4)铜原子与氯原子形成化合物的晶胞如图所示(黑球代表铜原子,白球表示氯原子)。

①已知铜和氯的电负性分别为1.9和3.0,则铜与氯形成的化合物属于________ 填(“离子”或“共价”)化合物。
②以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,例如图中原子1的坐标为( ,
, ,1),则原子2和3的坐标分别为
,1),则原子2和3的坐标分别为___________ 、__________ 。
③已知该晶体的密度为ρg/cm3,阿伏加 德罗常数为NA,则该晶体中铜原子和氯原子的最短距离为_____________ pm(只写计算式)。
(1)写出基态Cu2+的核外电子排布式:
(2)从原子结构角度分析高温Cu2O比CuO稳定的原因是
(3)[Cu(NH3)2]Ac可用于合成氨工业中的铜洗工序,除去进入合成塔前混合气中的CO(CO能使催化剂中毒)。
①Ac表示CH3COO-,Ac中碳原子的杂化方式为
②[Cu(NH3)2]Ac能够结合CO的原因是
(4)铜原子与氯原子形成化合物的晶胞如图所示(黑球代表铜原子,白球表示氯原子)。

①已知铜和氯的电负性分别为1.9和3.0,则铜与氯形成的化合物属于
②以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,例如图中原子1的坐标为(
 ,
, ,1),则原子2和3的坐标分别为
,1),则原子2和3的坐标分别为③已知该晶体的密度为ρg/cm3,阿伏加 德罗常数为NA,则该晶体中铜原子和氯原子的最短距离为
您最近一年使用:0次
名校
解题方法
10 . 离子液体是一类具有很高应用价值的绿色溶剂和催化剂,其中的EMIM+由H、C、N三种元素组成,结构如图甲所示。回答下列问题:
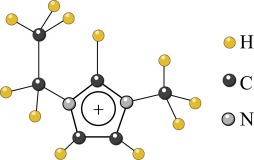
甲
(1)碳原子价层电子的轨道表达式为_____ ,基态碳原子中,核外电子占据的最高能级的电子云轮廓图为_____ 形。
(2)根据价层电子对互斥理论,NH3、NO3-、NO2-中,中心原子价层电子对数不同于其他两种粒子的是_____ 。NH3比PH3的沸点高,原因是_____ 。氮元素的第一电离能比同周期相邻元素都大的原因是_____ 。
(3)EMIM+中,碳原子的杂化轨道类型为_____ 。
(4)立方氮化硼硬度仅次于金刚石,但热稳定性远高于金刚石,其晶胞结构如图所示。立方氮化硼属于______ 晶体,其中硼原子的配位数为_____ 。已知:立方氮化硼密度为dg/cm3,B原子半径为xpm,N原子半径为ypm,阿伏加 德罗常数的值为NA,则该晶胞中原子的空间利用率为_____ (列出化简后的计算式)。


甲
(1)碳原子价层电子的轨道表达式为
(2)根据价层电子对互斥理论,NH3、NO3-、NO2-中,中心原子价层电子对数不同于其他两种粒子的是
(3)EMIM+中,碳原子的杂化轨道类型为
(4)立方氮化硼硬度仅次于金刚石,但热稳定性远高于金刚石,其晶胞结构如图所示。立方氮化硼属于

您最近一年使用:0次



