名校
1 . 2-TS是锂离子电池的电解质溶液添加剂,由原子序数依次增大的五种短周期主族元素X、Y、Z、T、W组成,结构如图所示。T和W位于同主族,基态Y原子核外每个能级上的电子数相等,X、Y、Z的原子序数之和等于14。下列叙述正确的是
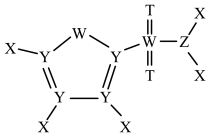
| A.第一电离能:T>Z>W | B.最高价氧化物对应水化物的酸性:Z<Y |
| C.最简单氢化物的键角:Y>T>W | D.X分别与Y、Z、T均可形成非极性分子 |
您最近一年使用:0次
2024-05-07更新
|
121次组卷
|
2卷引用:名校期末好题汇编-分子结构与性质(选择题)
名校
2 . 下列说法中正确的是
| A.NO2、SO2、BF3、NCl3分子中每原子的最外层电子都满足了8电子稳定结构 |
| B.P4和CH4都是正四面体形分子且键角都为109°28′ |
C. 中硼原子的杂化类型与苯中碳原子的杂化类型不同 中硼原子的杂化类型与苯中碳原子的杂化类型不同 |
| D.NH3分子中有一对未成键的孤电子对,它对成键电子的排斥作用较强 |
您最近一年使用:0次
2024-04-09更新
|
94次组卷
|
2卷引用:江西省南昌市第十九中学2023-2024学年高二上学期期末考试化学试卷
3 . 填空
(1)基态铜原子价层电子排布图为______ ﹔已知Cu第一电离能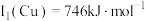 ,Fe第一电离能
,Fe第一电离能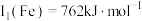 ,则
,则
______  (填“>”、“=”或“<”),其主要原因是
(填“>”、“=”或“<”),其主要原因是______ ;
(2) 和
和 的中心原子的杂化轨道类型分别为
的中心原子的杂化轨道类型分别为______ ,试判断 和
和 的键角大小关系:
的键角大小关系:
______  ,说明原因:
,说明原因:______
(3)比较 和
和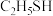 的酸性:
的酸性:
______ 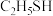 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
(1)基态铜原子价层电子排布图为
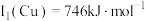 ,Fe第一电离能
,Fe第一电离能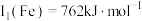 ,则
,则
 (填“>”、“=”或“<”),其主要原因是
(填“>”、“=”或“<”),其主要原因是(2)
 和
和 的中心原子的杂化轨道类型分别为
的中心原子的杂化轨道类型分别为 和
和 的键角大小关系:
的键角大小关系:
 ,说明原因:
,说明原因:(3)比较
 和
和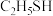 的酸性:
的酸性:
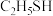 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
您最近一年使用:0次
2024-04-03更新
|
344次组卷
|
2卷引用:浙江省杭州市源清中学2023-2024学年高二上学期期末考试化学试题
名校
解题方法
4 . Ⅰ.8−羟基喹啉( )被广泛用作
)被广泛用作 等金属离子的络合剂和萃取剂,也是重要的医药中间体。回答下列问题:
等金属离子的络合剂和萃取剂,也是重要的医药中间体。回答下列问题:
(1)8−羟基喹啉的熔点明显低于7−羟基喹啉(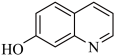 )、6−羟基喹啉(
)、6−羟基喹啉(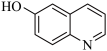 )的熔点的原因是
)的熔点的原因是___________ 。
(2)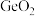 不能形成类似
不能形成类似 分子中的
分子中的 键,原因是
键,原因是___________ 。
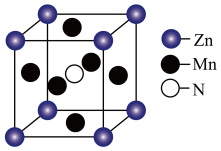
(3)某种含 特殊材料的晶胞结构如图所示,若该晶体的密度为
特殊材料的晶胞结构如图所示,若该晶体的密度为 ,则晶体中相邻N之间的最短距离为
,则晶体中相邻N之间的最短距离为___________  (列出计算式,
(列出计算式, 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
Ⅱ. 等氟化物可以做光导纤维材料,一定条件下,某
等氟化物可以做光导纤维材料,一定条件下,某 的晶体结构如下图。
的晶体结构如下图。

(4)与 距离最近且相等的
距离最近且相等的 有
有___________ 个,与 距离最近且相等的F-有
距离最近且相等的F-有___________ 个。
(5) 表示阿伏加德罗常数的值。
表示阿伏加德罗常数的值。 晶胞为正方体,边长为
晶胞为正方体,边长为 ,则晶体的摩尔体积
,则晶体的摩尔体积
___________  。(
。( )
)
(6)Cu-Mn-Al合金的晶胞如图1所示,该晶胞可视为Mn、Al位于Cu形成的立方体体心位置,如图2是沿立方格子对角面取得的截图。
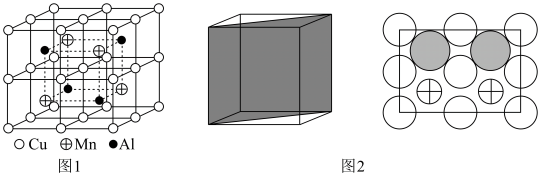
将Cu-Mn-Al合金晶胞沿棱投影于垂直面的是___________。(填字母序号)
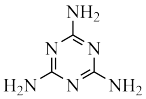
(7)一种类石墨的聚合物g﹣C3N4可由三聚氰胺制得。三聚氰胺分子不溶于冷水,溶于热水,主要原因是___________ 。
 )被广泛用作
)被广泛用作 等金属离子的络合剂和萃取剂,也是重要的医药中间体。回答下列问题:
等金属离子的络合剂和萃取剂,也是重要的医药中间体。回答下列问题:(1)8−羟基喹啉的熔点明显低于7−羟基喹啉(
 )、6−羟基喹啉(
)、6−羟基喹啉( )的熔点的原因是
)的熔点的原因是(2)
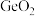 不能形成类似
不能形成类似 分子中的
分子中的 键,原因是
键,原因是(3)某种含
 特殊材料的晶胞结构如图所示,若该晶体的密度为
特殊材料的晶胞结构如图所示,若该晶体的密度为 ,则晶体中相邻N之间的最短距离为
,则晶体中相邻N之间的最短距离为 (列出计算式,
(列出计算式, 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
Ⅱ.
 等氟化物可以做光导纤维材料,一定条件下,某
等氟化物可以做光导纤维材料,一定条件下,某 的晶体结构如下图。
的晶体结构如下图。
(4)与
 距离最近且相等的
距离最近且相等的 有
有 距离最近且相等的F-有
距离最近且相等的F-有(5)
 表示阿伏加德罗常数的值。
表示阿伏加德罗常数的值。 晶胞为正方体,边长为
晶胞为正方体,边长为 ,则晶体的摩尔体积
,则晶体的摩尔体积
 。(
。( )
)(6)Cu-Mn-Al合金的晶胞如图1所示,该晶胞可视为Mn、Al位于Cu形成的立方体体心位置,如图2是沿立方格子对角面取得的截图。

将Cu-Mn-Al合金晶胞沿棱投影于垂直面的是___________。(填字母序号)
A.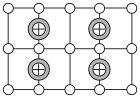 | B.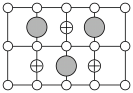 |
C. | D.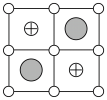 |
(7)一种类石墨的聚合物g﹣C3N4可由三聚氰胺制得。三聚氰胺分子不溶于冷水,溶于热水,主要原因是

您最近一年使用:0次
名校
解题方法
5 . 锂离子电池的开发与应用是新能源汽车走向实用的关键。
(1)LiFePO4是新型锂离子电池的正极材料,基态铁原子的价层电子排布图为___________ 。LiFePO4的结构如图A所示,锂离子电池充放电过程伴随A和B相互转化,则A→B为___________ 过程(填“充电”或“放电”)。 )。
)。
① 的键角
的键角___________ (填“等于”大于”或“小于”) 的键角。
的键角。 的VSEPR模型为
的VSEPR模型为___________ 。
②Htrz分子为平面结构,N原子的杂化轨道类型为___________ ,连接氢原子的氮原子在形成Htrz分子中的大π键时提供的电子数是___________ 。
(3)Be和B的第一电离能I1(Be)>I1(B)的原因是___________ 。
(4)LiAsF6、LiPF6、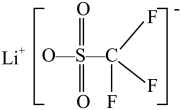 等物质常用作电池电解液的溶质,HOSO2CF3和HOSO2CH3在水溶液中酸性较强的是HOSO2CF3,理由是
等物质常用作电池电解液的溶质,HOSO2CF3和HOSO2CH3在水溶液中酸性较强的是HOSO2CF3,理由是___________ 。
(1)LiFePO4是新型锂离子电池的正极材料,基态铁原子的价层电子排布图为
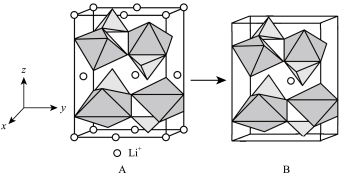
 )。
)。①
 的键角
的键角 的键角。
的键角。 的VSEPR模型为
的VSEPR模型为②Htrz分子为平面结构,N原子的杂化轨道类型为
(3)Be和B的第一电离能I1(Be)>I1(B)的原因是
(4)LiAsF6、LiPF6、
 等物质常用作电池电解液的溶质,HOSO2CF3和HOSO2CH3在水溶液中酸性较强的是HOSO2CF3,理由是
等物质常用作电池电解液的溶质,HOSO2CF3和HOSO2CH3在水溶液中酸性较强的是HOSO2CF3,理由是
您最近一年使用:0次
2024-03-16更新
|
295次组卷
|
2卷引用:河北省石家庄二中教育集团2023-2024学年高二年级上学期期末考试化学试题
名校
解题方法
6 . 下列关于分子的结构或性质的解释正确的是
| 选项 | 物质的结构或性质 | 解释 |
| A | 键角: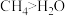 |  的键长大于 的键长大于 的键长 的键长 |
| B | 用乙酸乙酯而不用水溶解油漆 | 乙酸乙酯与油漆中的成分极性都较小,利用了相似相溶原理,而水分子极性较大,对油漆溶解效果不好 |
| C | 酸性: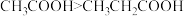 | 烃基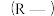 越长,推电子效应越小,羧基中羟基的极性越大,羧酸的酸性越弱 越长,推电子效应越小,羧基中羟基的极性越大,羧酸的酸性越弱 |
| D | 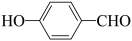 的沸点高于 的沸点高于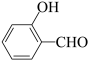 | 因为 分子间的范德华力大于 分子间的范德华力大于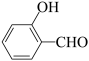 分子间的范德华力 分子间的范德华力 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-03-09更新
|
588次组卷
|
3卷引用:湖南省长沙市长郡中学2023-2024学年高二上学期期末考试化学试题
名校
解题方法
7 . 下列说法正确的是
A.酸性: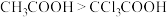 |
| B.HF酸电离平衡正向移动时,其电离程度一定增大 |
C.甲基是推电子基团,所以结合氢离子的能力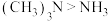 |
D.分子: ,键角: ,键角: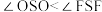 |
您最近一年使用:0次
名校
8 . 下列结论正确,且能用键能解释的是
| 化学键 |  |  |  |  |  |  |
键能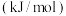 | 411 | 318 | 799 | 358 | 346 | 222 |
A.键角: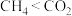 | B.键长: |
C.稳定性: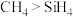 | D.电负性: |
您最近一年使用:0次
2024-03-05更新
|
488次组卷
|
4卷引用:2.1.2键参数——键能、键长与键角
(已下线)2.1.2键参数——键能、键长与键角(已下线)2.1.2 键参数——键能、键长与键角(巩固)四川省成都市成华区某校2023-2024学年高二下学期4月月考化学试题浙江省湖州市德清县求是高级中学有限公司2023-2024学年高二上学期期末考试化学试题
解题方法
9 . 镍能形成多种配合物如正四面体形的 和平面正方形的
和平面正方形的 、正八面体形的
、正八面体形的 等,下列说法正确的是
等,下列说法正确的是
 和平面正方形的
和平面正方形的 、正八面体形的
、正八面体形的 等,下列说法正确的是
等,下列说法正确的是A. 中的配位原子是氧原子 中的配位原子是氧原子 |
B. 中Ni、C、N不可能处在同一直线上 中Ni、C、N不可能处在同一直线上 |
C. 中 中 键角比107.3°小 键角比107.3°小 |
D. 和 和 中均有d轨道参与杂化 中均有d轨道参与杂化 |
您最近一年使用:0次
名校
解题方法
10 . 物质结构决定物质性质。下列性质差异与结构因素匹配错误的是
| 选项 | 性质差异 | 结构因素 |
| A | 沸点:正戊烷(36.1℃)高于新戊烷(9.5℃) | 范德华力大小 |
| B | 沸点:对羟基苯甲醛>邻羟基苯甲醛 | 氢键类型 |
| C | 溶解性:蔗糖在水中的溶解度大于萘在水中的溶解度 | 相似相溶 |
| D | 稳定性:H2O的分解温度(3000℃)远大于H2S(900℃) | 有无氢键 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



