名校
解题方法
1 . 铬是人体内微量元素之一,是重要的血糖调节剂。
(1)铬在元素周期表中的位置为___________ ,其基态原子核外电子占据的原子轨道数为___________ 。
(2)已知 半径小,正电场较强,容易与
半径小,正电场较强,容易与 、
、 、
、 等分子或离子形成多种配合物,
等分子或离子形成多种配合物, 是其中的一种。
是其中的一种。
①该配合物中提供孤电子对形成配位键的原子是___________ 。
②配体中中心原子的杂化方式为___________ (填字母)。
a. b.
b. c.sp d.
c.sp d.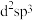
③该物质中, 的键角比独立存在的气态氨气分子中键角略大,其原因是
的键角比独立存在的气态氨气分子中键角略大,其原因是___________ 。
(3)钛铬合金是一种高温结构材料,第二电离能
___________ (填“ ”或“
”或“ ”)
”)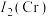 ,原因是
,原因是___________ 。
(4)铬的一种氮化物晶体立方晶胞结构如图所示,A点分数坐标为 ,则B点分数坐标为
,则B点分数坐标为___________ ,已知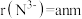 ,
,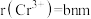 ,则AB间距离为
,则AB间距离为___________ nm。
(1)铬在元素周期表中的位置为
(2)已知
 半径小,正电场较强,容易与
半径小,正电场较强,容易与 、
、 、
、 等分子或离子形成多种配合物,
等分子或离子形成多种配合物, 是其中的一种。
是其中的一种。①该配合物中提供孤电子对形成配位键的原子是
②配体中中心原子的杂化方式为
a.
 b.
b. c.sp d.
c.sp d.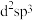
③该物质中,
 的键角比独立存在的气态氨气分子中键角略大,其原因是
的键角比独立存在的气态氨气分子中键角略大,其原因是(3)钛铬合金是一种高温结构材料,第二电离能

 ”或“
”或“ ”)
”)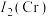 ,原因是
,原因是(4)铬的一种氮化物晶体立方晶胞结构如图所示,A点分数坐标为
 ,则B点分数坐标为
,则B点分数坐标为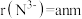 ,
,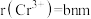 ,则AB间距离为
,则AB间距离为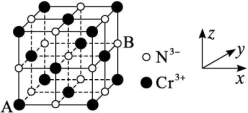
您最近半年使用:0次
名校
解题方法
2 . 现有五种元素A、B、C、D、E,其中A、B、C为三个不同周期的短周期元素,E为第四周期元素。请根据下列相关信息,回答下列问题:
(1)C基态原子中能量最高的电子,其电子云在空间有___________ 个伸展方向,C简单离子核外有___________ 种运动状态不同的电子。
(2)A2B2难溶于CS2,简要说明理由:______________ 。
(3)ED3分子的VSEPR模型名称为____________ ,空间构型为____________ 。
(4)下列气态分子BCl3、CCl4、H2O和BeCl2中,其键角由大到小的顺序为_____________ 。
(5)键的极性对物质的化学性质有重要影响。已知一些常见电子基团的吸电子效应的强度:RCO﹣>﹣F>﹣Cl>﹣Br>﹣I>﹣C≡CH>﹣C6H5>﹣H,则下列物质酸性由强到弱的顺序是___________ (填序号)。
A.CH3COOH B.ClCH2COOH C.HC≡CCH2COOH D.C6H5CH2COOH
元素 | 相关信息 |
A | 核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
B | 原子核外p电子数与s电子数相等 |
C | 基态原子的价电子排布为nsn-1npn+1 |
D | 能层数与C相同,且电负性比C大 |
E | 元素的主族序数与周期数的差为1,且第一电离能比同周期相邻两种元素都大 |
(2)A2B2难溶于CS2,简要说明理由:
(3)ED3分子的VSEPR模型名称为
(4)下列气态分子BCl3、CCl4、H2O和BeCl2中,其键角由大到小的顺序为
(5)键的极性对物质的化学性质有重要影响。已知一些常见电子基团的吸电子效应的强度:RCO﹣>﹣F>﹣Cl>﹣Br>﹣I>﹣C≡CH>﹣C6H5>﹣H,则下列物质酸性由强到弱的顺序是
A.CH3COOH B.ClCH2COOH C.HC≡CCH2COOH D.C6H5CH2COOH
您最近半年使用:0次
名校
3 . 回答下列问题:
(1)第四周期未成对电子数最多的元素是___________ (填元素符号),该元素基态原子核外电子共有___________ 种不同能量的电子。
(2)丁二酮(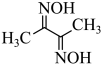 )中涉及元素的电负性由大到小的顺序为
)中涉及元素的电负性由大到小的顺序为___________ ,该物质中,σ键与π键数目之比为___________ 。
(3)比较键角大小:AsO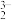
___________ AsO (填>、<或=)。
(填>、<或=)。
(4)铜的下列状态中,失去最外层一个电子所需能量最小的是___________。
(1)第四周期未成对电子数最多的元素是
(2)丁二酮(
 )中涉及元素的电负性由大到小的顺序为
)中涉及元素的电负性由大到小的顺序为(3)比较键角大小:AsO
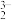
 (填>、<或=)。
(填>、<或=)。(4)铜的下列状态中,失去最外层一个电子所需能量最小的是___________。
| A.[Ar]3d104p1 | B.[Ar]3d10 | C.[Ar]3d94s1 | D.[Ar]3d104s1 |
您最近半年使用:0次
名校
解题方法
4 . 碳族元素的单质和化合物在化工、医药、材料等领域有着广泛的应用。
(1)锗是优良的半导体材料,基态Ge原子中,最高能级电子云轮廓图的名称为_______ 。
(2)碳可形成CO、CO2、H2CO3等多种无机化合物。
①在反应CO转化成CO2的过程中,下列说法正确的是_______ 。
A.每个分子中孤对电子数增多 B.分子的极性不变
C.C原子的杂化方式未改变 D.分子的键角变小
②干冰和冰是两种常见的分子晶体,晶体中的空间利用率:干冰_______ 冰(填“>”“<”或“=”);写出一种与CO2互为等电子体的阴离子_______ 。
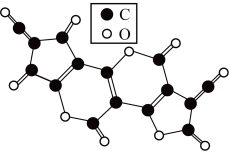
③X是碳的一种氧化物,X的五聚合体结构如图所示。X分子中每个原子都满足最外层8电子结构,X分子的电子式为_______ 。
(3)碳和硅的有关化学键键能如表所示:
硅与碳同族,也有系列氢化物,但硅烷在种类和数量上都远不如烷烃多,原因是_______ 。
(4)科学家们发现,许多碳和硅构成的晶体晶胞与ZnS晶胞结构一样,可以利用ZnS晶胞进行类比探究,六方硫化锌(纤锌矿型)的平行六面体晶胞(上下底面均为正方形)如图所示。

①晶体中正负离子的配位数之比为_______ 。
②已知每个Zn2+与其周围最近的S2-之间的距离都相等,以晶胞参数为单位长度建立坐标系,若A点坐标为(0,0,0),B点坐标为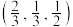 ,C点坐标为(0,0,u),则D点坐标为
,C点坐标为(0,0,u),则D点坐标为_______ 。
(1)锗是优良的半导体材料,基态Ge原子中,最高能级电子云轮廓图的名称为
(2)碳可形成CO、CO2、H2CO3等多种无机化合物。
①在反应CO转化成CO2的过程中,下列说法正确的是
A.每个分子中孤对电子数增多 B.分子的极性不变
C.C原子的杂化方式未改变 D.分子的键角变小
②干冰和冰是两种常见的分子晶体,晶体中的空间利用率:干冰
③X是碳的一种氧化物,X的五聚合体结构如图所示。X分子中每个原子都满足最外层8电子结构,X分子的电子式为

(3)碳和硅的有关化学键键能如表所示:
| 化学键 | C—C | C—H | C—O | Si—Si | Si—H | Si—O |
| 键能/kJ·mol-1 | 356 | 413 | 336 | 226 | 318 | 452 |
(4)科学家们发现,许多碳和硅构成的晶体晶胞与ZnS晶胞结构一样,可以利用ZnS晶胞进行类比探究,六方硫化锌(纤锌矿型)的平行六面体晶胞(上下底面均为正方形)如图所示。

①晶体中正负离子的配位数之比为
②已知每个Zn2+与其周围最近的S2-之间的距离都相等,以晶胞参数为单位长度建立坐标系,若A点坐标为(0,0,0),B点坐标为
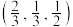 ,C点坐标为(0,0,u),则D点坐标为
,C点坐标为(0,0,u),则D点坐标为
您最近半年使用:0次
名校
解题方法
5 . “天问一号”着陆火星,“嫦娥五号”采回月壤,探索宇宙离不开化学。镍铼合金是制造喷气发动机的燃烧室、涡轮叶片及排气喷嘴的重要材料。75号元素铼Re,熔点仅次于钨,是稀有金属之一、回答:
(1)镍基态原子有___________ 种不同空间运动状态的电子,第四周期与基态镍原子单电子数相同的元素有___________ 种(不含镍元素)。
(2)Ni2+与丁二酮肟可形成鲜红色的二丁二酮肟合镍(M= 289 g·mol-1),结构如下图所示。0.2mol二丁二酮肟合镍分子内含有σ键___________ mol,碳碳键是由___________ 轨道重叠形成的。

a.sp3和sp2 b.sp2和 sp2 c.sp2和p d.sp3和p
(3) 中心原子为
中心原子为 ,
, 中心原子为
中心原子为 ,二者均为
,二者均为 形结构,但
形结构,但 中存在大
中存在大 键
键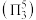 。
。 键角
键角___________  键角(填“>”“ <”或“=”)。比较
键角(填“>”“ <”或“=”)。比较 与
与 中
中 键的键长并说明原因
键的键长并说明原因___________ 。
(4)人类合成的第一个稀有气体化合物是XeF+PtF ,PtF
,PtF 中的键角有90°和180°两种。下列关于该化合物的说法中正确的是___________。
中的键角有90°和180°两种。下列关于该化合物的说法中正确的是___________。
(5)三氧化铼晶胞如图所示,摩尔质量为Mg/mol,晶胞密度为bg/cm3,铼原子填在氧原子围成的___________ (填“四面体”“立方体"或“八面体”)空隙中,该晶胞的空间利用率为___________ (铼的原子半径为rRepm,氧原子半径为rOpm,列出计算式)。
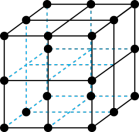
(6)Ga、Li和O三种原子形成的一种晶体基片在二极管中有重要用途。其四方晶胞结构如图所示:
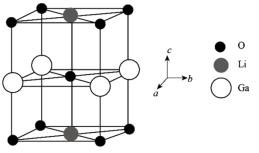
①上述晶胞沿着a轴的投影图为___________ (填字母)。
A. B.
B.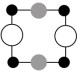 C.
C.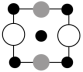
②用 表示阿伏加德罗常数的值,晶胞参数为
表示阿伏加德罗常数的值,晶胞参数为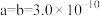 m,
m,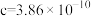 m,则其密度为
m,则其密度为___________  (列出计算式即可)。
(列出计算式即可)。
(1)镍基态原子有
(2)Ni2+与丁二酮肟可形成鲜红色的二丁二酮肟合镍(M= 289 g·mol-1),结构如下图所示。0.2mol二丁二酮肟合镍分子内含有σ键

a.sp3和sp2 b.sp2和 sp2 c.sp2和p d.sp3和p
(3)
 中心原子为
中心原子为 ,
, 中心原子为
中心原子为 ,二者均为
,二者均为 形结构,但
形结构,但 中存在大
中存在大 键
键 。
。 键角
键角 键角(填“>”“ <”或“=”)。比较
键角(填“>”“ <”或“=”)。比较 与
与 中
中 键的键长并说明原因
键的键长并说明原因(4)人类合成的第一个稀有气体化合物是XeF+PtF
 ,PtF
,PtF 中的键角有90°和180°两种。下列关于该化合物的说法中正确的是___________。
中的键角有90°和180°两种。下列关于该化合物的说法中正确的是___________。| A.熔化状态下不能导电 |
| B.XeF+中所有原子都满足8电子稳定结构 |
| C.用两个Cl替换F后,所得PtF4Cl2有两种结构 |
| D.含有离子键、极性键、非极性键和配位键 |
(6)Ga、Li和O三种原子形成的一种晶体基片在二极管中有重要用途。其四方晶胞结构如图所示:

①上述晶胞沿着a轴的投影图为
A.
 B.
B. C.
C.
②用
 表示阿伏加德罗常数的值,晶胞参数为
表示阿伏加德罗常数的值,晶胞参数为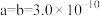 m,
m,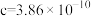 m,则其密度为
m,则其密度为 (列出计算式即可)。
(列出计算式即可)。
您最近半年使用:0次
名校
解题方法
6 . 2022年诺贝尔化学奖授子在发展点击化学方面做出贡献的科学家。点击化学的代表反应为CuCl催化的叠氮—炔基Husigen环加成反应,常用的无机试剂有 、
、 等。
等。
(1)铜在元素周期表中位置为___________ ,基态 的价电子排布式为
的价电子排布式为___________ 。
(2)N、S、O、F的第一电离能由大到小顺序为___________ 。
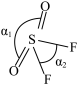
(3) 的分子结构如图所示,键角
的分子结构如图所示,键角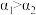 的原因主要是
的原因主要是___________ 。
(4) 是叠氮酸(
是叠氮酸( )的钠盐,
)的钠盐, 在常温下是液体,沸点相对较高,为308.8K,主要原因是
在常温下是液体,沸点相对较高,为308.8K,主要原因是___________ 。 分子的空间结构如图所示(图中键长单位为
分子的空间结构如图所示(图中键长单位为 )。
)。 、
、 和
和 的共价键键长分别为
的共价键键长分别为 、
、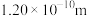 和
和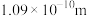 ;试画出
;试画出 分子的结构式
分子的结构式___________ 。
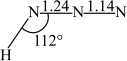
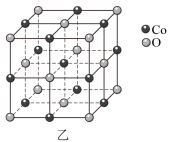
(5)一种钴的氧化物的晶胞结构如图乙所示,该氧化物中钴离子的配位数是___________ ,设 为阿伏伽德罗常数的值,晶胞参数为apm,该晶体的密度为
为阿伏伽德罗常数的值,晶胞参数为apm,该晶体的密度为___________  。
。
 、
、 等。
等。(1)铜在元素周期表中位置为
 的价电子排布式为
的价电子排布式为(2)N、S、O、F的第一电离能由大到小顺序为
(3)
 的分子结构如图所示,键角
的分子结构如图所示,键角 的原因主要是
的原因主要是
(4)
 是叠氮酸(
是叠氮酸( )的钠盐,
)的钠盐, 在常温下是液体,沸点相对较高,为308.8K,主要原因是
在常温下是液体,沸点相对较高,为308.8K,主要原因是 分子的空间结构如图所示(图中键长单位为
分子的空间结构如图所示(图中键长单位为 )。
)。 、
、 和
和 的共价键键长分别为
的共价键键长分别为 、
、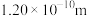 和
和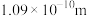 ;试画出
;试画出 分子的结构式
分子的结构式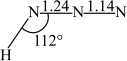
(5)一种钴的氧化物的晶胞结构如图乙所示,该氧化物中钴离子的配位数是
 为阿伏伽德罗常数的值,晶胞参数为apm,该晶体的密度为
为阿伏伽德罗常数的值,晶胞参数为apm,该晶体的密度为 。
。
您最近半年使用:0次
名校
解题方法
7 . 回答下列问题:
(1)NH3在水中的溶解度是常见气体中最大的。
①下列因素与NH3的水溶性没有关系的是___________ (填字母)。
a.NH3和H2O都是极性分子
b.NH3在水中易形成氢键
c.NH3溶于水建立了以下平衡: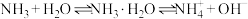
d.NH3是一种易液化的气体
②NH3溶于水时,大部分NH3与H2O通过氢键结合形成 。根据氨水的性质推知
。根据氨水的性质推知 的结构式为
的结构式为___________ 。(填字母)
a. b.
b.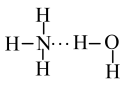 b. c.
b. c. d.
d.
(2)第ⅤA族氢化物RH3(NH3、PH3、AsH3)的某种性质随R的核电荷数的变化趋势如图所示。则Y轴可表示的氢化物(RH3)性质可能是___________。(填字母)

(3)AsH3的沸点(-62.5℃)比NH3的沸点(-33.5℃)低,原因是___________
(4)氮、磷、砷为同主族元素,As4O6的分子结构如图所示,其中As原子的杂化方式为___________ ,1 mol As4O6含有σ键的物质的量为___________ 。

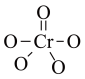
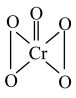
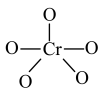
(5)CrO2Cl2常温下为深红色液体,能与CCl4、CS2等互溶,据此可判断CrO2Cl2是___________ (填“极性”或“非极性”)分子。
(6)NH 中的H-N-H的键角比 NH3中的H-N-H的键角大, 原因是
中的H-N-H的键角比 NH3中的H-N-H的键角大, 原因是___________ 。
(1)NH3在水中的溶解度是常见气体中最大的。
①下列因素与NH3的水溶性没有关系的是
a.NH3和H2O都是极性分子
b.NH3在水中易形成氢键
c.NH3溶于水建立了以下平衡:
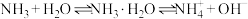
d.NH3是一种易液化的气体
②NH3溶于水时,大部分NH3与H2O通过氢键结合形成
 。根据氨水的性质推知
。根据氨水的性质推知 的结构式为
的结构式为a.
 b.
b.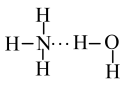 b. c.
b. c. d.
d.
(2)第ⅤA族氢化物RH3(NH3、PH3、AsH3)的某种性质随R的核电荷数的变化趋势如图所示。则Y轴可表示的氢化物(RH3)性质可能是___________。(填字母)

| A.稳定性 | B.沸点 | C.R-H键能 | D.分子间作用力 |
(4)氮、磷、砷为同主族元素,As4O6的分子结构如图所示,其中As原子的杂化方式为

(5)CrO2Cl2常温下为深红色液体,能与CCl4、CS2等互溶,据此可判断CrO2Cl2是
(6)NH
 中的H-N-H的键角比 NH3中的H-N-H的键角大, 原因是
中的H-N-H的键角比 NH3中的H-N-H的键角大, 原因是
您最近半年使用:0次
名校
解题方法
8 . 我国科学家研究发现 (
(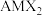 家族成员之一,A为一价金属,M为三价金属,X为氧族元素)在室温下具有超离子行为。回答下列问题:
家族成员之一,A为一价金属,M为三价金属,X为氧族元素)在室温下具有超离子行为。回答下列问题:
(1)基态铬原子的电子排布式为_________ ;基态硫原子核外电子中含有_________ 个未成对电子。
(2)同周期元素Si、P、S的电负性由大到小的顺序为________________ (用元素符号表示),O、S为同主族元素, 的键角比
的键角比 大的原因是
大的原因是________________ 。
(3)硫元素能形成多种微粒如 、
、 、
、 、
、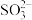 、
、 等,
等, 的中心原子的杂化类型为
的中心原子的杂化类型为_______________ , 的空间构型为
的空间构型为________ 。
(4)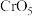 中
中 元素化合价为+6价,常温下呈蓝色,则其结构式可能为
元素化合价为+6价,常温下呈蓝色,则其结构式可能为________ (填标号)。
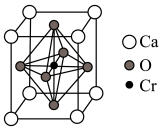
(5)某含铬化合物立方晶胞如图所示。该晶体的化学式为_____________ ;与Cr最近的氧原子的个数为________ ; 和
和 的最近距离为a nm,设
的最近距离为a nm,设 为阿伏加德罗常数的值,则该晶体密度
为阿伏加德罗常数的值,则该晶体密度______________  (填含a、
(填含a、 的表达式)。
的表达式)。
 (
(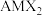 家族成员之一,A为一价金属,M为三价金属,X为氧族元素)在室温下具有超离子行为。回答下列问题:
家族成员之一,A为一价金属,M为三价金属,X为氧族元素)在室温下具有超离子行为。回答下列问题:(1)基态铬原子的电子排布式为
(2)同周期元素Si、P、S的电负性由大到小的顺序为
 的键角比
的键角比 大的原因是
大的原因是(3)硫元素能形成多种微粒如
 、
、 、
、 、
、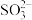 、
、 等,
等, 的中心原子的杂化类型为
的中心原子的杂化类型为 的空间构型为
的空间构型为(4)
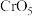 中
中 元素化合价为+6价,常温下呈蓝色,则其结构式可能为
元素化合价为+6价,常温下呈蓝色,则其结构式可能为
|
|
|
A | B | C |
 和
和 的最近距离为a nm,设
的最近距离为a nm,设 为阿伏加德罗常数的值,则该晶体密度
为阿伏加德罗常数的值,则该晶体密度 (填含a、
(填含a、 的表达式)。
的表达式)。
您最近半年使用:0次
名校
解题方法
9 . 氢能是一种极具发展潜力的清洁能源,下列物质都是具有广阔应用前景的储氢材料。按要求回答下列问题:
(1)氢化钠( )是一种常用的储氢剂,遇水后放出氢气并生成一种碱,该反应的还原剂的电子式为
)是一种常用的储氢剂,遇水后放出氢气并生成一种碱,该反应的还原剂的电子式为___________ 。
(2)钛系贮氢合金中的钛锰合金具成本低,吸氢量大,室温下易活化等优点,基态钛的价层电子排布式为___________ 。
(3) (氨硼烷)具有很高的储氢容量及相对低的放氢温度(
(氨硼烷)具有很高的储氢容量及相对低的放氢温度(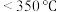 )而成为颇具潜力的化学储氢材料之一,它可通过环硼氮烷、
)而成为颇具潜力的化学储氢材料之一,它可通过环硼氮烷、 与
与 进行合成,则涉及的元素H、B、C、N、O电负性最大的是
进行合成,则涉及的元素H、B、C、N、O电负性最大的是___________ ,键角:
___________  (填“
(填“ ”或“
”或“ ”)。
”)。
(4)咔唑(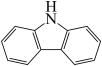 )是一种新型有机液体储氢材料,它的沸点比(
)是一种新型有机液体储氢材料,它的沸点比( )的高,其主要原因是
)的高,其主要原因是___________ 。
(5)氢气的安全贮存和运输是氢能应用的关键,铁镁合金是目前已发现的储氢密度最高的储氢材料之一,其晶胞结构如图所示。
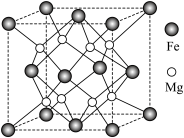
①距离 原子最近的
原子最近的 原子个数是
原子个数是___________ 。
②铁镁合金的化学式为___________ 。
③若该晶胞的晶胞边长为dnm,阿伏加德罗常数为NA,则该合金的密度为___________  。
。
④若该晶体储氢时, 分子在晶胞的体心和棱心位置,则含Mg 48g的该储氢合金可储存标准状况下
分子在晶胞的体心和棱心位置,则含Mg 48g的该储氢合金可储存标准状况下 的体积约为
的体积约为___________ L。
(1)氢化钠(
 )是一种常用的储氢剂,遇水后放出氢气并生成一种碱,该反应的还原剂的电子式为
)是一种常用的储氢剂,遇水后放出氢气并生成一种碱,该反应的还原剂的电子式为(2)钛系贮氢合金中的钛锰合金具成本低,吸氢量大,室温下易活化等优点,基态钛的价层电子排布式为
(3)
 (氨硼烷)具有很高的储氢容量及相对低的放氢温度(
(氨硼烷)具有很高的储氢容量及相对低的放氢温度(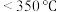 )而成为颇具潜力的化学储氢材料之一,它可通过环硼氮烷、
)而成为颇具潜力的化学储氢材料之一,它可通过环硼氮烷、 与
与 进行合成,则涉及的元素H、B、C、N、O电负性最大的是
进行合成,则涉及的元素H、B、C、N、O电负性最大的是
 (填“
(填“ ”或“
”或“ ”)。
”)。(4)咔唑(
 )是一种新型有机液体储氢材料,它的沸点比(
)是一种新型有机液体储氢材料,它的沸点比( )的高,其主要原因是
)的高,其主要原因是(5)氢气的安全贮存和运输是氢能应用的关键,铁镁合金是目前已发现的储氢密度最高的储氢材料之一,其晶胞结构如图所示。

①距离
 原子最近的
原子最近的 原子个数是
原子个数是②铁镁合金的化学式为
③若该晶胞的晶胞边长为dnm,阿伏加德罗常数为NA,则该合金的密度为
 。
。④若该晶体储氢时,
 分子在晶胞的体心和棱心位置,则含Mg 48g的该储氢合金可储存标准状况下
分子在晶胞的体心和棱心位置,则含Mg 48g的该储氢合金可储存标准状况下 的体积约为
的体积约为
您最近半年使用:0次
2023-05-25更新
|
337次组卷
|
3卷引用:宁夏石嘴山市第三中学2023-2024学年高三上学期第二次月考 化学试题
名校
10 . Ⅰ.图中硬质试管A中放入干燥洁净的细铜丝,烧杯中放入温水,试管B中放入甲醇,右方试管C中放入冷水。向B中不断鼓入空气,使甲醇蒸气和空气通过加热到红热程度的铜丝。

(1)反应后将试管C中的液体冷却,取出少量,加入到新制的Cu(OH)2悬浊液中,加热到沸腾可观察到现象是_______ 。
Ⅱ.硫酸铜可应用于电镀、颜料、医药、农药等方面。如图是探究铜与浓硫酸反应生成硫酸铜的实验装置图:
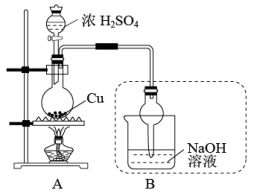
完成下列填空:
(2)图中盛放浓H2SO4的玻璃仪器名称是_______ 。写出图中装置B的作用: _______ 。
Ⅲ.[Cu(NH3)4]SO4·H2O晶体制备:
(3)制备过程:向盛有硫酸铜水溶液的试管里加入氨水,首先形成蓝色沉淀,继续添加氨水,沉淀溶解,得到深蓝色的透明溶液;再加入适量乙醇,将析出[Cu(NH3)4]SO4·H2O晶体。请解释加入乙醇后析出晶体的原因_______ 。
(4)写出沉淀溶解得透明溶液的离子方程式_______ 。
(5)1mol[Cu(NH3)4]SO4含有_______ molσ键。
(6)从结构的角度分析NH3比NF3的键角大的原因:_______ 。

(1)反应后将试管C中的液体冷却,取出少量,加入到新制的Cu(OH)2悬浊液中,加热到沸腾可观察到现象是
Ⅱ.硫酸铜可应用于电镀、颜料、医药、农药等方面。如图是探究铜与浓硫酸反应生成硫酸铜的实验装置图:

完成下列填空:
(2)图中盛放浓H2SO4的玻璃仪器名称是
Ⅲ.[Cu(NH3)4]SO4·H2O晶体制备:
(3)制备过程:向盛有硫酸铜水溶液的试管里加入氨水,首先形成蓝色沉淀,继续添加氨水,沉淀溶解,得到深蓝色的透明溶液;再加入适量乙醇,将析出[Cu(NH3)4]SO4·H2O晶体。请解释加入乙醇后析出晶体的原因
(4)写出沉淀溶解得透明溶液的离子方程式
(5)1mol[Cu(NH3)4]SO4含有
(6)从结构的角度分析NH3比NF3的键角大的原因:
您最近半年使用:0次