解题方法
1 . 下列有关物质结构与性质的比较正确的是
A.沸点: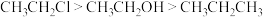 |
B.分子的极性: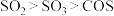 |
C.键角: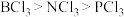 |
D.碱性强弱: |
您最近一年使用:0次
解题方法
2 . 卤族元素的化合物在科研和生产中有着重要的作用。请回答下列问题:
(1) (键角为180º)的中心Ⅰ原子价层电子对数为
(键角为180º)的中心Ⅰ原子价层电子对数为______ ;
______ (填“是”或“否”)具有极性;基态碘原子价电子排布式为______ 。
(2)物质磁性大小以磁矩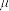 表示,
表示,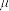 与未成对电子数之间的关系为:
与未成对电子数之间的关系为: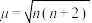 (n为未成对电子数)。配合物
(n为未成对电子数)。配合物 中配离子
中配离子 的
的 B.M(B.M磁矩单位),
B.M(B.M磁矩单位), 的杂化类型为
的杂化类型为______ 。
a. b.
b. c.
c.
配合物 中配离子
中配离子 的
的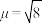 B.M,则配离子的空间构型为
B.M,则配离子的空间构型为______ 。
(3)在极高压强下,氯化钠可以和氯气化合生成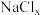 。
。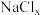 是立方系晶胞,结构如图所示,其中两个氯原子的坐标为
是立方系晶胞,结构如图所示,其中两个氯原子的坐标为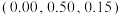 、
、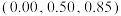 ,晶体的化学式为
,晶体的化学式为______ ;与Na距离最近的且相等的Cl有______ 个; 在晶体中键长为0.20nm,晶胞棱长为
在晶体中键长为0.20nm,晶胞棱长为______ nm(保留2位有效数字)。
(1)
 (键角为180º)的中心Ⅰ原子价层电子对数为
(键角为180º)的中心Ⅰ原子价层电子对数为
(2)物质磁性大小以磁矩
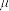 表示,
表示,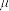 与未成对电子数之间的关系为:
与未成对电子数之间的关系为: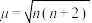 (n为未成对电子数)。配合物
(n为未成对电子数)。配合物 中配离子
中配离子 的
的 B.M(B.M磁矩单位),
B.M(B.M磁矩单位), 的杂化类型为
的杂化类型为a.
 b.
b. c.
c.
配合物
 中配离子
中配离子 的
的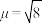 B.M,则配离子的空间构型为
B.M,则配离子的空间构型为(3)在极高压强下,氯化钠可以和氯气化合生成
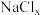 。
。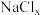 是立方系晶胞,结构如图所示,其中两个氯原子的坐标为
是立方系晶胞,结构如图所示,其中两个氯原子的坐标为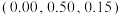 、
、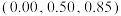 ,晶体的化学式为
,晶体的化学式为 在晶体中键长为0.20nm,晶胞棱长为
在晶体中键长为0.20nm,晶胞棱长为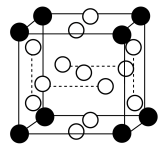
您最近一年使用:0次
名校
解题方法
3 . 下列说法正确的是
A. 分子的VSEPR模型: 分子的VSEPR模型: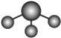 |
B.甲基是推电子基团,所以结合氢离子的能力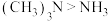 |
C.乙二胺( )的沸点比三甲胺 )的沸点比三甲胺 高的原因是乙二胺存在分子间氢键,三甲胺存在分子内氢键 高的原因是乙二胺存在分子间氢键,三甲胺存在分子内氢键 |
D.由铝原子核形成的下列三种微粒:a.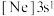 、b. 、b.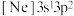 、c. 、c.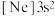 ,再失去一个电子所需最低能量由大到小的顺序是:c>a>b ,再失去一个电子所需最低能量由大到小的顺序是:c>a>b |
您最近一年使用:0次
名校
解题方法
4 . 检验微量砷的原理为 。
。 常温下为无色气体。下列说法正确的是
常温下为无色气体。下列说法正确的是
 。
。 常温下为无色气体。下列说法正确的是
常温下为无色气体。下列说法正确的是A.As的基态核外电子排布式为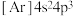 | B. 的空间构型为平面三角形 的空间构型为平面三角形 |
C.固态 属于共价晶体 属于共价晶体 | D. 既含离子键又含共价键 既含离子键又含共价键 |
您最近一年使用:0次
2023-06-02更新
|
1208次组卷
|
8卷引用:山东省济宁市第一中学2024届高三下学期4月份定时检测化学试题
山东省济宁市第一中学2024届高三下学期4月份定时检测化学试题江苏省扬州市2023届高三下学期三模化学试题江苏省淮安市2022-2023学年高二下学期6月期末考试化学试题(已下线)考点巩固卷06 物质结构与性质(4大考点55题)-2024年高考化学一轮复习考点通关卷(新高考通用)江苏省基地大联考2023-2024学年高三上学期第一次质量监测化学试题江苏省南京师范大学苏州实验学校2023-2024学年高三上学期零模考试热身练化学试题(已下线)热点17 分子结构与性质江苏省苏州市南京师范大学苏州实验学校2024届高三下学期二模考试化学(选修)试卷
名校
解题方法
5 . 下列图像正确的是
A. 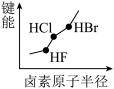 | B. 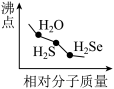 |
C. 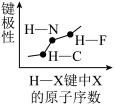 | D. 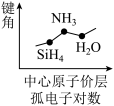 |
您最近一年使用:0次
2023-03-26更新
|
432次组卷
|
9卷引用:山东省济宁市兖州区2019-2020学年高二5月阶段性测试化学试题
山东省济宁市兖州区2019-2020学年高二5月阶段性测试化学试题江苏省泰州中学2020-2021学年高一下学期期末考试化学试题(已下线)第2章 章末综合测评B-2021-2022学年高二化学同步课时跟踪训练(人教版2019选择性必修2)河北省沧州市2021-2022学年高二下学期期末考试化学试题黑龙江省佳木斯市第十二中学2021-2022学年高二下学期期中考试化学试题河南省洛阳强基联盟2022-2023学年高二下学期3月联考化学试题湖北省宜昌市协作体2022-2023学年高二下学期期中考试化学试题湖南省岳阳市郡华学校2023-2024学年高二下学期入学考试化学试题江西省萍乡市2023-2024学年高二下学期4月期中考试化学试题
解题方法
6 . VIA族的氧、硫、硒(Se)、碲(Te)等元素的化合物在科学研究和工业生产中有许多重要用途。回答下列问题:
(1)基态O原子中,未成对电子数与成对电子数之比为_______ 。
(2)亚硫酰氯 在有机合成中有重要应用,分子中S原子的杂化轨道类型为
在有机合成中有重要应用,分子中S原子的杂化轨道类型为_______ ,分子的空间结构为_______ 。
(3)气态电中性基态原子得到一个电子转化为气态基态负离子所放出的能量叫做第一电子亲和能。S、Se、Te三种元素的第一电子亲和能由大到小的顺序是_______ , 、
、 和
和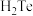 键角最小的是
键角最小的是_______ ,稳定性最强的是_______ 。
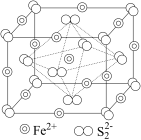
(4)黄铁矿是工业生产硫酸的原料,其晶胞结构如图所示,晶胞参数为anm,该晶体的电子式为_______ , 的配位数为
的配位数为_______ ,晶体的密度为_______  ,在1个晶胞中,由
,在1个晶胞中,由 围成的正八面体的个数为
围成的正八面体的个数为_______ 。
(1)基态O原子中,未成对电子数与成对电子数之比为
(2)亚硫酰氯
 在有机合成中有重要应用,分子中S原子的杂化轨道类型为
在有机合成中有重要应用,分子中S原子的杂化轨道类型为(3)气态电中性基态原子得到一个电子转化为气态基态负离子所放出的能量叫做第一电子亲和能。S、Se、Te三种元素的第一电子亲和能由大到小的顺序是
 、
、 和
和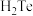 键角最小的是
键角最小的是(4)黄铁矿是工业生产硫酸的原料,其晶胞结构如图所示,晶胞参数为anm,该晶体的电子式为
 的配位数为
的配位数为 ,在1个晶胞中,由
,在1个晶胞中,由 围成的正八面体的个数为
围成的正八面体的个数为
您最近一年使用:0次
名校
解题方法
7 . 价层电子对互斥理论和杂化轨道理论都可以判断、解释分子或离子的空间构型,下列说法正确的是
A.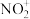 和 和 的键角相同 的键角相同 | B. 、 、 的中心原子价层电子对数相同 的中心原子价层电子对数相同 |
C. 、 、 中S原子的杂化方式相同 中S原子的杂化方式相同 | D. 、 、 都是直线形的分子 都是直线形的分子 |
您最近一年使用:0次
2022-07-15更新
|
294次组卷
|
3卷引用:山东省济宁市2021-2022学年高二下学期期末考试化学试题
山东省济宁市2021-2022学年高二下学期期末考试化学试题云南师范大学附属中学2023-2024学年高二上学期10月月考化学试题(已下线)第04讲 分子的空间结构-【寒假自学课】2024年高二化学寒假提升学与练(人教版2019)
名校
解题方法
8 . 5-氨基四唑硝酸盐受热迅速生成以 为主的环境友好型气体,并放出大量的热,是制造HTPB火箭推进剂的重要原料,结构简式如图,其中五元环为平面结构,下列说法正确的是
为主的环境友好型气体,并放出大量的热,是制造HTPB火箭推进剂的重要原料,结构简式如图,其中五元环为平面结构,下列说法正确的是

 为主的环境友好型气体,并放出大量的热,是制造HTPB火箭推进剂的重要原料,结构简式如图,其中五元环为平面结构,下列说法正确的是
为主的环境友好型气体,并放出大量的热,是制造HTPB火箭推进剂的重要原料,结构简式如图,其中五元环为平面结构,下列说法正确的是 
| A.基态N原子核外电子的运动状态有3种 |
| B.阴离子的空间构型为三角锥形 |
| C.该化合物中五元环上的5个原子的杂化方式都相同 |
D.该化合物因存在类似于苯分子的大 键,所以非常稳定 键,所以非常稳定 |
您最近一年使用:0次
2022-04-29更新
|
985次组卷
|
7卷引用:山东省济宁市2022届高三第二次模拟考试化学试题
21-22高三上·江苏·期中
名校
解题方法
9 . 肼(N2H4)又称为联氨,熔、沸点分别为1.4°C、113.5°C,可用如下方法制备肼:CO(NH2)2+ClO- +2OH- =N2H4+Cl-+CO +H2O。下列有关说法正确的是
+H2O。下列有关说法正确的是
 +H2O。下列有关说法正确的是
+H2O。下列有关说法正确的是| A.N2H4中只存在极性键 |
B. CO 的空间构型为三角锥形 的空间构型为三角锥形 |
| C.CO(NH2)2中C、N、O三种元素第一电离能大小顺序是:C<N<O |
| D.肼的相对分子质量与乙烯接近,但沸点远高于乙烯的原因是能形成分子间氢键 |
您最近一年使用:0次
2021-11-28更新
|
420次组卷
|
5卷引用:山东省济宁市2021-2022学年高三上学期期末考试化学试题
10 . X、Y、Z、W是原子序数依次增大的前四周期元素,X元素有1个2p空轨道,Y为同周期离子半径最小的金属元素,Z元素原子的最外层电子数比次外层电子数少2,W的内层电子已全充满,最外层只有2个电子。请回答下列问题:
(1)X能与氢、氮、氧三种元素构成化合物XO(NH2)2,该化合物分子中的σ键与π键的个数之比是___ ;该物质易溶于水的主要原因是___ 。
(2)元素Z的最高价氧化物中,Z原子的杂化方式是___ ,分子的空间构型是___ 。
(3)元素Z.与W形成的某种化合物的晶胞结构如图所示,则该化合物的化学式为___ 。原子的分数坐标,即将晶胞参数均看做“1”所得出的三维空间坐标,则晶胞中b原子的分数坐标为___ 。
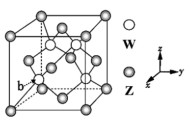
(4)Y的氯化物气态时通常以二聚分子形式存在,分子式为Y2Cl6,分子中所有原子均达到8电子稳定结构,则Y2Cl6的结构式为___ 。
(1)X能与氢、氮、氧三种元素构成化合物XO(NH2)2,该化合物分子中的σ键与π键的个数之比是
(2)元素Z的最高价氧化物中,Z原子的杂化方式是
(3)元素Z.与W形成的某种化合物的晶胞结构如图所示,则该化合物的化学式为

(4)Y的氯化物气态时通常以二聚分子形式存在,分子式为Y2Cl6,分子中所有原子均达到8电子稳定结构,则Y2Cl6的结构式为
您最近一年使用:0次



