解题方法
1 . 碳酸氢钠溶液中碳酸氢根离子以氢键相连成二聚离子,其结构如图所示。
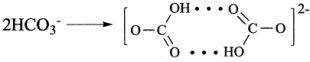
A.键能: | B. 的空间结构:平面三角形 的空间结构:平面三角形 |
C.溶解度: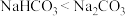 | D. 形成 形成 发生了化学反应 发生了化学反应 |
您最近一年使用:0次
7日内更新
|
77次组卷
|
2卷引用:福建省泉州中远学校2024届高三下学期5月模拟化学试题
2 . 下列相关微粒的说法正确的是
A.H2O的电子式: | B.中子数为20的氯原子: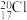 |
C.Na+的结构示意图: | D. 的空间构型为平面三角形 的空间构型为平面三角形 |
您最近一年使用:0次
名校
解题方法
3 . 下列化学用语表达不正确的是
A.H2O的电子式: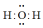 |
B.基态氧原子的轨道表示式: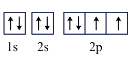 |
C.H2O中心原子的VSEPR模型: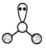 |
| D.H2O分子的空间结构:V形 |
您最近一年使用:0次
解题方法
4 . 锌电池具有成本低、安全性强、可循环使用等优点。一种新型锌电池的工作原理如图所示(凝胶中允许离子生成或迁移)。下列说法错误的是
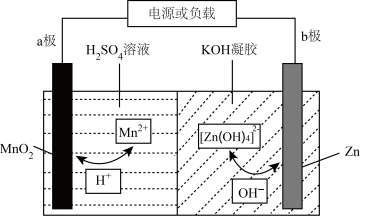
| A.充电过程中,b极接外接电源的负极 |
B.放电过程中,转移 时,b极消耗 时,b极消耗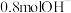 |
C.放电过程中,a极的电极反应式为 |
D.配离子 中Zn采用的是 中Zn采用的是 杂化,该配离子为空间四面体结构 杂化,该配离子为空间四面体结构 |
您最近一年使用:0次
名校
解题方法
5 . 下列分子或离子的空间结构和中心原子的杂化方式均正确的是
A. 平面三角形 平面三角形  杂化 杂化 | B. 平面三角形 平面三角形  杂化 杂化 |
C. V形 V形  杂化 杂化 | D. 三角锥形 三角锥形  杂化 杂化 |
您最近一年使用:0次
2024-04-21更新
|
243次组卷
|
7卷引用:福建省南安市侨光中学2023-2024学年高二下学期4月月考化学试题
福建省南安市侨光中学2023-2024学年高二下学期4月月考化学试题四川省内江市第六中学2022-2023学年高二上学期期中考试化学试题天津市静海区四校2022-2023学年高二下学期3月阶段性检测化学试题(已下线)期中模拟预测卷02(测试范围:选择性必修2+选择性必修3第1章)-2022-2023学年高二化学下学期期中期末考点大串讲(人教版2019)天津市第三中学2022-2023学年高二下学期期中质量检测化学试题陕西省渭南市华州区咸林中学2023-2024学年高二下学期第一次月考化学试题浙江省舟山中学2023-2024学年高二下学期4月月考化学试题
解题方法
6 . “价-类二维图”是元素化合物知识学习的重要模型,下图是某短周期主族元素的“价-类二维图”,其最高化合价c与最低化合价a的代数和为4。
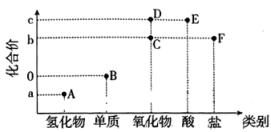
A.实验室可用 溶液吸收气体A 溶液吸收气体A |
| B.C分子的VSEPR模型为V形 |
| C.可用溴水检验F是否变质 |
| D.工业上通过B→D→E两步转化制备E |
您最近一年使用:0次
名校
7 . 氨气是一种重要的化工原料,极易溶于水,合成氨反应为N2(g)+3H2(g)=2NH3(g)  =-92.4kJ•mol-1。下列说法正确的是
=-92.4kJ•mol-1。下列说法正确的是
 =-92.4kJ•mol-1。下列说法正确的是
=-92.4kJ•mol-1。下列说法正确的是A.键角:H2O>NH3>NH |
B.相同浓度的氨水和 溶液中,水的电离程度相同 溶液中,水的电离程度相同 |
C.合成氨反应的 =E(N≡N)+3E(H-H)-6E(N-H)(E表示键能) =E(N≡N)+3E(H-H)-6E(N-H)(E表示键能) |
| D.1molN2与足量H2发生合成氨反应,放出的热量为92.4kJ |
您最近一年使用:0次
名校
解题方法
8 . 回答下列问题
(1)“棕色环”现象是检验溶液中 的一种方法。向含有
的一种方法。向含有 溶液的试管中加入
溶液的试管中加入 ,随后沿管壁加入浓硫酸,在溶液界面上出现“棕色环”,研究发现棕色物质化学式为
,随后沿管壁加入浓硫酸,在溶液界面上出现“棕色环”,研究发现棕色物质化学式为 。
。
① 中N元素采取
中N元素采取________ 杂化,其立体构型为________ (填名称);
② 中一种配体实际上是
中一种配体实际上是 ,则其中Fe元素的化合价为
,则其中Fe元素的化合价为________ ;写出 的一种等电子体的化学式
的一种等电子体的化学式________ ;
③ 中微粒间不存在的作用力有
中微粒间不存在的作用力有________ ;
a.极性键 b.非极性键 c.σ键 d.π键 c.配位键 f.离子键
④ 与
与 等金属离子形成的配合物中配位原子一般是S而不是N,其原因是
等金属离子形成的配合物中配位原子一般是S而不是N,其原因是________ 。
(2)太阳能电池板主要材料为单晶硅或多晶硅。Si的价电子轨道表示式为________ ; 可发生水解反应,机理如下。含s、p、d轨道的杂化类型有A.
可发生水解反应,机理如下。含s、p、d轨道的杂化类型有A. 、B.
、B. 、C.
、C. ,中间体
,中间体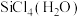 中Si采取的杂化类型为
中Si采取的杂化类型为________ (填字母)。________ ;
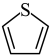
②分子中的大π键可以用符号 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为 )。请问噻吩中的大π键表示为
)。请问噻吩中的大π键表示为________ 。
(4)最简单的硼烷是 ,其分子结构如下左图,B原子的杂化方式为
,其分子结构如下左图,B原子的杂化方式为________ 。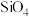 ]四面体(如右上图1所示)的方式形成链状、环状或网络状复杂阴离子,图2所示为一种环状硅酸根离子,其钠盐的化学式为
]四面体(如右上图1所示)的方式形成链状、环状或网络状复杂阴离子,图2所示为一种环状硅酸根离子,其钠盐的化学式为________ 。 熔融时形成一种能导电的液体,测得其中含有一种正四面体形阳离子和一种正八面体形阴离子。则
熔融时形成一种能导电的液体,测得其中含有一种正四面体形阳离子和一种正八面体形阴离子。则 熔融的电离方程式为
熔融的电离方程式为________ 。
(1)“棕色环”现象是检验溶液中
 的一种方法。向含有
的一种方法。向含有 溶液的试管中加入
溶液的试管中加入 ,随后沿管壁加入浓硫酸,在溶液界面上出现“棕色环”,研究发现棕色物质化学式为
,随后沿管壁加入浓硫酸,在溶液界面上出现“棕色环”,研究发现棕色物质化学式为 。
。①
 中N元素采取
中N元素采取②
 中一种配体实际上是
中一种配体实际上是 ,则其中Fe元素的化合价为
,则其中Fe元素的化合价为 的一种等电子体的化学式
的一种等电子体的化学式③
 中微粒间不存在的作用力有
中微粒间不存在的作用力有a.极性键 b.非极性键 c.σ键 d.π键 c.配位键 f.离子键
④
 与
与 等金属离子形成的配合物中配位原子一般是S而不是N,其原因是
等金属离子形成的配合物中配位原子一般是S而不是N,其原因是(2)太阳能电池板主要材料为单晶硅或多晶硅。Si的价电子轨道表示式为
 可发生水解反应,机理如下。含s、p、d轨道的杂化类型有A.
可发生水解反应,机理如下。含s、p、d轨道的杂化类型有A. 、B.
、B. 、C.
、C. ,中间体
,中间体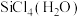 中Si采取的杂化类型为
中Si采取的杂化类型为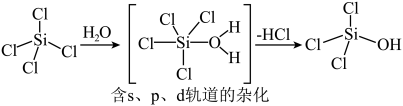
②分子中的大π键可以用符号
 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为 )。请问噻吩中的大π键表示为
)。请问噻吩中的大π键表示为(4)最简单的硼烷是
 ,其分子结构如下左图,B原子的杂化方式为
,其分子结构如下左图,B原子的杂化方式为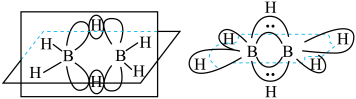
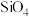 ]四面体(如右上图1所示)的方式形成链状、环状或网络状复杂阴离子,图2所示为一种环状硅酸根离子,其钠盐的化学式为
]四面体(如右上图1所示)的方式形成链状、环状或网络状复杂阴离子,图2所示为一种环状硅酸根离子,其钠盐的化学式为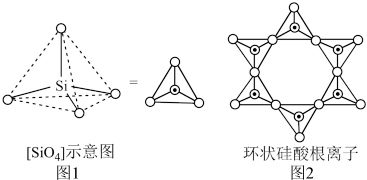
 熔融时形成一种能导电的液体,测得其中含有一种正四面体形阳离子和一种正八面体形阴离子。则
熔融时形成一种能导电的液体,测得其中含有一种正四面体形阳离子和一种正八面体形阴离子。则 熔融的电离方程式为
熔融的电离方程式为
您最近一年使用:0次
名校
9 . P原子在形成 分子时,
分子时,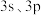 轨道和1个3d轨道参与形成
轨道和1个3d轨道参与形成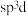 杂化,
杂化, 的空间构型为三角双锥形(如图所示)。下列关于
的空间构型为三角双锥形(如图所示)。下列关于 分子的说法不正确的是
分子的说法不正确的是
 分子时,
分子时,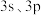 轨道和1个3d轨道参与形成
轨道和1个3d轨道参与形成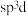 杂化,
杂化, 的空间构型为三角双锥形(如图所示)。下列关于
的空间构型为三角双锥形(如图所示)。下列关于 分子的说法不正确的是
分子的说法不正确的是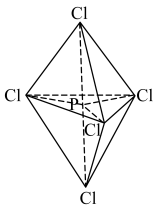
A. 分子中价层电子对数为5 分子中价层电子对数为5 | B. 分子中没有形成 分子中没有形成 键 键 |
C. 分子中所有 分子中所有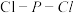 的键角都相等 的键角都相等 | D. 为非极性分子 为非极性分子 |
您最近一年使用:0次
名校
解题方法
10 . 氮及其化合物应用广泛。回答下列问题:
(1)基态N原子处于最高能级的电子云轮廓图为__________ 形。
(2)胍(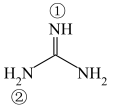 )为平面形分子,存在大π键
)为平面形分子,存在大π键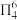 。胍属于
。胍属于__________ 分子(填“极性”或“非极性”),①号N原子H-N-C键角__________ ②号N原子H-N-C键角(填“>”“<”或“=”),胍易吸收空气中H2O和CO2,其原因是____________________________________ 。
(3)氮化钴属于立方晶系,经Cu掺杂得催化剂X,经Li掺杂得催化剂Y。
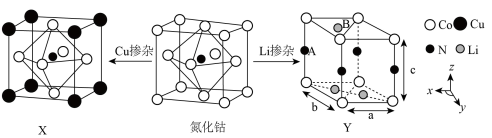
X属于立方晶系,晶胞参数为dpm,距离最近Co原子的核间距为__________ pm,Y属于六方晶系,晶胞参数为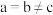 ,
, ,
,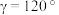 ,如A点原子的分数坐标为
,如A点原子的分数坐标为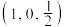 ,则B点Li原子的分数坐标为
,则B点Li原子的分数坐标为____________ ,1个N原子周围距离相等且最近的Li原子数目为_____________ 。
(1)基态N原子处于最高能级的电子云轮廓图为
(2)胍(
 )为平面形分子,存在大π键
)为平面形分子,存在大π键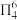 。胍属于
。胍属于(3)氮化钴属于立方晶系,经Cu掺杂得催化剂X,经Li掺杂得催化剂Y。

X属于立方晶系,晶胞参数为dpm,距离最近Co原子的核间距为
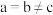 ,
, ,
,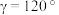 ,如A点原子的分数坐标为
,如A点原子的分数坐标为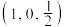 ,则B点Li原子的分数坐标为
,则B点Li原子的分数坐标为
您最近一年使用:0次



