名校
解题方法
1 . 按要求填空:
(1)元素O与Se同主族,电负性O___________ Se(选填“>”、“<”、“=”),基态Se原子价层电子空间运动状态有___________ 种。
(2) 离子的VSEPR模型为
离子的VSEPR模型为___________ ,离子空间构型为___________ 。
(3)6-氨基青霉烷酸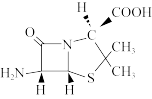 结构中S原子的杂化方式是
结构中S原子的杂化方式是___________ ,组成中C、N、O三种元素的第一电离能由大到小的顺序是___________ 。
(4)1mol环戊二烯(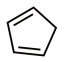 )中含有σ键的数目是
)中含有σ键的数目是___________ ,π键的数目为___________ 。
(5)SiCl4是生产高纯硅的前驱体,其中Si采取的杂化类型为___________ 。SiCl4可发生水解反应,机理如下:___________ (填标号)。
(6)已知H2O、NH3、CH4三种分子中,键角由大到小的顺序是___________ ,原因为___________ 。
(7)在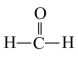 分子中,键角∠HCO
分子中,键角∠HCO___________ (填“>”“<”或“=”)∠HCH,理由是___________ 。
(1)元素O与Se同主族,电负性O
(2)
 离子的VSEPR模型为
离子的VSEPR模型为(3)6-氨基青霉烷酸
 结构中S原子的杂化方式是
结构中S原子的杂化方式是(4)1mol环戊二烯(
 )中含有σ键的数目是
)中含有σ键的数目是(5)SiCl4是生产高纯硅的前驱体,其中Si采取的杂化类型为

(6)已知H2O、NH3、CH4三种分子中,键角由大到小的顺序是
(7)在
 分子中,键角∠HCO
分子中,键角∠HCO
您最近一年使用:0次
名校
2 . 下列说法中正确的个数为
①Cu的第二电离能大于Zn的第二电离能
②H与Cl以1﹕1的关系结合为HCl是因为共价键具有方向性
③ 的VSEPR模型与空间结构一致
的VSEPR模型与空间结构一致
④在冰晶体中,每个H2O分子周围紧邻的分子有4个,是因为水分子之间存在氢键,氢键也具有方向性和饱和性
①Cu的第二电离能大于Zn的第二电离能
②H与Cl以1﹕1的关系结合为HCl是因为共价键具有方向性
③
 的VSEPR模型与空间结构一致
的VSEPR模型与空间结构一致④在冰晶体中,每个H2O分子周围紧邻的分子有4个,是因为水分子之间存在氢键,氢键也具有方向性和饱和性
| A.1 | B.2 | C.3 | D.4 |
您最近一年使用:0次
名校
3 . 用价层电子对互斥模型可以判断许多分子或离子的空间结构,有时也能用来推测键角大小,下列判断正确的是
A. 中心原子的价层电子对数为3,是平面三角形结构 中心原子的价层电子对数为3,是平面三角形结构 |
B.键角大小顺序为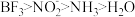 |
C. 是三角锥形的分子 是三角锥形的分子 |
D. 、 、 都是三角锥形的分子 都是三角锥形的分子 |
您最近一年使用:0次
2024-04-28更新
|
162次组卷
|
2卷引用:四川省内江市资中县第二中学2023-2024学年高二下学期3月月考化学试题
名校
解题方法
4 . 下列分子或离子的空间结构和中心原子的杂化方式均正确的是
A. 平面三角形 平面三角形  杂化 杂化 | B. 平面三角形 平面三角形  杂化 杂化 |
C. V形 V形  杂化 杂化 | D. 三角锥形 三角锥形  杂化 杂化 |
您最近一年使用:0次
2024-04-21更新
|
243次组卷
|
7卷引用:四川省内江市第六中学2022-2023学年高二上学期期中考试化学试题
四川省内江市第六中学2022-2023学年高二上学期期中考试化学试题天津市静海区四校2022-2023学年高二下学期3月阶段性检测化学试题(已下线)期中模拟预测卷02(测试范围:选择性必修2+选择性必修3第1章)-2022-2023学年高二化学下学期期中期末考点大串讲(人教版2019)天津市第三中学2022-2023学年高二下学期期中质量检测化学试题陕西省渭南市华州区咸林中学2023-2024学年高二下学期第一次月考化学试题浙江省舟山中学2023-2024学年高二下学期4月月考化学试题福建省南安市侨光中学2023-2024学年高二下学期4月月考化学试题
名校
5 . 下列分子或离子的空间立体构型与其中心原子VSEPR模型与一致的是
A. | B. | C. | D. |
您最近一年使用:0次
名校
解题方法
6 .  为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
①标准状况下,
 和
和 的混合气体中含有的π键数为
的混合气体中含有的π键数为

④6.2g白磷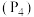 所含σ键的数目为
所含σ键的数目为
⑤0.25mol 中氙的价层电子对数为
中氙的价层电子对数为
⑥46g 中
中 杂化的原子数为
杂化的原子数为
⑦1mol 分子中,S原子的价层电子对数目为
分子中,S原子的价层电子对数目为
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是①标准状况下,

 和
和 的混合气体中含有的π键数为
的混合气体中含有的π键数为
②32g  单质(
单质( 分子结构:
分子结构: )中,
)中, 数目为
数目为

④6.2g白磷
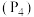 所含σ键的数目为
所含σ键的数目为
⑤0.25mol
 中氙的价层电子对数为
中氙的价层电子对数为
⑥46g
 中
中 杂化的原子数为
杂化的原子数为
⑦1mol
 分子中,S原子的价层电子对数目为
分子中,S原子的价层电子对数目为
| A.①③⑤⑦ | B.①②④⑤ | C.①④⑦ | D.①②③⑥ |
您最近一年使用:0次
名校
解题方法
7 . 下列描述中正确的是
A. 和 和 的中心原子均为 的中心原子均为 杂化 杂化 |
B. 的空间构型为平面三角形 的空间构型为平面三角形 |
C. 中有每个原子均满足最外层8电子稳定结构 中有每个原子均满足最外层8电子稳定结构 |
D. 分子的立体构型为V形 分子的立体构型为V形 |
您最近一年使用:0次
名校
解题方法
8 . 研究发现,铜基催化剂可以促进二氧化碳(CO2)转换成一氧化碳(CO)、甲醛(CH2O)或乙烯(CH2=CH2)及乙醇(CH3CH2OH)等多碳化合物,对于“碳达峰”和“碳中和”目标的顺利实现具有积极推动作用。
(1)Cu基态原子核外电子排布式为___________ ,该元素位于元素周期表第___________ 族,属于___________ 区。
(2)下列说法正确的是___________ (填序号)
a.H2O、CH4、CO2的沸点:H2O>CO2>CH4
b.CH4分子中含有极性键,是极性分子
c.CH2=CH2、CH2O分子中碳原子的杂化方式不同
d.根据价层电子互斥理论,CH2O,H2O,BF3,SO3分子中,H2O的中心原子价层电子对数不同于其他分子
(3)已知具有相同价电子数和相同原子数的分子或离子具有相同的结构,这一原理称为“等电子原理”。根据等电子原理,写出两个与CO2具有相同空间构型的分子或者离子___________ 。
(4)在海洋生物作用下形成CaCO3,亦是减缓大气中CO2增加的主要途径。CaCO3中的化学键除了σ键外,还存在___________ 和大π键,CO 大π键应表示为
大π键应表示为___________ 。(大π键可用符号Π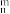 表示,其中n代表参与形成大π键的原子数,m代表参与形成大π键的电子数,如苯分子中的大π键表示为Π
表示,其中n代表参与形成大π键的原子数,m代表参与形成大π键的电子数,如苯分子中的大π键表示为Π )
)
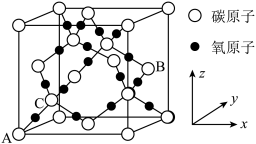
(5)铜基催化剂铁表面上铁原子吸附离解的碳原子局部示意图如图所示(图中小黑球代表碳原子,灰球代表铜原子)。则催化剂表面上C/Cu原子数比为___________ 。

(6)已和CO2在高温高压下所形成的晶体的晶胞如图所示,CO2的晶胞参数(棱长)apm,其密度为bg•cm-3,则阿伏加德罗常数为___________ (列出计算式即可)。
(1)Cu基态原子核外电子排布式为
(2)下列说法正确的是
a.H2O、CH4、CO2的沸点:H2O>CO2>CH4
b.CH4分子中含有极性键,是极性分子
c.CH2=CH2、CH2O分子中碳原子的杂化方式不同
d.根据价层电子互斥理论,CH2O,H2O,BF3,SO3分子中,H2O的中心原子价层电子对数不同于其他分子
(3)已知具有相同价电子数和相同原子数的分子或离子具有相同的结构,这一原理称为“等电子原理”。根据等电子原理,写出两个与CO2具有相同空间构型的分子或者离子
(4)在海洋生物作用下形成CaCO3,亦是减缓大气中CO2增加的主要途径。CaCO3中的化学键除了σ键外,还存在
 大π键应表示为
大π键应表示为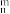 表示,其中n代表参与形成大π键的原子数,m代表参与形成大π键的电子数,如苯分子中的大π键表示为Π
表示,其中n代表参与形成大π键的原子数,m代表参与形成大π键的电子数,如苯分子中的大π键表示为Π )
)(5)铜基催化剂铁表面上铁原子吸附离解的碳原子局部示意图如图所示(图中小黑球代表碳原子,灰球代表铜原子)。则催化剂表面上C/Cu原子数比为

(6)已和CO2在高温高压下所形成的晶体的晶胞如图所示,CO2的晶胞参数(棱长)apm,其密度为bg•cm-3,则阿伏加德罗常数为

您最近一年使用:0次
名校
解题方法
9 . 根据所学内容填空:
(1)有下列物质:①HF、②Cl2、③H2O、④CCl4、⑤BF3、⑥CO2,其中属于极性分子的是_______ (填序号,下同),既有 键又有
键又有 键的是
键的是_______ 。
(2)下列分子中,空间构型为正四面体且键角为 的是
的是_______ 。
a. b.
b. c.
c.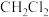 d.
d. e.
e. f.
f.
(3)H2O、 、
、 、
、 的气态分子中,中心原子价层电子对数不同于其他分子的是
的气态分子中,中心原子价层电子对数不同于其他分子的是____ 。
(4)丙烯晴分子( )中碳原子杂化轨道类型为
)中碳原子杂化轨道类型为_______ 。
(5)VIA族元素氧、硫、硒( )的化合物在研究和生产中有许多重要用途。
)的化合物在研究和生产中有许多重要用途。
① 离子的空间构型为
离子的空间构型为_______ 。
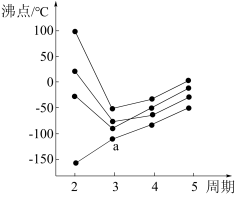
②如图所示,每条折线表示周期表IVA—VIIA族中的某一族元素氢化物的沸点变化。每个小黑点代表一种氢化物,其中a点代表的是_______ (化学式)
(1)有下列物质:①HF、②Cl2、③H2O、④CCl4、⑤BF3、⑥CO2,其中属于极性分子的是
 键又有
键又有 键的是
键的是(2)下列分子中,空间构型为正四面体且键角为
 的是
的是a.
 b.
b. c.
c.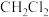 d.
d. e.
e. f.
f.
(3)H2O、
 、
、 、
、 的气态分子中,中心原子价层电子对数不同于其他分子的是
的气态分子中,中心原子价层电子对数不同于其他分子的是(4)丙烯晴分子(
 )中碳原子杂化轨道类型为
)中碳原子杂化轨道类型为(5)VIA族元素氧、硫、硒(
 )的化合物在研究和生产中有许多重要用途。
)的化合物在研究和生产中有许多重要用途。①
 离子的空间构型为
离子的空间构型为②如图所示,每条折线表示周期表IVA—VIIA族中的某一族元素氢化物的沸点变化。每个小黑点代表一种氢化物,其中a点代表的是

您最近一年使用:0次
名校
解题方法
10 . 下列说法错误的是
| A.价层电子对包括σ键电子对和中心原子上的孤电子对 |
B. 和 和 都是正四面体形微粒,且键角都为 都是正四面体形微粒,且键角都为 |
C. 分子中有一对未成键的孤电子对,它对成键电子的排斥作用较强 分子中有一对未成键的孤电子对,它对成键电子的排斥作用较强 |
D. 、 、 、 、 、 、 分子中每个原子的最外层电子都满足了8电子稳定结构 分子中每个原子的最外层电子都满足了8电子稳定结构 |
您最近一年使用:0次



