名校
解题方法
1 . 下列说法错误的是
| A.价层电子对包括σ键电子对和中心原子上的孤电子对 |
B. 和 和 都是正四面体形微粒,且键角都为 都是正四面体形微粒,且键角都为 |
C. 分子中有一对未成键的孤电子对,它对成键电子的排斥作用较强 分子中有一对未成键的孤电子对,它对成键电子的排斥作用较强 |
D. 、 、 、 、 、 、 分子中每个原子的最外层电子都满足了8电子稳定结构 分子中每个原子的最外层电子都满足了8电子稳定结构 |
您最近一年使用:0次
名校
解题方法
2 . 铜是生活中一种非常重要的金属,黄铜矿(CuFeS2)是炼铜的最主要矿物,火法炼铜时涉及反应:2CuFeS2+O2=Cu2S+2FeS+SO2。
(1)O的轨道表示式为_______ ,其最高能级的原子轨道形状为_______ ,第一电离能:O_____ N(填“>”或“<”),Fe2+的价层电子排布式为______ 。
(2)SO2的VSEPR构型为_______ ,键角_______ H2O(填“>”或“<”);Cu元素位于周期表的________ 区,Cu和Zn的部分电离能数据如表所示,观察数据可知I2(Cu)>I2(Zn),对此,你的解释是______ 。
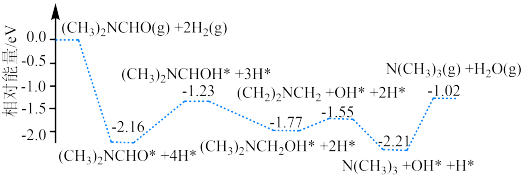
(3)我国科学家实现了铜催化剂将(CH3)2NCHO转化为N(CH3)3。计算机模拟单个分子在铜催化剂表面的反应历程如图所示:______ ;该反应在______ (填“高温”/“低温”/“任何温度”)下有自发性。
(1)O的轨道表示式为
(2)SO2的VSEPR构型为
| 元素 | Cu | Zn | |
| 电离能/(kJ•mol-1) | I1 | 746 | 906 |
| I2 | 1985 | 1733 | |
(3)我国科学家实现了铜催化剂将(CH3)2NCHO转化为N(CH3)3。计算机模拟单个分子在铜催化剂表面的反应历程如图所示:
您最近一年使用:0次
2024-03-10更新
|
127次组卷
|
2卷引用:四川省绵阳中学2023-2024学年高二下学期开学化学试题
名校
解题方法
3 . 下列化学用语表述正确的是
A.基态铬原子的价层电子排布式: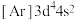 |
B.用电子云轮廓图描述2Py原子轨道的形状: 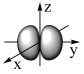 |
C.氨气分子的VSEPR模型: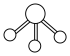 |
D.基态碳原子的核外电子轨道表示式为: 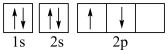 |
您最近一年使用:0次
2024-01-22更新
|
167次组卷
|
2卷引用:四川省德阳外国语学校2023-2024学年高二下学期入学考试化学试题
解题方法
4 . 下列说法正确的是
| A.同一原子中3s、3p、3d、4s的能量依次升高 |
B. 、 、 中S原子的VSEPR模型均为平面三角形 中S原子的VSEPR模型均为平面三角形 |
C.氯化钠是离子晶体,由 和 和 构成,常温下能导电 构成,常温下能导电 |
D. 和晶体硅都是共价化合物,属于共价晶体 和晶体硅都是共价化合物,属于共价晶体 |
您最近一年使用:0次
名校
5 . 下列关于杂化轨道的叙述中,不正确的是( )
| A.分子中中心原子通过sp3杂化轨道成键时,该分子不一定为正四面体结构 |
| B.杂化轨道只用于形成σ键或用于容纳未参与成键的孤电子对 |
| C.NH3和CH4两个分子中中心原子N和C都是通过sp3杂化轨道成键 |
D.ClO 的立体构型为平面三角形 的立体构型为平面三角形 |
您最近一年使用:0次
2023-06-08更新
|
76次组卷
|
2卷引用:四川省泸州市泸县第四中学2023-2024学年高二下学期开学化学试题
名校
解题方法
6 . 回答下列问题:
(1)甲烷在一定条件下可生成以下微粒:
A.碳正离子(CH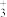 ) B.碳负离子(CH
) B.碳负离子(CH ) C. 甲基 (—CH3) D.碳烯 (
) C. 甲基 (—CH3) D.碳烯 ( CH2)
CH2)
①四种微粒中,键角为120°的是___________ (填序号)。
②碳负离子(CH )的空间构型为
)的空间构型为___________ ,与(CH )互为等电子体的一种分子是
)互为等电子体的一种分子是___________ (填化学式)。
(2)在制取合成氨原料气的过程中,常混有一些杂质,如CO会使催化剂中毒。除去CO的化学方程式为(HAc表示醋酸)Cu(NH3)2Ac+CO+NH3=Cu(NH3)3(CO)Ac.请回答下列问题:
①该反应中含有的第二周期非金属元素的第一电离能由大到小的顺序为___________ 。
②在一定条件下NH3和CO2能合成尿素CO(NH2)2,尿素中碳原子轨道的杂化类型为___________ ;1 mol尿素分子中,σ 键的数目为___________ 。
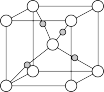
③Cu与O形成的某种化合物的晶胞结构如下图所示,若阿伏加德罗常数的值为NA,晶胞的边长为a pm,则该晶体的密度为___________ g·cm-3。
(1)甲烷在一定条件下可生成以下微粒:
A.碳正离子(CH
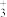 ) B.碳负离子(CH
) B.碳负离子(CH ) C. 甲基 (—CH3) D.碳烯 (
) C. 甲基 (—CH3) D.碳烯 ( CH2)
CH2)①四种微粒中,键角为120°的是
②碳负离子(CH
 )的空间构型为
)的空间构型为 )互为等电子体的一种分子是
)互为等电子体的一种分子是(2)在制取合成氨原料气的过程中,常混有一些杂质,如CO会使催化剂中毒。除去CO的化学方程式为(HAc表示醋酸)Cu(NH3)2Ac+CO+NH3=Cu(NH3)3(CO)Ac.请回答下列问题:
①该反应中含有的第二周期非金属元素的第一电离能由大到小的顺序为
②在一定条件下NH3和CO2能合成尿素CO(NH2)2,尿素中碳原子轨道的杂化类型为
③Cu与O形成的某种化合物的晶胞结构如下图所示,若阿伏加德罗常数的值为NA,晶胞的边长为a pm,则该晶体的密度为

您最近一年使用:0次
名校
解题方法
7 . 五种元素A、B、C、D、E,其中A元素形成的原子核内只有一个质子;B的基态原子s能级的总电子数比p能级的总电子数多1;C元素的原子最外层电子数是次外层的3倍;D在B的下一周期,在同周期元素中,D形成的简单离子半径最小;E是形成化合物种类最多的元素。
(1)A、E形成的化合物E2A4分子中σ键和π键数目之比为_______ ,B、C、E三种元素的第一电离能由大到小的顺序为_______ 。
(2)与PH3相比,BA3易液化的主要原因是_______ 。
(3)BC 离子的立体构型为
离子的立体构型为_______ ,BC 中B原子轨道的杂化类型为
中B原子轨道的杂化类型为_______ 。
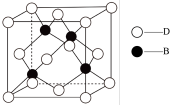
(4)化合物DB是人工合成的半导体材料,它的晶胞结构如图所示,其中最近两个D原子的核间距为a cm。该晶体的密度为_______ g·cm-3 (NA表示阿伏加德罗常数的值)。
(1)A、E形成的化合物E2A4分子中σ键和π键数目之比为
(2)与PH3相比,BA3易液化的主要原因是
(3)BC
 离子的立体构型为
离子的立体构型为 中B原子轨道的杂化类型为
中B原子轨道的杂化类型为(4)化合物DB是人工合成的半导体材料,它的晶胞结构如图所示,其中最近两个D原子的核间距为a cm。该晶体的密度为

您最近一年使用:0次
解题方法
8 . 下列分子中共价键键角最小的是
| A.CH4 | B.CO2 | C.NH3 | D.H2O |
您最近一年使用:0次
9 . 下列说话不正确 的是
| A.ClO4-、SO32−、ClO2-都为sp3杂化,离子构型分别为正四面体形、三角锥形、“V”形 |
| B.SO42−和CCl4互为等电子体,中心原子都采用sp3杂化,分子或离子构型为正四面体形 |
| C.CH3COOH中碳原子采用sp3、sp2杂化,σ键与π键数之比为7:1 |
| D.BF3、NF3中心原子都为sp2杂化,为平面三角形 |
您最近一年使用:0次
名校
10 . 下列物质的分子中,键角最小的是
| A.CH2=CH2 | B.H2O | C.NH3 | D.CH4 |
您最近一年使用:0次
2019-04-09更新
|
181次组卷
|
2卷引用:四川省自贡市田家炳中学2020-2021学年高二上学期开学考试化学试题



