名校
解题方法
1 .  为乙二胺四乙酸
为乙二胺四乙酸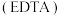 ,易与金属离子形成配合物。
,易与金属离子形成配合物。 为
为 与
与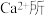 形成。下列叙述正确的是
形成。下列叙述正确的是

 为乙二胺四乙酸
为乙二胺四乙酸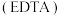 ,易与金属离子形成配合物。
,易与金属离子形成配合物。 为
为 与
与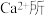 形成。下列叙述正确的是
形成。下列叙述正确的是
| A.b含有分子内氢键 | B.b中 的配位数为 的配位数为 |
C.a和b中的 原子均为 原子均为  杂化 杂化 | D.b含有共价键、离子键和配位键 |
您最近一年使用:0次
2023-02-17更新
|
399次组卷
|
11卷引用:2015-2016学年福建省厦门市高二上学期期末质检化学试卷
2015-2016学年福建省厦门市高二上学期期末质检化学试卷山西省朔州市怀仁市2020-2021学年高二下学期期末考试化学试题福建省三明市第一中学2016-2017学年高二下学期半期考试化学试题福建省厦门市湖滨中学2018-2019学年高二(理)上学期期中考试化学试题福建省厦门市思明区厦门外国语学校2019-2020学年高二上学期周末练习10——化学试题天津市耀华中学2020-2021学年高二下学期期中检测化学试题湖北省罗田县第一中学2021-2022学年高二下学期6月月考化学试题(实验班)湖北省当阳市第一高级中学2022-2023学年高三上学期期中考试化学试题(已下线)安徽省、云南省、吉林省、黑龙江省2023届高三2月适应性测试变式题(选择题11-13)江西省景德镇一中2022-2023学年高二下学期期中考试(19班)化学试题江西省宜春市宜丰中学2022-2023学年高三下学期3月月考化学试题
名校
解题方法
2 . 下列叙述中正确的是
A. 为角形的极性分子,形成分子晶体 为角形的极性分子,形成分子晶体 |
B. 的空间结构为平面三角形 的空间结构为平面三角形 |
C.氯化硼 的熔点为 的熔点为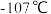 ,氯化硼液态时能导电而固态时不导电 ,氯化硼液态时能导电而固态时不导电 |
D. 和 和 的中心原子均为 的中心原子均为 杂化, 杂化,  分子呈正四面体形, 分子呈正四面体形, 呈三角锥形 呈三角锥形 |
您最近一年使用:0次
2021-02-07更新
|
1381次组卷
|
14卷引用:山西省朔州市怀仁县大地学校2019-2020学年高二下学期期末考试化学试题
山西省朔州市怀仁县大地学校2019-2020学年高二下学期期末考试化学试题黑龙江省龙东南联合体2018-2019学年高二下学期期末考试化学试题宁夏海原县第一中学2019-2020学年高二下学期期末考试化学试题(已下线)第35讲 分子结构与性质-2021年高考化学一轮复习名师精讲练新疆生产建设兵团第三师图木舒克市第一中学2022-2023学年高二下学期期末考试化学试题广西壮族自治区南宁市第二中学2022-2023学年高二下学期期末化学考试试卷(人教版2019)选择性必修2 阶段性综合评估测试卷(二)鲁科版2019选择性必修2阶段性综合评估测试卷(二)广东省佛山市南海区南海中学2021-2022学年高二年级下学期4月月考化学试题湖北省襄阳市第一中学2022-2023学年高二下学期3月月考化学试题四川省广安市第二中学校2022-2023学年高二下学期期中考试化学试题山东省新泰市第一中学2022-2023学年高二下学期第一次阶段考试化学试题四川省泸县第五中学2022-2023学年高二下学期5月期中考试化学试题河北省邯郸市磁县第一中学2023-2024学年高二上学期七调月考化学试题
3 . ⅤA族的氮、磷、砷(As)等元素在化合物中常表现出多种氧化态,含ⅤA族元素的化合物在医药生产中有许多重要用途。请回答下列问题:
(1)基态氮原子的价电子排布图是___ ;基态砷原子的电子排布式为___ 。
(2)砷与同周期第ⅦA族的溴的第一电离能相比,较大的是___ 。
(3)AsH3是无色稍有大蒜味的气体。AsH3的沸点高于PH3,其主要原因是___ 。
(4)Na3AsO4可作杀虫剂。AsO 的立体构型为
的立体构型为___ ,与其互为等电子体的一种分子为___ 。
(5)某砷的氧化物俗称“砒霜”,其分子结构如图所示。该化合物的分子式为___ ,砷原子采取___ 杂化。
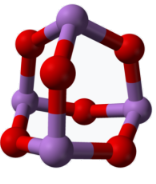
(6)GaAs是人工合成的新型半导体材料,其晶体结构与金刚石相似。GaAs晶体中,每个As与___ 个Ga相连。
(1)基态氮原子的价电子排布图是
(2)砷与同周期第ⅦA族的溴的第一电离能相比,较大的是
(3)AsH3是无色稍有大蒜味的气体。AsH3的沸点高于PH3,其主要原因是
(4)Na3AsO4可作杀虫剂。AsO
 的立体构型为
的立体构型为(5)某砷的氧化物俗称“砒霜”,其分子结构如图所示。该化合物的分子式为

(6)GaAs是人工合成的新型半导体材料,其晶体结构与金刚石相似。GaAs晶体中,每个As与
您最近一年使用:0次
解题方法
4 . 氟及其化合物用途非常广泛。回答下列问题:
(1)聚四氟乙烯商品名称为“特氟龙”,可做不粘锅涂层。它是一种准晶体,该晶体是一种无平移周期序、但有严格准周期位置序的独特晶体。可通过____________ 方法区分晶体、准晶体和非晶体。
(2)锑(Sb)与砷处于同一主族且相邻,基态锑原子价电子排布式为____________ 。[H2F]+[SbF6]-(氟酸锑)是一种超强酸,存在[H2F]+,写出一种与[H2F]+互为等电子体的阴离子是____________ 。
(3)硼酸(H3BO3)和四氟硼酸铵(NH4BF4)都有着重要的化工用途。
①H3BO3和NH4BF4涉及的四种元素中第二周期元素的第一电离能由大到小的顺序____________ (填元素符号)。
②H3BO3本身不能电离出H+,在水中易结合一个OH﹣生成[B(OH)4]﹣,而体现弱酸性。[B(OH)4]﹣中B原子的杂化类型为____________ 。
③NH4BF4(四氟硼酸铵)可用作铝或铜焊接助熔剂、能腐蚀玻璃等。四氟硼酸铵中存在____________ (填序号):
A.离子键 B. σ键 C.π键D.范德华力 E.配位键
(4)CuCl的熔点为426℃,熔化时几乎不导电;CuF的熔点为908℃。
①CuF比CuCl熔点高的原因是____________ ;
②CuF的晶胞结构如图。F-填充在Cu+围成的____________ 空隙中,空隙填充率为____________ %。

(1)聚四氟乙烯商品名称为“特氟龙”,可做不粘锅涂层。它是一种准晶体,该晶体是一种无平移周期序、但有严格准周期位置序的独特晶体。可通过
(2)锑(Sb)与砷处于同一主族且相邻,基态锑原子价电子排布式为
(3)硼酸(H3BO3)和四氟硼酸铵(NH4BF4)都有着重要的化工用途。
①H3BO3和NH4BF4涉及的四种元素中第二周期元素的第一电离能由大到小的顺序
②H3BO3本身不能电离出H+,在水中易结合一个OH﹣生成[B(OH)4]﹣,而体现弱酸性。[B(OH)4]﹣中B原子的杂化类型为
③NH4BF4(四氟硼酸铵)可用作铝或铜焊接助熔剂、能腐蚀玻璃等。四氟硼酸铵中存在
A.离子键 B. σ键 C.π键D.范德华力 E.配位键
(4)CuCl的熔点为426℃,熔化时几乎不导电;CuF的熔点为908℃。
①CuF比CuCl熔点高的原因是
②CuF的晶胞结构如图。F-填充在Cu+围成的

您最近一年使用:0次
名校
解题方法
5 . 已知P4单质的结构如下,P4在KOH溶液中的变化是:P4+3KOH+3H2O=3KH2PO2+PH3下列说法正确的是
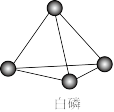

| A.产物PH3分子中所有的原子可能共平面 |
| B.31gP4含有1.5NA个P−P键 |
| C.相关元素的电负性大小顺序:P>O>H>K |
| D.P4中P原子为sp2杂化 |
您最近一年使用:0次
2020-08-21更新
|
283次组卷
|
7卷引用:山西省朔州市怀仁市第一中学校云东校区2019-2020学年高二下学期期末考试化学试题
解题方法
6 . 氧、钾、铬、碘的单质及其化合物在生产、生活中有广泛应用。
(1)上述四种基态原子中,未成对电子数最多的是_______ (填元素符号,下同)。最外层电子排布式相同的元素是_______ 。
(2)钾晶体的熔点______ (填“高于”或“低于”) 铬晶体的熔点。
(3)与IO 互为等电子体的分子有
互为等电子体的分子有_______ (写一种即可),IO 中碘原子的杂化轨道类型是
中碘原子的杂化轨道类型是________ 。
(4)KIO3晶体是一种性能良好的非线性光学材料,具有钙钛矿型的立方结构,晶胞中K、I、O分别处于顶角、体心、面心位置,如图所示。氧、钾离子最近核间距为d cm,NA代表阿伏加 德罗常数的值。则KIO3晶胞的密度(ρ)为________ g•cm-3。

(1)上述四种基态原子中,未成对电子数最多的是
(2)钾晶体的熔点
(3)与IO
 互为等电子体的分子有
互为等电子体的分子有 中碘原子的杂化轨道类型是
中碘原子的杂化轨道类型是(4)KIO3晶体是一种性能良好的非线性光学材料,具有钙钛矿型的立方结构,晶胞中K、I、O分别处于顶角、体心、面心位置,如图所示。氧、钾离子最近核间距为d cm,NA代表阿伏加 德罗常数的值。则KIO3晶胞的密度(ρ)为

您最近一年使用:0次
2020-08-21更新
|
79次组卷
|
2卷引用:山西省运城市2019-2020学年高二下学期期末测试化学试题
解题方法
7 . 有关雷酸(H—O—N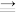 C)和氰酸(H —O—C≡N)的说法错误的是
C)和氰酸(H —O—C≡N)的说法错误的是
 C)和氰酸(H —O—C≡N)的说法错误的是
C)和氰酸(H —O—C≡N)的说法错误的是| A.两者互为同分异构体 |
| B.元素电负性:O>N>C |
| C.物质中所含元素第一电离能:N>O>C |
| D.两种分子中的所有原子均在同一直线上 |
您最近一年使用:0次
2020-08-21更新
|
151次组卷
|
5卷引用:山西省运城市2019-2020学年高二下学期期末测试化学试题
解题方法
8 . 引起灰霾的PM2.5微细粒子包含(NH4)2SO4、NH4NO3、含锌有机颗粒物及扬尘等。通过测定灰霾中锌等重金属的含量,可知交通污染是目前造成我国灰霾天气主要原因之一。
(1)Zn2+在基态时核外电子排布式为_________ 。
(2)PM2.5富含大量的有毒、有害物质,易引发二次光化学烟雾污染,光化学烟雾中含有NOx、O3、CH2=CH-CHO、HCOOH、CH3COOONO2(PAN)等二次污染物。
①N2O分子的立体构型为______ 。
②CH2=CH-CHO分子中碳原子的杂化方式为______
③1mol HCOOH 中含σ键数目为_____ 。
④NO 能被FeSO4溶液吸收生成配合物[Fe(NO)(H2O)5]SO4,该配合物中心离子的配体为______ ,Fe的化合价为_____ 。
(1)Zn2+在基态时核外电子排布式为
(2)PM2.5富含大量的有毒、有害物质,易引发二次光化学烟雾污染,光化学烟雾中含有NOx、O3、CH2=CH-CHO、HCOOH、CH3COOONO2(PAN)等二次污染物。
①N2O分子的立体构型为
②CH2=CH-CHO分子中碳原子的杂化方式为
③1mol HCOOH 中含σ键数目为
④NO 能被FeSO4溶液吸收生成配合物[Fe(NO)(H2O)5]SO4,该配合物中心离子的配体为
您最近一年使用:0次
2020-08-21更新
|
237次组卷
|
2卷引用:山西省运城市2019-2020学年高二下学期期末测试化学试题
9 . 钛很多重要的化合物。如TiO2、TiCl4、[Ti(OH)2(H2O)4]Cl2。如图为TiO2催化下,O3降解CH3CHO的示意图。回答下列问题:

(1)基态Ti原子的价层电子排布式为________ 。
(2)1molCH3CHO中含有的σ键的数目为_________ (设阿伏加 德罗常数的值为NA),碳原子的杂化方式为________ 。
(3)乙醛的沸点_________ (填“高于”或“低于”)乙醇的沸点,原因是_________ 。
(4)半夹心结构催化剂M能催化乙烯、丙烯、苯乙烯的聚合,其结构如下图所示。

①M中非金属元素O、C的第一电离能大小顺序_________ 。
②基态Cl原子的核外电子占据的最高能级的电子云轮廓图为__________ 形。
③M中不含(填代号)________ 。
a.π键 b.离子键 c.σ键 d.配位键
(5)根据等电子原理,可推断O3的空间构型是__________ 。
(6)TiCl4的沸点为136.4℃易溶于乙醇等有机溶剂,说明TiCl4属于_________ 晶体。
(7)钛原子(Ti)一定条件下和碳原子可形成气态团簇分子;分子模型如图1所示,其中白球表示Ti原子,黑球表示碳原子,则其分子式为________ 。已知晶体TiO2的晶胞如图2所示,其晶胞边长为540.0pm,密度为_________ g•cm-3(列式表示),Ti与O之间的距离为________ pm(列式表示)。


(1)基态Ti原子的价层电子排布式为
(2)1molCH3CHO中含有的σ键的数目为
(3)乙醛的沸点
(4)半夹心结构催化剂M能催化乙烯、丙烯、苯乙烯的聚合,其结构如下图所示。

①M中非金属元素O、C的第一电离能大小顺序
②基态Cl原子的核外电子占据的最高能级的电子云轮廓图为
③M中不含(填代号)
a.π键 b.离子键 c.σ键 d.配位键
(5)根据等电子原理,可推断O3的空间构型是
(6)TiCl4的沸点为136.4℃易溶于乙醇等有机溶剂,说明TiCl4属于
(7)钛原子(Ti)一定条件下和碳原子可形成气态团簇分子;分子模型如图1所示,其中白球表示Ti原子,黑球表示碳原子,则其分子式为

您最近一年使用:0次
2020-08-06更新
|
91次组卷
|
2卷引用:山西省朔州市重点中学2019-2020学年高一下学期期末教学质量检测化学试题
解题方法
10 . 元素X的基态原子的2p能级有4个电子;元素Y的M层电子运动状态与X的价电子运动状态相同;元素Z位于第四周期,其基态原子的2价阳离子M层轨道全部排满电子。下列推断正确的是
A.Y是S元素,基态原子最外层电子排布图为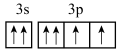 |
| B.离子晶体ZX、ZY的熔点:ZX>ZY |
| C.在Y的氢化物H2Y分子中,Y原子轨道的杂化类型是sp2 |
| D.Y与X可形成YX32-,立体构型为四面体 |
您最近一年使用:0次
2020-08-06更新
|
561次组卷
|
3卷引用:山西省朔州市重点中学2019-2020学年高一下学期期末教学质量检测化学试题
山西省朔州市重点中学2019-2020学年高一下学期期末教学质量检测化学试题山西省孝义市2019-2020学年高二下学期期末考试化学试题(已下线)解密13 物质结构与性质(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练



