解题方法
1 . 碳(C)、氮(N)、氧(O)、硫(S)等是常见的非金属元素,钴(Co)是一种重要的金属元素,回答下列问题:
(1)一种由含钴的配合物形成的新型高能材料的结构如图所示。

①阴离子 是该材料的组成部分,则1mol该阴离子中含σ键的数目为
是该材料的组成部分,则1mol该阴离子中含σ键的数目为_______ (NA为阿伏加德罗常数的值),已知该离子是平面结构,则图中标记*的N和O原子之间的σ键是由N原子的_______ 杂化轨道与O原子的_______ 轨道重叠形成。
②写出一种与 互为等电子体的分子:
互为等电子体的分子:_______ (填化学式)。
③实验证明NH3的极性比NCl3大,其原因是_______ 。
(2)一种新型环烯类储氢材料分子式为C16S8,分子中的原子都处于同平面上(结构如图所示),每个平面上下两侧最多可储存10个H2分子。

①有关键长数据如下:
从表中数据可以推测C16S8中碳硫键的性质为_______ (填字母)。
A.类似于C-S单键的性质
B.类似于C=S双键的性质
C.兼有C-S单键和C=S双键的性质
②储氢时,C16S8与H2间的作用力是_______ 。
(3) 和NH3是配合物
和NH3是配合物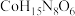 的配体,若该配合物的中心离子的价电子层有4个未成对电子,则其配位数为6的正二价配离子化学式为
的配体,若该配合物的中心离子的价电子层有4个未成对电子,则其配位数为6的正二价配离子化学式为_______ 。
(4)CoO2是一种磁性材料,其晶胞结构如图甲所示,俯视图如图乙所示。

①原子坐标参数:A为(0,0,0);B为(0.31,0.31,0),则C原子的坐标参数为_______ 。
②若阿伏加德罗常数的值为NA,则该晶体密度为_______  (列出计算表达式)。
(列出计算表达式)。
(1)一种由含钴的配合物形成的新型高能材料的结构如图所示。

①阴离子
 是该材料的组成部分,则1mol该阴离子中含σ键的数目为
是该材料的组成部分,则1mol该阴离子中含σ键的数目为②写出一种与
 互为等电子体的分子:
互为等电子体的分子:③实验证明NH3的极性比NCl3大,其原因是
(2)一种新型环烯类储氢材料分子式为C16S8,分子中的原子都处于同平面上(结构如图所示),每个平面上下两侧最多可储存10个H2分子。

①有关键长数据如下:
| 化学键 | C-S | C=S | C16S8 |
| 键长/pm | 181 | 155 | 176 |
从表中数据可以推测C16S8中碳硫键的性质为
A.类似于C-S单键的性质
B.类似于C=S双键的性质
C.兼有C-S单键和C=S双键的性质
②储氢时,C16S8与H2间的作用力是
(3)
 和NH3是配合物
和NH3是配合物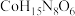 的配体,若该配合物的中心离子的价电子层有4个未成对电子,则其配位数为6的正二价配离子化学式为
的配体,若该配合物的中心离子的价电子层有4个未成对电子,则其配位数为6的正二价配离子化学式为(4)CoO2是一种磁性材料,其晶胞结构如图甲所示,俯视图如图乙所示。

①原子坐标参数:A为(0,0,0);B为(0.31,0.31,0),则C原子的坐标参数为
②若阿伏加德罗常数的值为NA,则该晶体密度为
 (列出计算表达式)。
(列出计算表达式)。
您最近一年使用:0次
解题方法
2 . [Zn(CN)4]2-在水溶液中可与HCHO发生反应生成[Zn(H2O)4]2+和HOCH2CN,下列说法错误的是
| A.C、N、O第一电离能由大到小的顺序为:N>O>C |
| B.1 mol HOCH2CN分子中含有的σ键与π键的物质的量之比为3∶1 |
| C.H2O分子中氧原子、HOCH2CN分子中碳原子轨道的杂化类型均为sp3 |
D.[Zn(CN)4]2-中Zn2+与CN-的C原子形成配位键,结构可表示为 |
您最近一年使用:0次
3 . 汽车尾气中的氮氧化物、碳氢化物与臭氧反应是造成城市光化学污染的主要原因,其中常见的反应为CH3CH=CHCH3(2-丁烯)+2O3→2CH3CHO+2O2,已知NA为阿伏加德罗常数的值,下列有关说法正确的是
| A.标准状况下,2.24L CH3CHO中所含原子数目为0.7NA |
| B.O2和O3均只含非极性键,均为非极性分子 |
C.CH3CHO和CH3CH=CHCH3分子中采取 杂化和 杂化和 杂化的碳原子数目之比均为1:1 杂化的碳原子数目之比均为1:1 |
| D.若有2mol O3参与反应,则反应中转移的电子数目为12NA |
您最近一年使用:0次
2022-10-08更新
|
969次组卷
|
3卷引用:河北省任丘市第一中学2022-2023学年高三上学期期中考试化学试题
名校
解题方法
4 . 碳铂(结构简式如下)是一种广谱抗癌药物。下列关于碳铂的说法错误的是
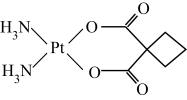

| A.中心原子的配位数为4 |
B.分子中 键与 键与 键数目之比为13∶1 键数目之比为13∶1 |
C. 和 和 杂化的碳原子数之比为2∶1 杂化的碳原子数之比为2∶1 |
| D.分子中含有极性键、非极性键、配位键和离子键 |
您最近一年使用:0次
名校
5 . 我国科学家通过X射线衍射获得了如图所示青蒿素的分子结构,有关青蒿素的说法错误的是


| A.该分子中存在极性键和非极性键 |
B.该分子中碳原子和氧原子均存在 、 、 两种杂化方式 两种杂化方式 |
C.该有机物的分子式为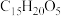 |
| D.青蒿素分子具有较强的氧化性 |
您最近一年使用:0次
2022-07-14更新
|
180次组卷
|
2卷引用:河北省石家庄市2021-2022学年高二下学期期末考试化学试题
名校
6 . As2O3(砒霜)是两性氧化物,分子结构如图所示,与盐酸反应能生成AsCl3,AsCl3和LiAlH4反应的产物之一为AsH3。下列说法不正确的是
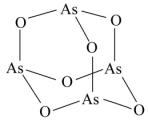

| A.As2O3分子中As原子的杂化方式为sp3 |
B.AlH 的价层电子对互斥模型是四面体形 的价层电子对互斥模型是四面体形 |
| C.AsCl3的空间构型为平面正三角形,As原子的杂化方式为sp3 |
| D.AsH3分子的键角小于109°28′ |
您最近一年使用:0次
2023-01-05更新
|
633次组卷
|
3卷引用:河北省唐山市开滦第一中学2022-2023学年高二上学期12月月考化学试题
解题方法
7 . 冰、干冰、金刚石的晶体结构如图,下列说法错误的是
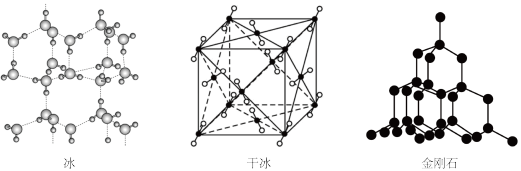

A.金刚石中碳原子的杂化方式为 杂化 杂化 |
| B.冰融化的过程中破坏了氢键和共价键 |
| C.冰和干冰的晶体类型相同,均具有自范性 |
D.干冰晶体中,1个 分子周围有12个紧邻的 分子周围有12个紧邻的 分子 分子 |
您最近一年使用:0次
名校
解题方法
8 . 白磷( ,结构如图所示)与
,结构如图所示)与 反应得
反应得 ,
, 可继续与
可继续与 反应:
反应:
 。固态
。固态 中含有
中含有 、
、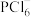 两种离子。下列关于
两种离子。下列关于 、
、 、
、 和
和 的说法正确的是
的说法正确的是
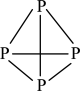
 ,结构如图所示)与
,结构如图所示)与 反应得
反应得 ,
, 可继续与
可继续与 反应:
反应:
 。固态
。固态 中含有
中含有 、
、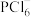 两种离子。下列关于
两种离子。下列关于 、
、 、
、 和
和 的说法正确的是
的说法正确的是
A. 很稳定是因为分子间含有氢键 很稳定是因为分子间含有氢键 |
B. 的空间构型为平面三角形 的空间构型为平面三角形 |
C. 与 与 中的P原子杂化方式均为 中的P原子杂化方式均为 杂化,键角相同 杂化,键角相同 |
D.1  分子中成键电子对与孤电子对的比值为3∶2 分子中成键电子对与孤电子对的比值为3∶2 |
您最近一年使用:0次
2022-12-30更新
|
592次组卷
|
5卷引用:河北省邯郸市第一中学2022-2023学年高三上学期一轮复习(四)化学试题
名校
解题方法
9 . 邻氨基吡啶的铜配合物在有机不对称合成中起催化诱导效应,其结构简式如图所示。下列相关说法正确的是
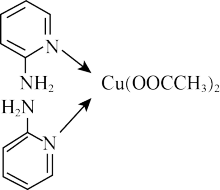

A.Cu原子的价电子排布图为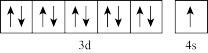 |
| B.组成该配合物的第二周期元素的电负性大小顺序为N>O>C |
| C.所有N原子的杂化方式相同,所有C原子的杂化方式也相同 |
D.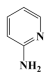 分子中可能有13个原子在同一平面上 分子中可能有13个原子在同一平面上 |
您最近一年使用:0次
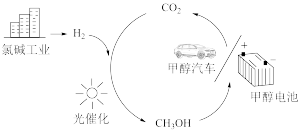
10 . 科学家进行如图所示的 制备及应用的研究,下列说法不正确的是
制备及应用的研究,下列说法不正确的是
 制备及应用的研究,下列说法不正确的是
制备及应用的研究,下列说法不正确的是
A. 中C原子的杂化类型为 中C原子的杂化类型为 |
B.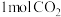 含有约 含有约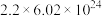 个电子 个电子 |
C. 和 和 合成甲醇符合原子利用率100% 合成甲醇符合原子利用率100% |
| D.图中涉及反应包含非极性键的断裂和生成 |
您最近一年使用:0次
2022-12-22更新
|
691次组卷
|
3卷引用:河北省部分学校2022-2023学年高三上学期期末考试变式汇编(1-9)



