1 . 如表为四种短周期元素的相关信息
回答下列问题(注:涉及元素的均要用对应元素的元素符号书写作答)
(1)Y元素的最简单氢化物的空间构型是___ 。
(2)Z、Q、R相比,其原子半径由大到小的顺序是___ 。
(3)最高价的R与Z元素组成的化合物中R原子的杂化方式为___ ,其中R在周期表中的位置是__ ,R的基态原子电子排布式为___ 。
(4)与O3分子互为等电子体的一种分子为___ ,阴离子为__ 。
(5)Y与R相比,非金属性较强的是___ ,能证明这一结论的事实是___ 。(用化学方程式表示)
| 元素 | 元素的相关信息 |
| Y | 原子最外层电子数是次外层电子数的2倍 |
| Z | 地壳中含量最多的元素 |
| Q | 短周期中金属性最强 |
| R | 常温下,R的单质是淡黄色固体,常在火山喷口附近沉积 |
(1)Y元素的最简单氢化物的空间构型是
(2)Z、Q、R相比,其原子半径由大到小的顺序是
(3)最高价的R与Z元素组成的化合物中R原子的杂化方式为
(4)与O3分子互为等电子体的一种分子为
(5)Y与R相比,非金属性较强的是
您最近一年使用:0次
名校
2 . 锰及其化合物用途非常广泛。回答下列问题:
(1)Al70Pd21Mn9是一种准晶体(介于晶体和非晶体之间的固体),能准确证明其不是晶体的方法是___________ 。
(2)基态Mn原子的价电子排布式为_________ ,未成对电子数为_____ 个。
(3)MnS熔点(1610℃)比MnO熔点(1650℃)低,其原因是____________ 。
(4)锰的一种配合物的化学式为[Mn(CO)5(CH3CN)]Br。
①配合物中锰元素的价态为________ 。
②配体CH3CN与中心原子形成配位键时,提供孤对电子的原子是_____ ,该分子中碳原子的杂化方式为_______ ;C、H、N的电负性从大到小的顺序为________ 。
(5)锰的含氧酸有HMnO4(高锰酸)、H2MnO3(亚锰酸),高锰酸的酸性比亚锰酸强,理由是_________ 。
(6)某种含锰特殊材料的晶胞结构如下图所示:
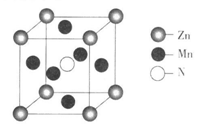
若晶胞参数为a nm,用NA表示阿伏伽德罗常数的值,则该晶胞的密度为____ ( 列出代数式即可)。
(1)Al70Pd21Mn9是一种准晶体(介于晶体和非晶体之间的固体),能准确证明其不是晶体的方法是
(2)基态Mn原子的价电子排布式为
(3)MnS熔点(1610℃)比MnO熔点(1650℃)低,其原因是
(4)锰的一种配合物的化学式为[Mn(CO)5(CH3CN)]Br。
①配合物中锰元素的价态为
②配体CH3CN与中心原子形成配位键时,提供孤对电子的原子是
(5)锰的含氧酸有HMnO4(高锰酸)、H2MnO3(亚锰酸),高锰酸的酸性比亚锰酸强,理由是
(6)某种含锰特殊材料的晶胞结构如下图所示:

若晶胞参数为a nm,用NA表示阿伏伽德罗常数的值,则该晶胞的密度为
您最近一年使用:0次
2018-05-17更新
|
386次组卷
|
2卷引用:河北省石家庄精英中学2020-2021学年高二下学期期末考试化学试题
名校
3 . 下列有关 和
和 的说法正确的是
的说法正确的是
 和
和 的说法正确的是
的说法正确的是A. 和 和 的空间结构都是三角锥形 的空间结构都是三角锥形 |
B. 和 和 的中心原子的价层电子对数均为4 的中心原子的价层电子对数均为4 |
C. 和 和 形成的化合物 形成的化合物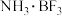 ,中各原子最外层都达到8电子稳定结构 ,中各原子最外层都达到8电子稳定结构 |
D. 中N原子上的孤电子对数为1, 中N原子上的孤电子对数为1, 中B原子上无孤电子对 中B原子上无孤电子对 |
您最近一年使用:0次
名校
4 . 目前新冠肺炎的药物研发和疫苗研制取得了很大进展,其中法匹拉韦药物(结构如图)显示有一定的临床疗效。下列关于此物质的说法不正确的是
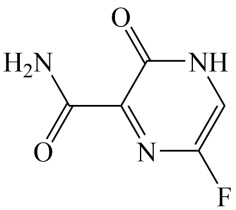

| A.由5种元素组成 |
| B.能发生水解反应和消去反应 |
| C.能使酸性KMnO4溶液褪色 |
| D.3个N原子的杂化方式相同 |
您最近一年使用:0次
名校
解题方法
5 . 磷及其化合物在电池、催化等领域有重要应用。黑磷与石墨类似,也具有层状结构(图1)。 为大幅度提高锂电池的充电速率,科学家最近研发了黑磷-石墨复合负极材料,其单层结构俯视图如图2所示。
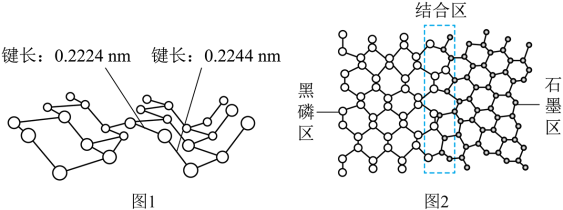
回答下列问题:
(1)Li、C、P三种元素中,电负性最小的是_________________ (用元素符号作答)。
(2)基态磷原子价电子排布式为________________ 。
(3)图2黑磷区中P原子的杂化方式为_________________ ,石墨区中C原子的杂化方式为____________ 。
(4)氢化物PH3、CH4、NH3的沸点由高到低顺序为________________ 。
(5)根据图1和图2的信息,下列说法正确的有________ (填字母)。
A. 黑磷区中P-P键的键能不完全相同
B. 黑磷与石墨都属于混合型晶体
C. 由石墨与黑磷制备该复合材料的过程,发生了化学反应
D. 石墨与黑磷的交界结合区域中,P原子与C原子共平面
E. 复合材料单层中,P原子与C原子之间的作用力属范德华力
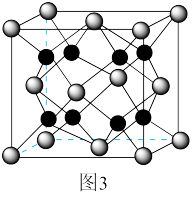
(6)贵金属磷化物Rh2P (化学式量为237)可用作电解水的高效催化剂,其立方晶胞如图3所示。已知晶胞参数为anm,晶体中与P距离最近的Rh的数目为___________________ , 晶体的密度为__________ g·cm-3(列出计算式)。

回答下列问题:
(1)Li、C、P三种元素中,电负性最小的是
(2)基态磷原子价电子排布式为
(3)图2黑磷区中P原子的杂化方式为
(4)氢化物PH3、CH4、NH3的沸点由高到低顺序为
(5)根据图1和图2的信息,下列说法正确的有
A. 黑磷区中P-P键的键能不完全相同
B. 黑磷与石墨都属于混合型晶体
C. 由石墨与黑磷制备该复合材料的过程,发生了化学反应
D. 石墨与黑磷的交界结合区域中,P原子与C原子共平面
E. 复合材料单层中,P原子与C原子之间的作用力属范德华力
(6)贵金属磷化物Rh2P (化学式量为237)可用作电解水的高效催化剂,其立方晶胞如图3所示。已知晶胞参数为anm,晶体中与P距离最近的Rh的数目为

您最近一年使用:0次
2021-05-28更新
|
735次组卷
|
9卷引用:河北省石家庄市第二十四中学2020-2021学年高二第二学期期中考试化学试题
河北省石家庄市第二十四中学2020-2021学年高二第二学期期中考试化学试题广东省2021年普通高中学业水平选择考适应性测试化学试题(已下线)难点10 物质结构与性质综合题-2021年高考化学【热点·重点·难点】专练(新高考)湖南省长沙市第一中学2021-2022学年高三上学期月考化学试题(已下线)3.3.2 过渡晶体和混合型晶体-2021-2022学年高二化学课后培优练(人教版2019选择性必修2)广东省深圳外国语学校2021-2022学年下学期高三第二次检测考试化学试题(已下线)专题19 物质结构与性质-2022年高考化学二轮复习重点专题常考点突破练湖南省株洲市攸县第一中学2022届高三下学期四月月考化学试题广东省惠州市惠州中学2022-2023学年高二下学期化学考试题
名校
6 . 世上首个五氮阴离子盐(N5)6(H3O)3(NH4)4Cl(用M代表)是我国研制出来的。
(1)元素的基态气态原子得到一个电子形成气态负一价离子时所放出的能量为第一电子亲和能(E1),下列说法错误的是___________ 。(填标号)
A.E1:C<O<F
B.沸点: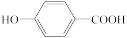 <
< 
C.甲醛中碳氢键间夹角小于苯中的键角
D.尿素CO(NH2)2中碳原子和氮原子均为sp2杂化
(2)M晶体的部分结构如下图。

①关于M中两阳离子的叙述正确的为___________ 。(填标号)
A.中心原子的杂化类型不同 B.中心原子的价层电子对数不同
C.立体结构相同 D.化学键类型相同
E.键角H3O+更大 F.H3O+中键的极性更大
②分子(或离子)中大π键可表示为π ,右下角m为参与形成大π键的原子数,右上角n为参与形成大π键的电子数(如苯中m=6,n=6),将M中阴离子N
,右下角m为参与形成大π键的原子数,右上角n为参与形成大π键的电子数(如苯中m=6,n=6),将M中阴离子N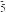 的大π键表示成π
的大π键表示成π ,则m+n的数值为
,则m+n的数值为___________ 。
(3)SO 的空间构型是
的空间构型是___________ ,请写出一种与它互为等电子体的分子___________ 。
(4)(CN)2分子为对称拟卤素,某些化学性质与卤素相似,其电子式为___________ ,中心原子的杂化方式为___________ 。
(5)氨水中存在氢键,请写出一水合氨分子最有可能的结构式:___________ 。
(6)1 mol 1,4-环己二烯 中σ键的个数为
中σ键的个数为___________ 。
(1)元素的基态气态原子得到一个电子形成气态负一价离子时所放出的能量为第一电子亲和能(E1),下列说法错误的是
A.E1:C<O<F
B.沸点:
 <
< 
C.甲醛中碳氢键间夹角小于苯中的键角
D.尿素CO(NH2)2中碳原子和氮原子均为sp2杂化
(2)M晶体的部分结构如下图。

①关于M中两阳离子的叙述正确的为
A.中心原子的杂化类型不同 B.中心原子的价层电子对数不同
C.立体结构相同 D.化学键类型相同
E.键角H3O+更大 F.H3O+中键的极性更大
②分子(或离子)中大π键可表示为π
 ,右下角m为参与形成大π键的原子数,右上角n为参与形成大π键的电子数(如苯中m=6,n=6),将M中阴离子N
,右下角m为参与形成大π键的原子数,右上角n为参与形成大π键的电子数(如苯中m=6,n=6),将M中阴离子N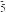 的大π键表示成π
的大π键表示成π ,则m+n的数值为
,则m+n的数值为(3)SO
 的空间构型是
的空间构型是(4)(CN)2分子为对称拟卤素,某些化学性质与卤素相似,其电子式为
(5)氨水中存在氢键,请写出一水合氨分子最有可能的结构式:
(6)1 mol 1,4-环己二烯
 中σ键的个数为
中σ键的个数为
您最近一年使用:0次
解题方法
7 . 碳、氮及其化合物广泛存在于自然界中,回答下列问题:
(1)科学家已证实,存在一种空心且类似于足球结构的物质N60,它可能成为一种很好的火箭燃料。固态N60的晶体类型为_______ 。
(2)氰酸是一种无机物,化学式为HCNO,是一种具有挥发性和腐蚀性的液体,高毒。HCNO的组成元素中第一电离能最小的是_______ (填元素符号,下同),电负性最大的是_______ 。
(3)镍能形成多种配合物,如正四面体形的Ni(CO)4,、正方形的 和正八面体形的
和正八面体形的 。下列说法不正确的是
。下列说法不正确的是_______ (填标号)。
A. CO分子内σ键和π键的数目之比为1:2
B. NH3的空间构型为平面三角形
C. Ni2+在形成配合物时,其配位数可能为4或6
D. Ni(CO)4和 中,镍元素均是sp3杂化
中,镍元素均是sp3杂化
(4)化合物(CH3)3N能溶于水,其原因是_______ ,(CH3)3N与盐酸反应生成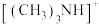 ,
,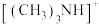 中新生成的化学键的类型为
中新生成的化学键的类型为_______ 。
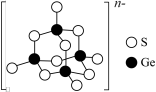
(5)阳离子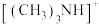 和阴离子A按个数比4:1组成化合物,阴离子A的结构如图所示,则S原子的杂化轨道类型是
和阴离子A按个数比4:1组成化合物,阴离子A的结构如图所示,则S原子的杂化轨道类型是_______ ,阴离子A的化学式为_______ 。
(6)某碳单质的晶胞结构如图所示,回答下列问题:

①该晶胞中含_______ 个C原子。
②将每个C原子视为一个球,若C原子的半径为R,1个C原子的体积为V,1个晶胞的体积为V0,堆积系数 ,则该晶体的堆积系数
,则该晶体的堆积系数
_______ (保留1位有效数字,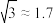 ,
, )。(提示:图中箭头标记的两个原子是相切的,两个原子球心分别位于立方体晶胞顶点和立方体晶胞体对角线的四等分点)
)。(提示:图中箭头标记的两个原子是相切的,两个原子球心分别位于立方体晶胞顶点和立方体晶胞体对角线的四等分点)
(1)科学家已证实,存在一种空心且类似于足球结构的物质N60,它可能成为一种很好的火箭燃料。固态N60的晶体类型为
(2)氰酸是一种无机物,化学式为HCNO,是一种具有挥发性和腐蚀性的液体,高毒。HCNO的组成元素中第一电离能最小的是
(3)镍能形成多种配合物,如正四面体形的Ni(CO)4,、正方形的
 和正八面体形的
和正八面体形的 。下列说法不正确的是
。下列说法不正确的是A. CO分子内σ键和π键的数目之比为1:2
B. NH3的空间构型为平面三角形
C. Ni2+在形成配合物时,其配位数可能为4或6
D. Ni(CO)4和
 中,镍元素均是sp3杂化
中,镍元素均是sp3杂化(4)化合物(CH3)3N能溶于水,其原因是
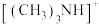 ,
,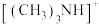 中新生成的化学键的类型为
中新生成的化学键的类型为(5)阳离子
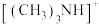 和阴离子A按个数比4:1组成化合物,阴离子A的结构如图所示,则S原子的杂化轨道类型是
和阴离子A按个数比4:1组成化合物,阴离子A的结构如图所示,则S原子的杂化轨道类型是
(6)某碳单质的晶胞结构如图所示,回答下列问题:

①该晶胞中含
②将每个C原子视为一个球,若C原子的半径为R,1个C原子的体积为V,1个晶胞的体积为V0,堆积系数
 ,则该晶体的堆积系数
,则该晶体的堆积系数
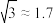 ,
, )。(提示:图中箭头标记的两个原子是相切的,两个原子球心分别位于立方体晶胞顶点和立方体晶胞体对角线的四等分点)
)。(提示:图中箭头标记的两个原子是相切的,两个原子球心分别位于立方体晶胞顶点和立方体晶胞体对角线的四等分点)
您最近一年使用:0次
2021-07-15更新
|
150次组卷
|
2卷引用:河北省部分名校2020-2021学年高二下学期期末联考化学试题
8 . 正氰酸(H-O-C≡N)与异氰酸(H-N=C=O)、雷酸(H-O-N≡C)互为同分异构体,均可以与氨水形成相应铵盐。下列说法错误的是
| A.三种酸的分子均能形成分子间氢键 |
| B.三种酸的分子中,氧原子的杂化方式相同 |
| C.三种酸的组成元素中,氧的电负性最大 |
| D.三种酸的铵盐中,只有雷酸铵的阴、阳离子均含有配位键 |
您最近一年使用:0次
名校
解题方法
9 . 三草酸合铁酸钾(K3[Fe(C2O4)3]·3H2O)是制备铁触媒的主要原料。该配合物在光照下发生分解:2K3[Fe(C2O4)3]·3H2O 3K2C2O4+2FeC2O4+2CO2↑+6H2O。下列说法错误的是
3K2C2O4+2FeC2O4+2CO2↑+6H2O。下列说法错误的是
 3K2C2O4+2FeC2O4+2CO2↑+6H2O。下列说法错误的是
3K2C2O4+2FeC2O4+2CO2↑+6H2O。下列说法错误的是| A.Fe3+的最高能层电子排布式为3d5 |
| B.铁元素位于第4周期VIIIB族 |
C. 中C原子的杂化方式为sp2 中C原子的杂化方式为sp2 |
| D.CO2分子中键和键数目比为1:1 |
您最近一年使用:0次
2021-04-10更新
|
185次组卷
|
3卷引用:河北省河间市第十四中学2020-2021学年高二下学期期中考试化学试题
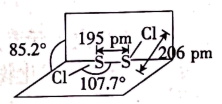
10 . 二氯化二硫(结构如图所示)遇水产生能使品红溶液褪色的气体,一种制备 的方法为
的方法为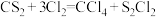 。下列说法不正确的是
。下列说法不正确的是
 的方法为
的方法为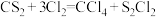 。下列说法不正确的是
。下列说法不正确的是
A. 分子中既含极性键又含非极性键 分子中既含极性键又含非极性键 |
B. 、 、 、 、 、 、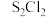 均为非极性分子 均为非极性分子 |
C. 、 、 、 、 的中心原子的杂化方式依次为 的中心原子的杂化方式依次为 、 、 、 、 |
D. 中σ键与π键的数目之比为1:1 中σ键与π键的数目之比为1:1 |
您最近一年使用:0次



