名校
解题方法
1 . 下列实验方案设计、现象和结论都正确的是
| 选项 | 实验目的 | 实验方案设计 | 现象和结论 |
| A | 检验溴乙烷是否水解 | 向溴乙烷中加入氢氧化钠溶液共热,滴加硝酸银溶液 | 未出现浅黄色沉淀,证明溴乙烷未发生水解 |
| B | 探究不同价态硫元素的转化 | 向Na2SO3和Na2S的混合溶液中加入浓硫酸 | 溶液变浑浊,证明 和S2-发生了氧化还原反应 和S2-发生了氧化还原反应 |
| C | 实验室中制取并检验乙烯 | 取4mL乙醇,加入12mL浓硫酸及少量沸石,逐渐升温至170℃,将产生的气体依次通过品红和溴水 | 溴水褪色,说明产物中有乙烯生成 |
| D | 验证Cl-与H2O在配合中存在相互竞争 | 向0.1mol·L-1CuSO4溶液中加入少量NaCl固体 | 溶液由蓝色变为黄绿色,说明发生了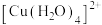 到 到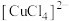 的转化 的转化 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
2 . 粉煤灰是燃煤电厂排出的工业废渣,开展粉煤灰综合利用,变废为宝,具有很高的社会和经济效益。某电厂的粉煤灰主要化学成分是 和
和 ,还含有少量的
,还含有少量的 和
和 等,一种从高铝粉煤灰中提取铝的工艺流程如下:
等,一种从高铝粉煤灰中提取铝的工艺流程如下:

已知①“焙烧”时,粉煤灰中的硅、铝转化为 ,它能与酸反应。
,它能与酸反应。
②某离子沉淀完全时,其浓度不大于 。
。
回答下列问题:
(1)“焙烧”前将粉煤灰和碳酸钠固体混合粉磨的目的是___________ ,使得反应更快更完全;“焙烧”生成 的化学方程式为
的化学方程式为___________ 。
(2)原硅酸 不稳定易脱水分解,
不稳定易脱水分解, 中
中 的杂化方式为
的杂化方式为___________ ;“浸渣1”的主要成分是 、
、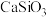 和
和___________ ,其中,基态氧原子的电子排布式___________ 。
(3)“调 ”目的是将
”目的是将 、
、 沉淀完全且其他金属离子不沉淀,则“溶液1”中
沉淀完全且其他金属离子不沉淀,则“溶液1”中 浓度为
浓度为___________  (已知25℃时,
(已知25℃时, )。
)。
(4)“碱溶”时,反应的离子方程式为___________ 。
(5)“ 晶种”为细小的晶体颗粒,有利于
晶种”为细小的晶体颗粒,有利于 析出,“溶液2”的阴离子有
析出,“溶液2”的阴离子有___________ 和___________ 。
(6)工业上获取金属铝需用到助熔剂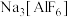 ,实验证明,硼原子则常与
,实验证明,硼原子则常与 形成
形成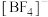 ,相同的配体
,相同的配体 ,B配位数较少的主要原因是
,B配位数较少的主要原因是___________ 。
(7)金属铝的晶胞结构如图甲所示,原子之间相互位置关系的平面图如图乙所示,已知 的原子半径为
的原子半径为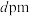 ,
, 为阿伏加德罗常数的值。
为阿伏加德罗常数的值。

该晶体内 原子的配位数为
原子的配位数为___________ ,晶体的密度为___________  。(用含d和
。(用含d和 的代数式表示)
的代数式表示)
 和
和 ,还含有少量的
,还含有少量的 和
和 等,一种从高铝粉煤灰中提取铝的工艺流程如下:
等,一种从高铝粉煤灰中提取铝的工艺流程如下:
已知①“焙烧”时,粉煤灰中的硅、铝转化为
 ,它能与酸反应。
,它能与酸反应。②某离子沉淀完全时,其浓度不大于
 。
。回答下列问题:
(1)“焙烧”前将粉煤灰和碳酸钠固体混合粉磨的目的是
 的化学方程式为
的化学方程式为(2)原硅酸
 不稳定易脱水分解,
不稳定易脱水分解, 中
中 的杂化方式为
的杂化方式为 、
、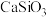 和
和(3)“调
 ”目的是将
”目的是将 、
、 沉淀完全且其他金属离子不沉淀,则“溶液1”中
沉淀完全且其他金属离子不沉淀,则“溶液1”中 浓度为
浓度为 (已知25℃时,
(已知25℃时, )。
)。(4)“碱溶”时,反应的离子方程式为
(5)“
 晶种”为细小的晶体颗粒,有利于
晶种”为细小的晶体颗粒,有利于 析出,“溶液2”的阴离子有
析出,“溶液2”的阴离子有(6)工业上获取金属铝需用到助熔剂
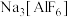 ,实验证明,硼原子则常与
,实验证明,硼原子则常与 形成
形成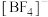 ,相同的配体
,相同的配体 ,B配位数较少的主要原因是
,B配位数较少的主要原因是(7)金属铝的晶胞结构如图甲所示,原子之间相互位置关系的平面图如图乙所示,已知
 的原子半径为
的原子半径为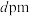 ,
, 为阿伏加德罗常数的值。
为阿伏加德罗常数的值。
该晶体内
 原子的配位数为
原子的配位数为 。(用含d和
。(用含d和 的代数式表示)
的代数式表示)
您最近一年使用:0次
名校
解题方法
3 . 现有六种元素,其中A、B、C、D、E为短周期主族元素,F为第四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题。
(1)某同学根据上述信息,推断A基态原子的核外电子排布图为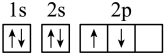 ,该同学所画的电子排布图违背了
,该同学所画的电子排布图违背了________ 。
(2)B元素的电负性_______ (填“大于”、“小于”或“等于”) C元素的电负性。B元素的第一电离能_______ ( 填“大于”、“小于”或“等于”) C元素的第一电离能。
(3)化合物AC和B的单质熔沸点较高的是_______ (填化学式),原因是___________________ 。
(4)E原子中电子占据的最高能层符号是______ ,该能层具有的原子轨道数为______ 。
(5)题中F元素位于元素周期表中的位置为______ ,位于_______ 区(填s、p、d、f或ds)。
(6)B、C的简单氢化物分子结合质子能力较强的是 (写化学式)___________ ,用一个离子方程式加以证明:_____________________ 。
| A元素形成的物质种类繁多,其形成的一种固体单质工业上常用作切割工具 |
| B元素原子的核外p电子数比s电子数少1 |
| C元素基态原子p轨道有两个未成对电子 |
| D原子的第一至第四电离能分别是:I1=738kJ·mol-1;I2=1451kJ·mol-1;I3=7733kJ·mol-1;I4=10540kJ·mol-1 |
| E原子核外所有p轨道全满或半满 |
| F在周期表的第6纵列 |
 ,该同学所画的电子排布图违背了
,该同学所画的电子排布图违背了(2)B元素的电负性
(3)化合物AC和B的单质熔沸点较高的是
(4)E原子中电子占据的最高能层符号是
(5)题中F元素位于元素周期表中的位置为
(6)B、C的简单氢化物分子结合质子能力较强的是 (写化学式)
您最近一年使用:0次
名校
解题方法
4 . 现有部分短周期元素的性质或原子结构如下表:
(1)元素T的原子最外层共有___________ 种不同运动状态的电子;元素X的一种同位素可测定文物年代,这种同位素的符号是___________ 。
(2)元素Y与氢元素形成一种离子YH ,写出该微粒的结构式
,写出该微粒的结构式___________ (用元素符号表示且体现配位键)。
(3)下列表述中能证明非金属性较强的是Z这一事实的是___________ 。
a.常温下Z的单质和T的单质状态不同
b.Z的氢化物比T的氢化物稳定
c.一定条件下Z和T的单质都能与氢氧化钠溶液反应
(4)探寻物质的性质差异性是学习的重要方法之一、T、X、Y、Z四种元素的最高价氧化物的水化物中化学性质明显不同于其他三种酸的是___________ (写化学式)。
| 元素编号 | 元素性质或原子结构 |
| T | M层上有2对成对电子 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| Z | 元素最高正价是+7价 |
(2)元素Y与氢元素形成一种离子YH
 ,写出该微粒的结构式
,写出该微粒的结构式(3)下列表述中能证明非金属性较强的是Z这一事实的是
a.常温下Z的单质和T的单质状态不同
b.Z的氢化物比T的氢化物稳定
c.一定条件下Z和T的单质都能与氢氧化钠溶液反应
(4)探寻物质的性质差异性是学习的重要方法之一、T、X、Y、Z四种元素的最高价氧化物的水化物中化学性质明显不同于其他三种酸的是
您最近一年使用:0次
5 . 向盛有硝酸银溶液的试管中加入氨水,首先形成难溶物,继续滴加氨水,难溶物溶解得到无色透明溶液,下列说法正确的是
A.反应后溶液中没有沉淀,所以反应前后 的浓度不变 的浓度不变 |
B.沉淀溶解后,生成的 难电离 难电离 |
C.在 中, 中, 给出孤对电子, 给出孤对电子, 提供空轨道 提供空轨道 |
D.该实验能证明 比 比 稳定 稳定 |
您最近一年使用:0次
2021-07-22更新
|
395次组卷
|
4卷引用:福建省德化一中、永安一中、漳平一中三校协作2021-2022学年高二下学期5月联考化学试题
福建省德化一中、永安一中、漳平一中三校协作2021-2022学年高二下学期5月联考化学试题辽宁省锦州市2020-2021学年高二下学期期末考试化学试题(已下线)第3.4讲 配合物与超分子-2021-2022学年高二化学链接教材精准变式练(人教版2019选择性必修2)(已下线)第22讲 沉淀溶解平衡的应用(word讲义)-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)
名校
6 . 反应 中有关物质的说法错误的是
中有关物质的说法错误的是
 中有关物质的说法错误的是
中有关物质的说法错误的是A.中心离子的电子排布式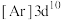 |
B. 分子与 分子与 分子间可形成氢键 分子间可形成氢键 |
| C.金属Cu晶体中的原子堆积方式为面心立方最密堆积 |
D.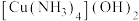 中,中心离子的配位数为4 中,中心离子的配位数为4 |
您最近一年使用:0次
7 . 以A和有机锌试剂(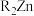 )为起始原料,通过催化偶联反应增长碳链的机理(部分步骤和产物省略)如图所示,下列说法错误的是
)为起始原料,通过催化偶联反应增长碳链的机理(部分步骤和产物省略)如图所示,下列说法错误的是
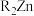 )为起始原料,通过催化偶联反应增长碳链的机理(部分步骤和产物省略)如图所示,下列说法错误的是
)为起始原料,通过催化偶联反应增长碳链的机理(部分步骤和产物省略)如图所示,下列说法错误的是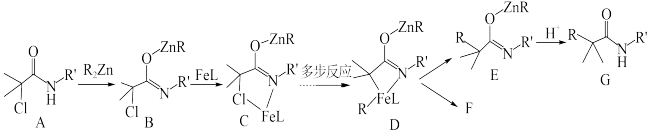
| A.F为催化剂,其化学式为FeL |
| B.B→C过程中Fe元素的化合价不变 |
| C.C中Cl和N均用p轨道上的电子与Fe形成配位键 |
D.总反应式为 |
您最近一年使用:0次
名校
8 . 2023年的诺贝尔化学奖授予了“发现和合成量子点”的三位科学家。下图是一种量子点的结构,下列说法不正确的是

A.基态原子第一电离能: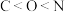 |
B.基态Se原子的价层电子排布式为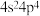 |
| C.该结构中C和N原子轨道的杂化类型相同 |
D.该结构中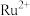 提供空轨道,N原子提供孤电子对 提供空轨道,N原子提供孤电子对 |
您最近一年使用:0次
2024-02-25更新
|
183次组卷
|
2卷引用:福建省三明市第一中学2023-2024学年高二下学期3月月考化学试题
名校
9 . 下列有关说法正确 的是
|
|
| A.电子云密度大的区域电子数目多 | B.晶胞中每个Cu原子周围有12个紧邻的原子 |
|
 晶胞结构 晶胞结构 |
| C.铜离子与氨分子之间形成离子键 | D.每个 晶胞平均占有8个 晶胞平均占有8个 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
10 . 某物质 A 的实验式为CoCl3·4NH3, 1molA 中加入足量的 AgNO3溶液中能生成1mol白色沉淀,以强碱处理并没有NH3放出,则关于此化合物的说法中不正确的是
| A.Co3+与NH3、Cl-形成配位键 | B.配合物配位数为6 |
| C.该配合物可能是平面正方形结构 | D.此配合物可写成[Co (NH3) 4Cl2]Cl |
您最近一年使用:0次