名校
解题方法
1 . 矾是一些金属硫酸盐的统称,其中皓矾的化学式为 ,可用作媒染剂、木材防腐剂。下图是
,可用作媒染剂、木材防腐剂。下图是 的结构示意图:
的结构示意图: 离子。
离子。
1. 分子的分子构型为
分子的分子构型为___________ ,中心原子杂化方式为___________ 杂化。
2. 的沸点
的沸点___________ (填>、<或=)水的沸点,原因可能是___________ 。
3. 中,
中, 与
与 间的作用力为
间的作用力为___________ , 与
与 间的作用力为
间的作用力为___________ 。
4. 与
与 中的中心原子均为
中的中心原子均为 杂化,
杂化, 中H—O—H键角
中H—O—H键角___________ (填>、<或=) 中O—S—O键角,原因是
中O—S—O键角,原因是___________ 。
5.写出 溶于氨水的化学方程式
溶于氨水的化学方程式___________ 。
6. 受热失水时,随着温度的升高,先失去一个水分子,变为
受热失水时,随着温度的升高,先失去一个水分子,变为 ,再失去其它的水,首先失去的水分子应为
,再失去其它的水,首先失去的水分子应为___________ (填①或②),原因是___________ 。
 ,可用作媒染剂、木材防腐剂。下图是
,可用作媒染剂、木材防腐剂。下图是 的结构示意图:
的结构示意图: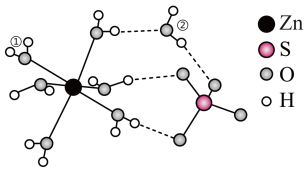
 离子。
离子。1.
 分子的分子构型为
分子的分子构型为2.
 的沸点
的沸点3.
 中,
中, 与
与 间的作用力为
间的作用力为 与
与 间的作用力为
间的作用力为4.
 与
与 中的中心原子均为
中的中心原子均为 杂化,
杂化, 中H—O—H键角
中H—O—H键角 中O—S—O键角,原因是
中O—S—O键角,原因是5.写出
 溶于氨水的化学方程式
溶于氨水的化学方程式6.
 受热失水时,随着温度的升高,先失去一个水分子,变为
受热失水时,随着温度的升高,先失去一个水分子,变为 ,再失去其它的水,首先失去的水分子应为
,再失去其它的水,首先失去的水分子应为
您最近一年使用:0次
解题方法
2 . 联氨(N2H4)又称肼,在航天、能源等领域具有广泛应用。
Ⅰ.N2H4分子中所有原子均达到稀有气体原子的稳定结构。
(1)写出N2H4的电子式。___________
(2)N2H4晶体受热熔化时,破坏的作用力有___________。
(3)酸碱质子理论提出:凡是能给出质子的分子或离子称为酸,凡是能接受质子的分子或离子称为碱。
①由N2H4+H2O N2H
N2H +OH- 可知N2H4是
+OH- 可知N2H4是___________ 。
A.酸 B.碱
②选择足量的盐酸或NaOH溶液与N2H4充分反应,生成盐的化学式为___________ 。
Ⅱ.肼具有强还原性,可作火箭推进剂燃料,反应的热化学方程式表示为:2N2H4(l)+N2O4(g)=3N2(g)+4H2O(g) ∆H<0。
(4)①结合化学反应原理分析,该反应可自发进行的原因是___________ 。
②N2H4和N2O4作为火箭推进剂的主要原因是___________ 。
Ⅲ.肼可还原钴离子制备纳米金属钴,纳米金属钴具有特殊的物理、化学和表面性质。
(5)下列状态的钴中,电离最外层一个电子所需能量最小的是_______ 。
A.[Ar]3d74s2 B.[Ar]3d74s14p1 C.[Ar]3d74s1
(6)Co2+被N2H4还原的离子方程式如下,完成方程式并配平_______ 。
 Co2++
Co2++ N2H4+
N2H4+ ___________=
___________= Co↓+
Co↓+ N2↑+
N2↑+ H2O
H2O
当转移7.224×1024个电子数时,生成金属钴___________ 克。
(7)金属钴可以形成多种配合物。一种配合物由Co3+、NH3、Cl-、H2O组成,实验显示Co3+、NH3、Cl-、H2O的物质的量之比为1∶3∶3∶1.向该配合物的水溶液加入AgNO3溶液,只能沉淀出三分之一的Cl-。
①该配合物的化学式是___________ 。
A.[Co(NH3)3ClH2O]Cl2 B.[Co(NH3)3Cl2H2O]Cl C.[Co(NH3)3H2O]Cl3
②该配合物的配体有___________ 。
Ⅰ.N2H4分子中所有原子均达到稀有气体原子的稳定结构。
(1)写出N2H4的电子式。
(2)N2H4晶体受热熔化时,破坏的作用力有___________。
| A.范德华力 | B.氢键 | C.共价键 | D.离子键 |
①由N2H4+H2O
 N2H
N2H +OH- 可知N2H4是
+OH- 可知N2H4是A.酸 B.碱
②选择足量的盐酸或NaOH溶液与N2H4充分反应,生成盐的化学式为
Ⅱ.肼具有强还原性,可作火箭推进剂燃料,反应的热化学方程式表示为:2N2H4(l)+N2O4(g)=3N2(g)+4H2O(g) ∆H<0。
(4)①结合化学反应原理分析,该反应可自发进行的原因是
②N2H4和N2O4作为火箭推进剂的主要原因是
Ⅲ.肼可还原钴离子制备纳米金属钴,纳米金属钴具有特殊的物理、化学和表面性质。
(5)下列状态的钴中,电离最外层一个电子所需能量最小的是
A.[Ar]3d74s2 B.[Ar]3d74s14p1 C.[Ar]3d74s1
(6)Co2+被N2H4还原的离子方程式如下,完成方程式并配平
 Co2++
Co2++ N2H4+
N2H4+ ___________=
___________= Co↓+
Co↓+ N2↑+
N2↑+ H2O
H2O当转移7.224×1024个电子数时,生成金属钴
(7)金属钴可以形成多种配合物。一种配合物由Co3+、NH3、Cl-、H2O组成,实验显示Co3+、NH3、Cl-、H2O的物质的量之比为1∶3∶3∶1.向该配合物的水溶液加入AgNO3溶液,只能沉淀出三分之一的Cl-。
①该配合物的化学式是
A.[Co(NH3)3ClH2O]Cl2 B.[Co(NH3)3Cl2H2O]Cl C.[Co(NH3)3H2O]Cl3
②该配合物的配体有
您最近一年使用:0次
名校
解题方法
3 . 硼酸(H3BO3)晶体结构为层状,其二维平面结构如图:______ mol氢键。
(2)硼酸是一元弱酸,它本身不给出H+,但与水作用后能给出H+。用离子方程式说明硼酸水溶液呈酸性的原因为_______ 。

(2)硼酸是一元弱酸,它本身不给出H+,但与水作用后能给出H+。用离子方程式说明硼酸水溶液呈酸性的原因为
您最近一年使用:0次
名校
解题方法
4 . 一种含Se的新型AIE分子(IV)的合成路线如图:_______ 。
(2)IV中具有孤电子对的原子有_______ 。
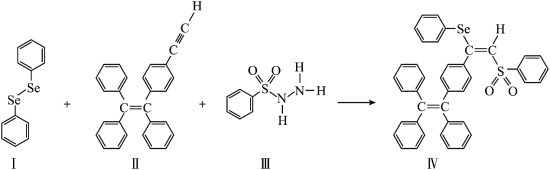
| A.I中仅有σ键 |
| B.I中的Se-Se为非极性共价键 |
| C.II易溶于水 |
| D.II中原子的杂化轨道类型只有sp、sp2、sp3 |
| A.C | B.O | C.S | D.Se |
您最近一年使用:0次
名校
解题方法
5 . 羰基铁[Fe(CO)5]广泛用于催化剂,汽油抗爆剂等,为黄色粘稠状液体,熔点为-20℃,沸点为103℃,60℃在空气中可自燃,其结构和部分键长如图所示。
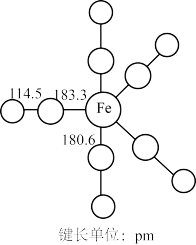
(1)Fe(CO)5晶体类型为___________ 。(填“离子晶体”或“分子晶体”)
(2)下列说法正确的是___________。

(1)Fe(CO)5晶体类型为
(2)下列说法正确的是___________。
| A.中心Fe原子可能采取sp3杂化 | B.配体与Fe原子所形成的配位键的键能相同 |
| C.Fe在周期表中位于Ⅷ族,属于d区元素 | D.制备Fe(CO)5应在隔绝空气的条件下进行 |
您最近一年使用:0次
6 . 短周期主族元素W、X、Y、Z的原子序数依次增大,四种元素形成的化合物甲的结构为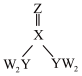 ,其中各原子的最外层均处于稳定结构。W与X、Y、Z均可形成电子数相等的分子,
,其中各原子的最外层均处于稳定结构。W与X、Y、Z均可形成电子数相等的分子,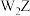 常温常压下为液体。下列说法正确的是
常温常压下为液体。下列说法正确的是
A.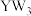 分子中的键角为120° 分子中的键角为120° | B. 的稳定性大于 的稳定性大于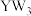 |
| C.物质甲的1个分子中存在6个σ键 | D.Y元素的氧化物对应的水化物为强酸 |
您最近一年使用:0次
2022-08-28更新
|
3290次组卷
|
18卷引用:上海市华东师范大学附属东昌中学2023-2024学年高三上学期第四次测试化学试卷
上海市华东师范大学附属东昌中学2023-2024学年高三上学期第四次测试化学试卷山东省泰安市2020届高三一轮检测试题化学试题山东省泰安市2020届高三第三次模拟试卷化学试题河北省张家口市宣化一中2020-2021学年高二下学期期初考试化学试题吉林省辽源市田家炳高级中学2020-2021学年高二下学期期中化学试题福建省三明市五县2021-2022学年高二下学期联合质检考试(期中)化学试题全书综合评测(已下线)第30讲 分子结构与性质(练)-2023年高考化学一轮复习讲练测(新教材新高考)广东省东莞市第四高级中学2022-2023学年高二上学期期中考试化学试题陕西省西安市铁一中学2022-2023学年高三上学期1月期末考试化学试题湖南省长沙市周南中学2022-2023学年高二上学期期末考试化学试题广东省东莞市七校2022-2023学年高二上学期(12月)期中考试化学试题宁夏银川市唐徕中学2022-2023学年高二下学期期中考试化学试题广东省广州市第十六中学2022-2023学年高二下学期5月月考化学试题福建省泉州市铭选中学 泉州九中 侨光中学三校2022-2023学年高二下学期7月期末化学试题江西省宜丰中学创新部2023-2024学年高二上学期第一次(10月)月考化学试题(已下线)第二章 分子结构与性质(A卷)贵州省安龙县第一中学2023-2024学年高二下学期第一次阶段考试化学试题
7 . 在CuSO4·5H2O晶体中( )
| A.存在水分子 | B.没有共价键 | C.只有离子键 | D.含有金属键 |
您最近一年使用:0次
8 . 关于[Cr(H2O)4Br2]Br·2H2O的说法正确的是( )
| A.配体为水分子,配位原子是O,外界为Br- | B.中心原子的配位数为6 |
| C.中心原子Cr采取sp3杂化 | D.中心原子的化合价为+2价 |
您最近一年使用:0次
2017-05-11更新
|
267次组卷
|
4卷引用:沪科版化学拓展性课程2《化学键和晶体结构》测试题



