名校
1 . 下列关于SO2、SO3、NH3、NH 说法中正确的是
说法中正确的是
 说法中正确的是
说法中正确的是| A.SO2水溶液能导电,SO2是电解质 | B.NH 中含有配位键 中含有配位键 |
| C.SO3中硫原子轨道杂化类型为sp3 | D.NH3为非极性分子 |
您最近一年使用:0次
2022高三·全国·专题练习
真题
解题方法
2 . 配位化合物X由配体L2-(如图)和具有正四面体结构的[Zn4O]6+构成。______ 。
(2)L2-所含元素中,电负性最大的原子处于基态时电子占据最高能级的电子云轮廓图为______ 形;每个L2-中采取sp2杂化的C原子数目为______ 个,C与O之间形成σ键的数目为______ 个。
(3)X晶体内部空腔可吸附小分子,要增强X与H2O的吸附作用,可在L2-上引入______ 。(假设X晶胞形状不变)。
(4)X晶体具有面心立方结构,其晶胞由8个结构相似的组成单元(如图)构成。______ 。
②X晶体中Zn2+的配位数为______ 。
③已知ZnO键长为dnm,理论上图中A、B两个Zn2+之间的最短距离的计算式为_____ nm。
④已知晶胞参数为2anm,阿伏加德罗常数的值为NA,L2-与[Zn4O]6+的相对分子质量分别为M1和M2,则X的晶体密度为_____ g•cm-3(列出化简的计算式)。
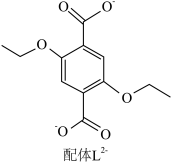
(2)L2-所含元素中,电负性最大的原子处于基态时电子占据最高能级的电子云轮廓图为
(3)X晶体内部空腔可吸附小分子,要增强X与H2O的吸附作用,可在L2-上引入
| A.-Cl | B.-OH | C.-NH2 | D.-CH3 |
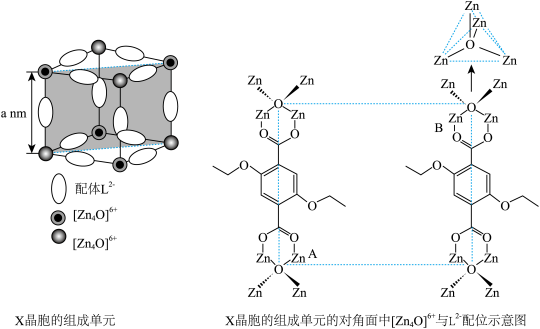
②X晶体中Zn2+的配位数为
③已知ZnO键长为dnm,理论上图中A、B两个Zn2+之间的最短距离的计算式为
④已知晶胞参数为2anm,阿伏加德罗常数的值为NA,L2-与[Zn4O]6+的相对分子质量分别为M1和M2,则X的晶体密度为
您最近一年使用:0次
解题方法
3 . 下列说法或图示表达错误的是
A.基态Zn2+价层电子的轨道表示式: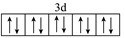 |
B.ClO 的VSEPR模型与离子的空间结构一致 的VSEPR模型与离子的空间结构一致 |
C.NaOH的电子式: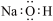 |
| D.在[Cd(NH3)4]2+中,NH3提供孤对电子,Cd2+提供空轨道 |
您最近一年使用:0次
解题方法
4 . DNA中四种碱基间的配对方式如图(~代表糖苷键,“ ”代表氢键),下列说法错误的是
”代表氢键),下列说法错误的是
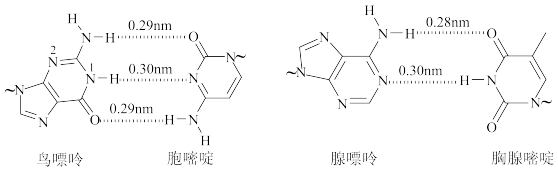
 ”代表氢键),下列说法错误的是
”代表氢键),下列说法错误的是
| A.基态原子的第一电离能:N>O | B. 与 与 通过配位键形成 通过配位键形成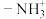 |
C.鸟嘌吟中1号N的杂化类型为 | D.鸟嘌吟中N—H键的平均键长大于0.29nm |
您最近一年使用:0次
名校
解题方法
5 . 有一种化学式为 的配位化合物,其阴离子结构如下图所示,关于该化合物的说法不正确的是
的配位化合物,其阴离子结构如下图所示,关于该化合物的说法不正确的是
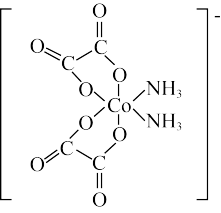
 的配位化合物,其阴离子结构如下图所示,关于该化合物的说法不正确的是
的配位化合物,其阴离子结构如下图所示,关于该化合物的说法不正确的是
| A.该化合物中,Co的化合价为+3 |
| B.该化合物中,Co的配位数为6 |
| C.该化合物中含有的作用力只包括极性键、非极性键、配位键 |
| D.该化合物中碳原子和氮原子的杂化方式不同 |
您最近一年使用:0次
2022-12-03更新
|
400次组卷
|
3卷引用:重庆市南开中学校2022-2023学年高三上学期第四次月考化学试题
名校
解题方法
6 . 复兴号高铁车体材质用到Mn、Co等元素。Mn的一种配合物化学式为[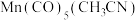 ],下列说法错误的是
],下列说法错误的是
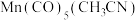 ],下列说法错误的是
],下列说法错误的是| A.该配合物中锰原子的配位数为6 |
B. 中C原子的杂化类型为 中C原子的杂化类型为 、 、 |
| C.该配合物中非金属原子的电负性大小为H<C<N<O |
D.等物质的量的 和CO中的π键数目之比为1∶1 和CO中的π键数目之比为1∶1 |
您最近一年使用:0次
2022-11-19更新
|
264次组卷
|
4卷引用:重庆市第八中学2023届高三上学期适应性月考卷(三)化学试题
解题方法
7 . 铁(Fe)、钴(Co)、铬(Ni)是第四周期第VⅢ族的元素,在化学上称为铁系元素,其化合物在生产生活中应用广泛。
(1)基态Co原子的核外电子排布式为___________ 。
(2)铁系元素能与CO形成 、
、 等金属羰基化合物。已知室温时
等金属羰基化合物。已知室温时 为浅黄色液体,沸点103℃,则
为浅黄色液体,沸点103℃,则 中含有的化学键类型包括___________。
中含有的化学键类型包括___________。
(3)以甲醇为溶剂, 可与色胺酮分子配位结合形成对DNA具有切割作用的色胺酮钴配合物(合成过程如下所示)。
可与色胺酮分子配位结合形成对DNA具有切割作用的色胺酮钴配合物(合成过程如下所示)。

①色胺酮分子中所含元素(C、N、O)第一电离能由小到大的顺序为___________ 。
②色氨酮分子中C原子的杂化类型为___________ 。
③X射线衍射分析显示色胺酮钴配合物晶胞中还含有一个CH3OH分子,CH3OH是通过___________ (填作用力)与色胺酮钴配合物相结合。
(4)Ge单晶具有金刚石型结构,其中Ge原子的杂化方式为___________ ,微粒之间存在的作用力是___________ 。
(5)晶胞有两个基本要素:
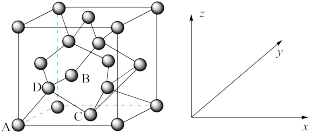
①原子坐标参数,表示晶胞内部各原子的相对位置。如图为Ge单晶的晶胞,其中原子坐标参数A为 ;B为
;B为 ;C为
;C为 。则D原子的坐标参数为
。则D原子的坐标参数为___________ 。
②晶胞参数,用于描述晶胞的大小和形状。已知Ge单晶的晶胞参数(棱长)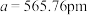 ,其密度为
,其密度为___________ g∙cm−3 (列出计算式即可,设NA为阿伏加德罗常数)。
(1)基态Co原子的核外电子排布式为
(2)铁系元素能与CO形成
 、
、 等金属羰基化合物。已知室温时
等金属羰基化合物。已知室温时 为浅黄色液体,沸点103℃,则
为浅黄色液体,沸点103℃,则 中含有的化学键类型包括___________。
中含有的化学键类型包括___________。| A.共价键 | B.离子键 | C.金属键 | D.配位键 |
 可与色胺酮分子配位结合形成对DNA具有切割作用的色胺酮钴配合物(合成过程如下所示)。
可与色胺酮分子配位结合形成对DNA具有切割作用的色胺酮钴配合物(合成过程如下所示)。
①色胺酮分子中所含元素(C、N、O)第一电离能由小到大的顺序为
②色氨酮分子中C原子的杂化类型为
③X射线衍射分析显示色胺酮钴配合物晶胞中还含有一个CH3OH分子,CH3OH是通过
(4)Ge单晶具有金刚石型结构,其中Ge原子的杂化方式为
(5)晶胞有两个基本要素:
①原子坐标参数,表示晶胞内部各原子的相对位置。如图为Ge单晶的晶胞,其中原子坐标参数A为
 ;B为
;B为 ;C为
;C为 。则D原子的坐标参数为
。则D原子的坐标参数为
②晶胞参数,用于描述晶胞的大小和形状。已知Ge单晶的晶胞参数(棱长)
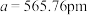 ,其密度为
,其密度为
您最近一年使用:0次
解题方法
8 . 一水合甘氨酸锌是一种矿物类饲料添加剂,其结构简式如图所示。下列说法错误的是


A.基态Zn原子价电子排布式为 |
B.Cu与Zn相邻,第一电离能: |
C.该物质中, 的配位数为5,配原子为O、N 的配位数为5,配原子为O、N |
D.电负性由小到大的顺序为 |
您最近一年使用:0次
2022-09-24更新
|
586次组卷
|
3卷引用:重庆第二十三中学校2021-2022学年高二下学期第一次月考化学试题
名校
解题方法
9 . 用图示的方法能够直观形象地传授化学知识,下列图示不正确的是
 | 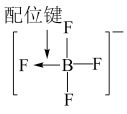 | 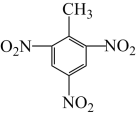 | 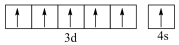 |
| A.铁原子的结构示意图 | B. 的结构式 的结构式 | C.TNT的结构简式 | D.铬原子的价层电子轨道表示式 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-09-09更新
|
216次组卷
|
2卷引用:重庆市主城区七校2021-2022学年高二下学期期末联考化学试题
解题方法
10 . 蛋白质主要由C、H、O、N四种化学元素组成,可能还会含有P、S等元素。铬是人体必需的微量元素。请回答下列有关问题:
(1)Cr的价层电子排布为_______ 。
(2)C、N、O三种元素第一电离能由大到小的顺序是_______ 。
(3)H、O、S三种元素电负性由小到大的顺序是_______ 。
(4)SO3分子的VSEPR模型名称为_______ , 空间结构名称是
空间结构名称是_______ 。
(5)化学式为CrCl3·6H2O的化合物有多种结构,其中一种可表示为[CrCl2(H2O)4]Cl·2H2O,该配合物中配位原子是_______ ,配位数为_______ 。
(6)H3O+中O原子的杂化类型是_______ ,H3O+中H—O—H键角_______ (填“>”“<”或“=”)H2O中H—O—H键角。
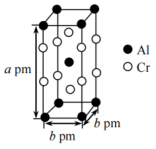
(7)铬和铝可形成 ,
, 具有体心四方结构,如图所示。设Cr和Al的原子半径分别为
具有体心四方结构,如图所示。设Cr和Al的原子半径分别为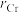 pm和
pm和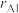 pm,则金属原子的空间占有率为
pm,则金属原子的空间占有率为_______ %(列出计算表达式)。
(1)Cr的价层电子排布为
(2)C、N、O三种元素第一电离能由大到小的顺序是
(3)H、O、S三种元素电负性由小到大的顺序是
(4)SO3分子的VSEPR模型名称为
 空间结构名称是
空间结构名称是(5)化学式为CrCl3·6H2O的化合物有多种结构,其中一种可表示为[CrCl2(H2O)4]Cl·2H2O,该配合物中配位原子是
(6)H3O+中O原子的杂化类型是
(7)铬和铝可形成
 ,
, 具有体心四方结构,如图所示。设Cr和Al的原子半径分别为
具有体心四方结构,如图所示。设Cr和Al的原子半径分别为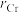 pm和
pm和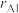 pm,则金属原子的空间占有率为
pm,则金属原子的空间占有率为
您最近一年使用:0次



