名校
1 . 近日,济南大学原长洲教授制备了一种高性能的钾离子电池负极材料(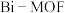 ),反应可简单表示为
),反应可简单表示为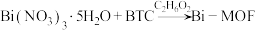 。回答下列问题:
。回答下列问题:
(1)铋(Bi)位于元素周期表中第6周期ⅤA族,基态Bi原子的价层电子排布式为___________ 。 中阴离子的立体构型为
中阴离子的立体构型为___________ 。基态O原子核外成对电子数与未成对电子数之比为___________ 。
(2)BTC分子中组成元素C、N、O的电负性由大到小排序为___________ 。 的沸点高于
的沸点高于 ,原因是
,原因是___________ 。
(3)冠醚是皇冠状的分子,可用不同大小的空穴适配不同大小的碱金属离子。18-冠-6(18指C、O原子总数为18,6指氧原子数)与钾离子形成的超分子结构如图所示。已知:超分子是由两种或两种以上的分子通过分子间相互作用形成的分子聚集体。超分子定义中的分子是广义的,包括离子。 原子的杂化类型为
原子的杂化类型为___________ 。
②下列叙述正确的是___________ (填字母)。
A.含该超分子的物质属于分子晶体 B.冠醚可用于分离不同的碱金属离子
C.中心碱金属离子的配位数固定不变 D.冠醚与碱金属离子之间形成氢键
(4)该电池负极材料(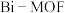 )充电时,会形成钾铋合金
)充电时,会形成钾铋合金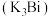 ,其晶胞结构如图,已知该晶胞底边长为
,其晶胞结构如图,已知该晶胞底边长为 ,高为
,高为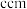 ,
, 为阿伏伽德罗常数的值。该晶体密度
为阿伏伽德罗常数的值。该晶体密度___________  (只列计算式)。
(只列计算式)。
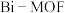 ),反应可简单表示为
),反应可简单表示为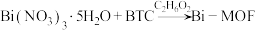 。回答下列问题:
。回答下列问题:(1)铋(Bi)位于元素周期表中第6周期ⅤA族,基态Bi原子的价层电子排布式为
 中阴离子的立体构型为
中阴离子的立体构型为(2)BTC分子中组成元素C、N、O的电负性由大到小排序为
 的沸点高于
的沸点高于 ,原因是
,原因是(3)冠醚是皇冠状的分子,可用不同大小的空穴适配不同大小的碱金属离子。18-冠-6(18指C、O原子总数为18,6指氧原子数)与钾离子形成的超分子结构如图所示。已知:超分子是由两种或两种以上的分子通过分子间相互作用形成的分子聚集体。超分子定义中的分子是广义的,包括离子。
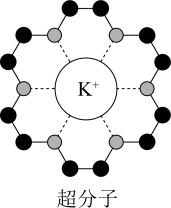
 原子的杂化类型为
原子的杂化类型为②下列叙述正确的是
A.含该超分子的物质属于分子晶体 B.冠醚可用于分离不同的碱金属离子
C.中心碱金属离子的配位数固定不变 D.冠醚与碱金属离子之间形成氢键
(4)该电池负极材料(
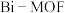 )充电时,会形成钾铋合金
)充电时,会形成钾铋合金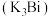 ,其晶胞结构如图,已知该晶胞底边长为
,其晶胞结构如图,已知该晶胞底边长为 ,高为
,高为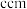 ,
, 为阿伏伽德罗常数的值。该晶体密度
为阿伏伽德罗常数的值。该晶体密度 (只列计算式)。
(只列计算式)。
您最近一年使用:0次
名校
2 .  主要用作颜料、釉料及磁性材料,一种利用含钴催化剂废料(主要含
主要用作颜料、釉料及磁性材料,一种利用含钴催化剂废料(主要含 、
、 ,还含有少量的
,还含有少量的 、
、 ,
, 、
、 、
、 )制备氧化钴
)制备氧化钴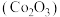 的工艺流程如图所示。
的工艺流程如图所示。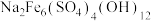 ;②金属钴与铁具有相似的化学性质;③氧化性
;②金属钴与铁具有相似的化学性质;③氧化性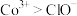 。
。
回答下列问题:
(1)钴元素基态原子的电子排布式为___________ 。
(2)“酸浸”时滤渣的主要成分为___________ (填化学式)。
(3)“除铁”时加入 溶液,
溶液, 的电子式为
的电子式为___________ 。
(4) 在空气中加热煅烧得到
在空气中加热煅烧得到 的化学方程式为
的化学方程式为___________ 。
(5)①钴被称为无机配合物之王,配合物 的中心离子的配位数为
的中心离子的配位数为___________ ,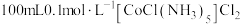 溶液中加入足量
溶液中加入足量 溶液,生成
溶液,生成___________ 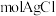 。
。
②钴的一种化合物的晶胞结构如图所示。 周围与其最近的
周围与其最近的 的个数为
的个数为___________ 。
 主要用作颜料、釉料及磁性材料,一种利用含钴催化剂废料(主要含
主要用作颜料、釉料及磁性材料,一种利用含钴催化剂废料(主要含 、
、 ,还含有少量的
,还含有少量的 、
、 ,
, 、
、 、
、 )制备氧化钴
)制备氧化钴 的工艺流程如图所示。
的工艺流程如图所示。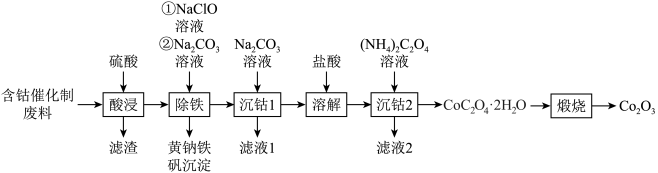
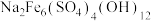 ;②金属钴与铁具有相似的化学性质;③氧化性
;②金属钴与铁具有相似的化学性质;③氧化性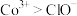 。
。回答下列问题:
(1)钴元素基态原子的电子排布式为
(2)“酸浸”时滤渣的主要成分为
(3)“除铁”时加入
 溶液,
溶液, 的电子式为
的电子式为(4)
 在空气中加热煅烧得到
在空气中加热煅烧得到 的化学方程式为
的化学方程式为(5)①钴被称为无机配合物之王,配合物
 的中心离子的配位数为
的中心离子的配位数为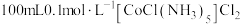 溶液中加入足量
溶液中加入足量 溶液,生成
溶液,生成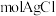 。
。②钴的一种化合物的晶胞结构如图所示。
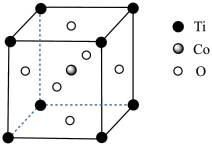
 周围与其最近的
周围与其最近的 的个数为
的个数为
您最近一年使用:0次
名校
3 . 冰晶石(Ng3AlF6)是电解铝工业的助熔剂、制造乳白色玻璃和搪瓷的遮光剂。制取冰晶石的反应为 ,下列有关化学用语表示正确的是
,下列有关化学用语表示正确的是
 ,下列有关化学用语表示正确的是
,下列有关化学用语表示正确的是A.基态Al原子的价层电子轨道表示式: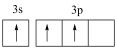 |
B.CO2的电子式: |
C.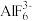 的结构式: 的结构式: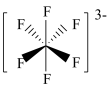 |
D. 的VSEPR模型: 的VSEPR模型: |
您最近一年使用:0次
7日内更新
|
202次组卷
|
3卷引用:甘肃省兰州市第二中学2023-2024学年高三下学期第十次月考化学试题
4 . 配合物在许多方面有着广泛的用途,目前我国科学家利用配合物在能源转化与储存方面有着杰出的贡献,请根据题意回答下列问题:(已知: 在溶液中为橙色,
在溶液中为橙色, 在溶液中为黄色)
在溶液中为黄色)
(1)下列反应曾用于检测司机是否酒后驾驶,原理如下:

基态Cr原子外围电子轨道表示式为___________ ;配合物 中与Cr3+形成配位键的原子是
中与Cr3+形成配位键的原子是___________ (填元素符号)。
(2)现有下列实验:___________ ,溶剂X可以是___________ (填名称),继续添加氨水,沉淀溶解的离子方程式为___________ 。
②该实验能说明NH3、H2O与Cu2+结合的能力由强到弱的顺序是___________ 。
(3)下列有关化学实验的“操作→现象→解释”均正确的是___________(填字母)。
 在溶液中为橙色,
在溶液中为橙色, 在溶液中为黄色)
在溶液中为黄色)(1)下列反应曾用于检测司机是否酒后驾驶,原理如下:

基态Cr原子外围电子轨道表示式为
 中与Cr3+形成配位键的原子是
中与Cr3+形成配位键的原子是(2)现有下列实验:

②该实验能说明NH3、H2O与Cu2+结合的能力由强到弱的顺序是
(3)下列有关化学实验的“操作→现象→解释”均正确的是___________(填字母)。
| 选项 | 操作 | 现象 | 解释 |
| A | 向某溶液中滴加KSCN溶液 | 产生红色沉淀 | 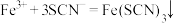 |
| B | 向由0.1mol CrCl3∙6H2O配成的溶液中加入足量AgNO3溶液 | 产生0.2mol沉淀 | 已知Cr3+的配位数为6,则CrCl3∙6H2O的化学式可表示为 |
| C | 向K2Cr2O7溶液中先滴加3滴浓硫酸,再改加10滴浓NaOH | 溶液先橙色加深,后变为黄色 | 溶液中存在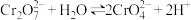 |
| D | 向AgCl悬浊液中滴加氨水 | 沉淀溶解 | AgCl不溶于水,但溶于氨水,重新电离成Ag+和Cl- |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
5 . 若X、Y两种粒子之间可形成配位键,则下列说法正确的是
| A.X、Y只能是分子 |
| B.X、Y只能是离子 |
| C.若X提供空轨道,则Y至少要提供一对孤电子对 |
| D.一定是X提供空轨道,Y提供孤电子对 |
您最近一年使用:0次
名校
6 . X、Y、Z、W是四种原子序数依次增大的前4周期元素,其中Y原子s能级电子数是其p能级电子数目的2倍,Z和Y位于同一周期,W位于ds区,其基态原子的价电子中有1个未成对电子,四种元素可形成如图所示的某离子。下列说法正确的是

| A.Z的第一电离能在同周期元素中最大 |
B.Y原子是 杂化,Z原子是 杂化,Z原子是 杂化 杂化 |
| C.该离子中W的配位数是4,配体数是2 |
| D.该离子中W的最外层电子数是1 |
您最近一年使用:0次
2024-05-27更新
|
101次组卷
|
2卷引用:2024届甘肃省民乐县第一中学高三下学期5月模拟考试化学试卷
7 . 某种离子液体的结构如图所示,X、Y、Z、M、Q为原子序数依次增大的短周期元素,Y、Z、M为同周期相邻元素,Z的原子序数等于X、Y原子序数之和,Q为非金属性最强的元素。下列说法正确的是
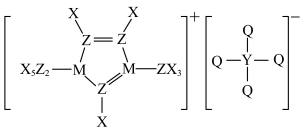
| A.该化合物中所有原子均为8电子结构 |
| B.由X、M、Q三种元素形成的化合物中只含有共价键、配位键 |
C.阴离子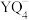 空间构型为正四面体形 空间构型为正四面体形 |
| D.氢化物的熔点:M>Z |
您最近一年使用:0次
名校
解题方法
8 . 化合物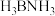 是一种潜在的储氢材料,它可由六元环状化合物
是一种潜在的储氢材料,它可由六元环状化合物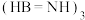 通过反应
通过反应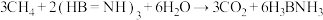 制得。下列叙述错误的是
制得。下列叙述错误的是
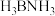 是一种潜在的储氢材料,它可由六元环状化合物
是一种潜在的储氢材料,它可由六元环状化合物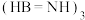 通过反应
通过反应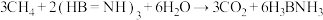 制得。下列叙述错误的是
制得。下列叙述错误的是A.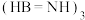 分子中所有的原子在同一平面上 分子中所有的原子在同一平面上 |
| B.反应前后N与B原子的杂化轨道类型不变 |
C. 、 、 均为含极性共价键的非极性分子 均为含极性共价键的非极性分子 |
D.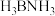 中N原子提供孤电子对与B原子形成配位键 中N原子提供孤电子对与B原子形成配位键 |
您最近一年使用:0次
2024-05-22更新
|
96次组卷
|
4卷引用:甘肃省白银市靖远县2024届高三下学期全真模拟化学试题
名校
解题方法
9 . 设 为阿伏加德罗常数的值。下列叙述正确的是
为阿伏加德罗常数的值。下列叙述正确的是
 为阿伏加德罗常数的值。下列叙述正确的是
为阿伏加德罗常数的值。下列叙述正确的是A.1mol 的中心原子价层电子对数为 的中心原子价层电子对数为 |
B.1L0.1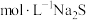 溶液中阴离子总数小于 溶液中阴离子总数小于 |
C.碱性氢氧燃料电池中每2.24L(标准状况)气体被氧化时转移电子数为 |
D.98g 中含有的配位键数为 中含有的配位键数为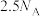 |
您最近一年使用:0次
2024-05-19更新
|
93次组卷
|
2卷引用:甘肃省张掖市某校2023-2024学年高三下学期模拟考试化学试题
10 . 某种含铜微粒可用于汽车尾气脱氮的催化剂,催化机理如下图所示。下列说法不正确的是
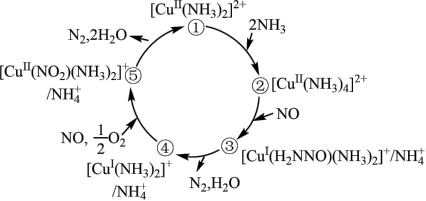
| A.图中所有铜的配合物中铜的配位数有2,3,4,6四种情况 |
B.在配离子 中, 中, 提供孤对电子, 提供孤对电子, 提供空轨道 提供空轨道 |
| C.状态③到状态④的变化过程中有O―H键的形成 |
D.该脱硝过程的总反应方程式为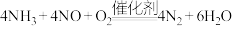 |
您最近一年使用:0次



