1 . 25℃,金属阳离子 与
与 逐步结合的平衡常数如下:
逐步结合的平衡常数如下:
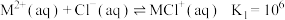


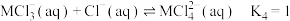
下列说法正确的是[已知:平均配位数
 与
与 逐步结合的平衡常数如下:
逐步结合的平衡常数如下: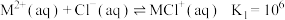


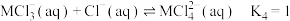
下列说法正确的是[已知:平均配位数

A.溶液中 数目越多, 数目越多,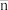 越大 越大 |
B.当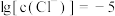 时, 时, 与 与 间不能形成配位键 间不能形成配位键 |
C.已知 ,可推知 ,可推知 的金属活动性强于 的金属活动性强于 |
D.当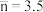 时,溶液中 时,溶液中 略大于 略大于 |
您最近一年使用:0次
2024高三下·浙江·专题练习
2 . Li、B、C、Ga等元素的单质或化合物在很多领域有广泛的应用。请回答:
(1)基态31Ga原子的价电子排布式为___________ 。
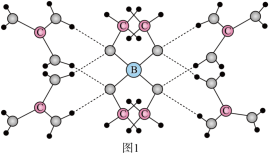
(2)一种含B化合物可用作吸附材料,其化学式为[C(NH2)3]4[B(OCH3)4]3Cl,部分晶体结构如图1所示,其中 [C(NH2)3]+为平面结构。不正确 的是___________。
(3)比较C-B-C键角大小:B(CH3)3___________ B(CH3)3(OCH3) (填“>”“=”或“<”),并说明理由___________ 。
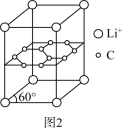
(4)一种锂离子电池负极材料为两层石墨层中嵌入Li+,形成如图2所示的晶胞结构。该物质的化学式可以表示为___________ ,Li+的配位数为___________ 。
(1)基态31Ga原子的价电子排布式为
(2)一种含B化合物可用作吸附材料,其化学式为[C(NH2)3]4[B(OCH3)4]3Cl,部分晶体结构如图1所示,其中 [C(NH2)3]+为平面结构。
| A.基态原子的第一电离能:C<N<O |
| B.基态原子未成对电子数:B<C<N<O |
| C.该晶体中存在的化学键有离子键、共价键、配位键、氢键 |
| D.晶体中B、C、N和O原子轨道的杂化类型分别为sp3、sp2、sp3、sp3 |
(3)比较C-B-C键角大小:B(CH3)3
(4)一种锂离子电池负极材料为两层石墨层中嵌入Li+,形成如图2所示的晶胞结构。该物质的化学式可以表示为
您最近一年使用:0次
3 . 下列说法不正确 的是
A.基态Cr原子的价层电子轨道式: |
B.共价化合物Al2Cl6中所有原子均满足8电子稳定结构,其结构式: |
C.N,N-二甲基甲酰胺: |
D.N2、N 、N4、N 、N4、N 互为同素异形体 互为同素异形体 |
您最近一年使用:0次
名校
解题方法
4 . 根据实验目的设计方案并进行实验,下列有关方案设计、实验现象或结论都正确的是
| 实验目的 | 方案设计 | 现象 | 结论 | |
| A | 比较Cu和Fe的金属性强弱 | 取同浓度的① 、② 、② 溶液,滴加同浓度氨水 溶液,滴加同浓度氨水 | ①先沉淀后溶解,②沉淀后不溶解 | 金属性:Cu<Fe |
| B | 检验己烯中的碳碳双键 | 取少量己烯,加入溴的四氯化碳溶液,振荡 | 上下两层均无色 | 己烯中含碳碳双键 |
| C | 比较配离子的稳定性 | 向盛有少量蒸馏水的试管里加2滴 ,然后再加2滴硫氰化钾溶液 ,然后再加2滴硫氰化钾溶液 | 溶液由黄色变血红色 |  与 与 形成的配离子更稳定 形成的配离子更稳定 |
| D | 比较温度对反应速率的影响 | 将2mL 0.1mol/L  溶液(A)浸入0℃水浴中、2mL 0.05mol/L 溶液(A)浸入0℃水浴中、2mL 0.05mol/L  溶液(B)浸入50℃水浴中,再同时滴加0.1mol/L稀硫酸2mL 溶液(B)浸入50℃水浴中,再同时滴加0.1mol/L稀硫酸2mL | B溶液比A溶液先出现浑浊 | 温度越高,反应速率越快 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
7日内更新
|
295次组卷
|
2卷引用:2024届浙江省金华市东阳市高三下学期三模化学试题
5 . 氮、铁及其化合物在生产生活中有重要应用。
(1)某化合物的晶胞如图,其化学式为_______ ,其阴离子存在_______ 种不同取向。
已知:3个及以上原子若处于共平面,如有彼此平行的p轨道,则可“肩并肩”重叠形成大π键
(3)南开大学某课题组合成无机二茂铁的配离子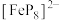 ,其中环状配体
,其中环状配体 以π电子参与配位,结构如图,1个该配离子中与
以π电子参与配位,结构如图,1个该配离子中与 形成配位键的电子共有
形成配位键的电子共有_______ 个。_______ 分子(填“极性”或“非极性”),①号N的碱性_______ ②号N的碱性(填“>”、“<”或“=”),请说明理由_______ 。
(1)某化合物的晶胞如图,其化学式为

| A.第二电离能:N>O>C | B.基态 的简化电子排布式[Ar] 的简化电子排布式[Ar]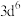 |
C.离子半径: | D.键角: |
已知:3个及以上原子若处于共平面,如有彼此平行的p轨道,则可“肩并肩”重叠形成大π键
(3)南开大学某课题组合成无机二茂铁的配离子
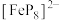 ,其中环状配体
,其中环状配体 以π电子参与配位,结构如图,1个该配离子中与
以π电子参与配位,结构如图,1个该配离子中与 形成配位键的电子共有
形成配位键的电子共有

您最近一年使用:0次
解题方法
6 . 威尔逊氏病是一种遗传性疾病,铜元素会在肝脏和其他组织内积聚。二巯基丙醇(Ⅰ: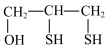 )能和铜结合成化合物Ⅱ:
)能和铜结合成化合物Ⅱ: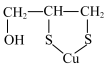 ,并通过尿液排出体外,故可用于治疗威尔逊氏病。
,并通过尿液排出体外,故可用于治疗威尔逊氏病。
(2)金属铜的化合物应用也十分广泛。如铜的某种氧化物广泛应用于太阳能电池领域。其晶胞如图所示:

②该晶胞为立方体,边长为anm,设
 为阿伏加德罗常数的值,则该晶胞的密度为
为阿伏加德罗常数的值,则该晶胞的密度为 。
。③下列说法正确的是
A.
 中的S原子均采取sp杂化
中的S原子均采取sp杂化B.
 中所有元素中S的电负性最大
中所有元素中S的电负性最大C.
 在水溶液中以
在水溶液中以 形式存在,
形式存在, 的配位原子为O
的配位原子为OD.
 和铜结合成
和铜结合成 ,是因为S的电负性比O小,更易与铜离子形成配位键
,是因为S的电负性比O小,更易与铜离子形成配位键(3)①水、②甲醇、③甲硫醇(
 )的沸点从大到小的顺序为
)的沸点从大到小的顺序为
您最近一年使用:0次
7 . 设 为阿伏加德罗常数的值。下列有关铁及其化合物说法正确的是
为阿伏加德罗常数的值。下列有关铁及其化合物说法正确的是
 为阿伏加德罗常数的值。下列有关铁及其化合物说法正确的是
为阿伏加德罗常数的值。下列有关铁及其化合物说法正确的是A. 与足量的 与足量的 反应,转移电子的数目为 反应,转移电子的数目为 |
B.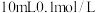 的 的 溶液中含有 溶液中含有 的数目为 的数目为 |
C.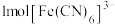 中含有 中含有 键的数目为 键的数目为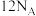 |
D. 基态 基态 中未成对电子的数目为 中未成对电子的数目为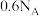 |
您最近一年使用:0次
2024-05-24更新
|
175次组卷
|
2卷引用:2024届浙江省高三下学期5月份大联考化学试题
8 . 某矿石的组成为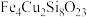 ,以此为原料实现如下转化:
,以此为原料实现如下转化:
请回答:
(1)下列说法正确的是________(填序号)。
(2) 与矿石中金属阳离子的配位能力由强到弱的顺序是
与矿石中金属阳离子的配位能力由强到弱的顺序是________ 。
(3)生成深蓝色溶液的化学方程式为________ 。
(4) 遇酸会迅速分解,请设计实验证明氧化产物与还原产物
遇酸会迅速分解,请设计实验证明氧化产物与还原产物________ 。 遇酸分解的离子方程式为
遇酸分解的离子方程式为________ 。
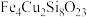 ,以此为原料实现如下转化:
,以此为原料实现如下转化:
请回答:
(1)下列说法正确的是________(填序号)。
A. 是由极性键形成的极性分子 是由极性键形成的极性分子 |
B.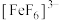 的氧化性弱于 的氧化性弱于 |
| C.矿石中Si与O形成相互独立的正四面体结构 |
D.固体A中含有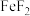 |
(2)
 与矿石中金属阳离子的配位能力由强到弱的顺序是
与矿石中金属阳离子的配位能力由强到弱的顺序是(3)生成深蓝色溶液的化学方程式为
(4)
 遇酸会迅速分解,请设计实验证明氧化产物与还原产物
遇酸会迅速分解,请设计实验证明氧化产物与还原产物 遇酸分解的离子方程式为
遇酸分解的离子方程式为
您最近一年使用:0次
名校
9 . 短周期主族元素X、Y、Z、M、Q分布在三个周期,原子序数依次增大。基态Y、Z、Q原子的核外未成对电子数之比为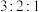 ,M的简单离子半径为同周期最小。下列说法不正确的是
,M的简单离子半径为同周期最小。下列说法不正确的是
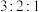 ,M的简单离子半径为同周期最小。下列说法不正确的是
,M的简单离子半径为同周期最小。下列说法不正确的是| A.X、Q简单阴离子所带电荷相同 |
B. 、 、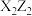 均为极性分子 均为极性分子 |
C.离子键百分数: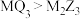 |
| D.Y、M均可作为配位键的成键原子 |
您最近一年使用:0次
名校
10 . 某学习小组以铝铁铜合金为主要原料制备 和
和 胶体粒子,流程如下:
胶体粒子,流程如下:
 和
和 胶体粒子,流程如下:
胶体粒子,流程如下: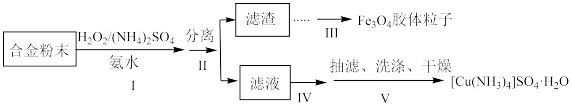
A.步骤I缓慢滴加 并不断搅拌,有利于提高 并不断搅拌,有利于提高 的利用率 的利用率 |
B.滤渣的成分为 |
| C.步骤Ⅳ可以加入95%乙醇进行醇析 |
D.步骤Ⅳ若用蒸发浓缩、冷却结晶,得到的一水硫酸四氨合铜晶体会含有较多 等杂质 等杂质 |
您最近一年使用:0次



