名校
解题方法
1 . 短周期非金属元素W、X、Y、Z原子序数依次增大,其中基态Y原子的电子具有4种不同的空间运动状态,X、Z均与Y原子相邻。W、X、Z可形成化合物Q,其结构如图: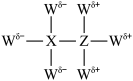 ,下列相关说法错误的是
,下列相关说法错误的是
| A.X、Y、Z元素的第一电离能和电负性均依次增大 |
| B.Q分子中X、Z间存在配位键,且由X提供孤电子对 |
C. 分子的 分子的 模型名称和空间结构名称均为正四面体形 模型名称和空间结构名称均为正四面体形 |
D.Q比 熔点高很多的主要原因是 熔点高很多的主要原因是 和 和 之间存在一种弱电性的相互作用 之间存在一种弱电性的相互作用 |
您最近一年使用:0次
7日内更新
|
280次组卷
|
2卷引用:2024届辽宁省大连市第二十四中学高三下学期第五次模拟化学试卷
名校
2 . 常温下向 的混合液中滴加
的混合液中滴加 溶液,混合液中
溶液,混合液中 与
与 的关系如图所示,
的关系如图所示, 或
或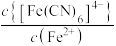 或
或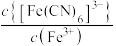 。下列叙述正确的是
。下列叙述正确的是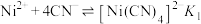 ;
;
② ;
;
③ ,且
,且 。
。
 的混合液中滴加
的混合液中滴加 溶液,混合液中
溶液,混合液中 与
与 的关系如图所示,
的关系如图所示, 或
或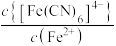 或
或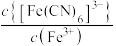 。下列叙述正确的是
。下列叙述正确的是
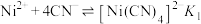 ;
;②
 ;
;③
 ,且
,且 。
。A.直线a代表 与 与 的关系 的关系 |
B.平衡常数 的数量级为 的数量级为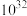 |
C.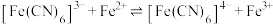 不易发生 不易发生 |
D.向含相同浓度的 和 和 的溶液中滴加 的溶液中滴加 溶液,先生成 溶液,先生成 |
您最近一年使用:0次
7日内更新
|
165次组卷
|
3卷引用:辽宁省沈阳市第二中学2023-2024学年高三下学期第五次模拟考试化学试卷
解题方法
3 . 某种矿物饲料添加剂的结构简式如图,已知W、X、Y、Z原子序数依次增大,均为短周期元素,X、Y、Z为同周期相邻元素,Q为30号元素,下列叙述不正确的是
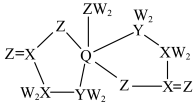
| A.同周期主族元素中第一电离能比Z大的只有一种 |
B.Q元素位于周期表的 区 区 |
C.X原子的杂化类型为 、 、 |
| D.该结构中存在共价键和配位键 |
您最近一年使用:0次
名校
解题方法
4 . 某科研团队,在前期新型电荷转移金属配合物研究中取得了一系列重要进展,引入金属Ni离子取代四硫富瓦烯四苯羧酸(M)配体中的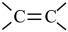 单元(如图所示),合成了具有不饱和配位点和新的氧化还原活性金属中心的N,从而赋予材料更加丰富的物理、化学功能。下列有关说法正确的是
单元(如图所示),合成了具有不饱和配位点和新的氧化还原活性金属中心的N,从而赋予材料更加丰富的物理、化学功能。下列有关说法正确的是
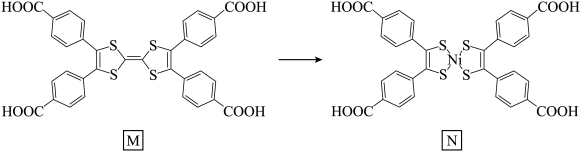
| A.M、N中所有原子一定共面 |
| B.N中Ni的配体和配位数均为4 |
| C.M与N中C原子的杂化方式完全相同 |
D.由于形成了共轭大 键,故M属于导电高分子 键,故M属于导电高分子 |
您最近一年使用:0次
2024-05-31更新
|
342次组卷
|
3卷引用:2024届辽宁省沈阳市第二中学高三下学期三模化学试题
解题方法
5 . 下列有关生产、生活应用中,所对应的离子方程式书写正确的是
A.用硝酸银与氨水制备银氨溶液: |
B.用 除去废水中的 除去废水中的 |
C.用酸性 溶液验证 溶液验证 的还原性: 的还原性: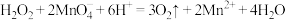 |
D.用 检验久置 检验久置 溶液中的 溶液中的 : :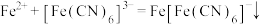 |
您最近一年使用:0次
2024-05-30更新
|
198次组卷
|
2卷引用:2024届辽宁省部分学校高三下学期联考三模化学试题
名校
6 . 四氮化四硫(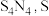 为
为 价)为橙黄色固体,易被氧化,难溶于水,易溶于四氯化碳,可用氨气与
价)为橙黄色固体,易被氧化,难溶于水,易溶于四氯化碳,可用氨气与 反应制备,反应装置如图所示(夹持和加热装置已省略)。
反应制备,反应装置如图所示(夹持和加热装置已省略)。
已知: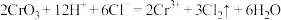 ;
;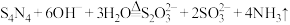
步骤如下: ,打开
,打开 和
和 ,先向装置C中通入干燥纯净的
,先向装置C中通入干燥纯净的 ,待装置C中充满黄绿色气体时,开始加热C,使
,待装置C中充满黄绿色气体时,开始加热C,使 与
与 在
在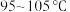 下反应生成
下反应生成 ;
;
②待装置C中的 全部反应后,关闭止水夹
全部反应后,关闭止水夹 ,撤掉装置A、B;
,撤掉装置A、B;
③ 处连接制
处连接制 的装置,关闭止水夹
的装置,关闭止水夹 ,打开
,打开 和
和 ,通入干燥纯净的
,通入干燥纯净的 ,反应制得
,反应制得 。
。
回答下列问题:
(1)装置A用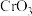 粉末与浓盐酸反应制取
粉末与浓盐酸反应制取 ,发生装置A可以选用
,发生装置A可以选用_________ 。(填选项) 时为使装置C受热均匀,可采用的最佳加热方式为
时为使装置C受热均匀,可采用的最佳加热方式为____________ ;
(3)制取 的同时装置C中还生成一种常见固体单质和一种盐,写出反应的化学方程式
的同时装置C中还生成一种常见固体单质和一种盐,写出反应的化学方程式_____________ ;
(4)装置E的作用是____________ 、_________ ;
(5)测定 的纯度:称取
的纯度:称取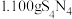 样品(杂质不参与反应),加入
样品(杂质不参与反应),加入 溶液,并加热,释放出的氨气用足量
溶液,并加热,释放出的氨气用足量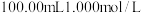 硼酸吸收[假定溶液体积不变,反应为:
硼酸吸收[假定溶液体积不变,反应为: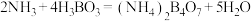 ].反应后的溶液再用
].反应后的溶液再用 的盐酸进行滴定[滴定反应为:
的盐酸进行滴定[滴定反应为: ],重复三次实验.实验数据记录如下表所示:
],重复三次实验.实验数据记录如下表所示:
____________ .(填选项)
A.滴定时应先快后慢滴入盐酸,且眼睛注视滴定管中液面变化
B.滴加最后半滴方法是:将旋塞稍稍转动,使半滴溶液悬于管口,用锥形瓶内壁将半滴溶液沾落,再用洗瓶以少量蒸馏水吹洗锥形瓶内壁,使溶液流入锥形瓶,振荡摇匀
C.滴定终点装盐酸的滴定管液面如图所示,则读数为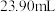
D.滴定管在滴定前有气泡,滴定后气泡消失,导致测定的结果偏高
②制得的 的纯度为
的纯度为____________ 。(保留四位有效数字)
(6)副产物 溶于水加入硫酸铜溶液中先沉淀后溶解,再向溶解后的深蓝色溶液中加入乙醇后,析出深蓝色晶体,下列叙述正确的是____________.(填选项)
溶于水加入硫酸铜溶液中先沉淀后溶解,再向溶解后的深蓝色溶液中加入乙醇后,析出深蓝色晶体,下列叙述正确的是____________.(填选项)
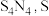 为
为 价)为橙黄色固体,易被氧化,难溶于水,易溶于四氯化碳,可用氨气与
价)为橙黄色固体,易被氧化,难溶于水,易溶于四氯化碳,可用氨气与 反应制备,反应装置如图所示(夹持和加热装置已省略)。
反应制备,反应装置如图所示(夹持和加热装置已省略)。已知:
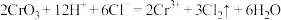 ;
;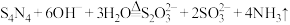
步骤如下:

 ,打开
,打开 和
和 ,先向装置C中通入干燥纯净的
,先向装置C中通入干燥纯净的 ,待装置C中充满黄绿色气体时,开始加热C,使
,待装置C中充满黄绿色气体时,开始加热C,使 与
与 在
在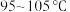 下反应生成
下反应生成 ;
;②待装置C中的
 全部反应后,关闭止水夹
全部反应后,关闭止水夹 ,撤掉装置A、B;
,撤掉装置A、B;③
 处连接制
处连接制 的装置,关闭止水夹
的装置,关闭止水夹 ,打开
,打开 和
和 ,通入干燥纯净的
,通入干燥纯净的 ,反应制得
,反应制得 。
。回答下列问题:
(1)装置A用
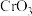 粉末与浓盐酸反应制取
粉末与浓盐酸反应制取 ,发生装置A可以选用
,发生装置A可以选用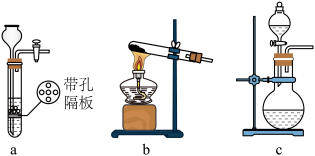
 时为使装置C受热均匀,可采用的最佳加热方式为
时为使装置C受热均匀,可采用的最佳加热方式为(3)制取
 的同时装置C中还生成一种常见固体单质和一种盐,写出反应的化学方程式
的同时装置C中还生成一种常见固体单质和一种盐,写出反应的化学方程式(4)装置E的作用是
(5)测定
 的纯度:称取
的纯度:称取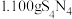 样品(杂质不参与反应),加入
样品(杂质不参与反应),加入 溶液,并加热,释放出的氨气用足量
溶液,并加热,释放出的氨气用足量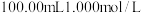 硼酸吸收[假定溶液体积不变,反应为:
硼酸吸收[假定溶液体积不变,反应为: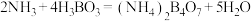 ].反应后的溶液再用
].反应后的溶液再用 的盐酸进行滴定[滴定反应为:
的盐酸进行滴定[滴定反应为: ],重复三次实验.实验数据记录如下表所示:
],重复三次实验.实验数据记录如下表所示:实验序号 | 初始读数 | 最终读数 |
Ⅰ | 0.20 | 20.42 |
Ⅱ | 0.40 | 24.85 |
Ⅲ | 1.00 | 21.18 |

A.滴定时应先快后慢滴入盐酸,且眼睛注视滴定管中液面变化
B.滴加最后半滴方法是:将旋塞稍稍转动,使半滴溶液悬于管口,用锥形瓶内壁将半滴溶液沾落,再用洗瓶以少量蒸馏水吹洗锥形瓶内壁,使溶液流入锥形瓶,振荡摇匀
C.滴定终点装盐酸的滴定管液面如图所示,则读数为
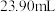
D.滴定管在滴定前有气泡,滴定后气泡消失,导致测定的结果偏高
②制得的
 的纯度为
的纯度为(6)副产物
 溶于水加入硫酸铜溶液中先沉淀后溶解,再向溶解后的深蓝色溶液中加入乙醇后,析出深蓝色晶体,下列叙述正确的是____________.(填选项)
溶于水加入硫酸铜溶液中先沉淀后溶解,再向溶解后的深蓝色溶液中加入乙醇后,析出深蓝色晶体,下列叙述正确的是____________.(填选项)A.析出的深蓝色晶体为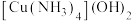 |
| B.深蓝色晶体中的阴阳离子构型都为正四面体形 |
C. 与 与 形成的配位键比 形成的配位键比 与 与 形成的配位键更稳定 形成的配位键更稳定 |
D.由配体 形成配离子 形成配离子 的过程中 的过程中 键角变大 键角变大 |
您最近一年使用:0次
2024-05-26更新
|
119次组卷
|
2卷引用:2024届辽宁省丹东市高三下学期总复习质量测试化学试卷(二)
解题方法
7 . 某化合物的结构如图所示,M、W、X、Y、Z是原子序数依次增大的短周期主族元素,其原子序数之和为31,Y原子的最外层电子数等于X原子核外电子总数,下列说法正确的是
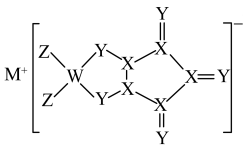
A.电负性: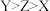 | B.简单离子半径: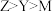 |
| C.X原子与Y原子之间存在配位键 | D.Y元素第一电离能比同周期相邻元素都低 |
您最近一年使用:0次
8 . 利用 氧化
氧化 制备水合肼
制备水合肼 ,并模拟利用水合肼处理铜氨
,并模拟利用水合肼处理铜氨 废液回收铜粉的实验流程如图所示:
废液回收铜粉的实验流程如图所示: 具有强还原性。
具有强还原性。
下列说法错误的是
 氧化
氧化 制备水合肼
制备水合肼 ,并模拟利用水合肼处理铜氨
,并模拟利用水合肼处理铜氨 废液回收铜粉的实验流程如图所示:
废液回收铜粉的实验流程如图所示:
 具有强还原性。
具有强还原性。下列说法错误的是
A.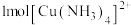 含有 含有 键 键 |
| B.步骤Ⅰ中为避免温度过高,可采用冰水浴 |
C. 与 与 反应合成水合肼的化学方程式为 反应合成水合肼的化学方程式为 |
D.步骤Ⅱ中可将 水溶液逐滴加入 水溶液逐滴加入 溶液中 溶液中 |
您最近一年使用:0次
名校
解题方法
9 . 利用炼锌钴渣[主要含 、
、 、
、 和
和 、
、 单质]制备
单质]制备 和高纯
和高纯 的流程如下。
的流程如下。 时,
时,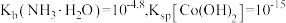
②锌的化合物与铝的化合物部分性质有相似性
请回答下列问题:
(1)写出“酸浸”过程中 发生反应的离子方程式
发生反应的离子方程式___________ 。
(2)“沉铁”过程中 实际用量远大于理论用量的主要原因
实际用量远大于理论用量的主要原因___________ ;该过程加入 的作用为
的作用为___________ 。
(3)“沉镍”过程 对溶液中
对溶液中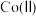 、
、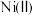 含量的影响如图。
含量的影响如图。
___________ 。
②该过程 可能发生的反应如下:
可能发生的反应如下:
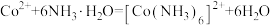
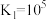


则
___________ 。
(4)“沉钴”过程生成 的离子方程式为
的离子方程式为___________ 。
(5)在电解过程中为了保持电解液成分稳定,应不断加入___________ (填化学式)。
(6)将含有未成对电子的物质置于外磁场中,会使磁场的强度增大,称其为顺磁性物质。下列物质中,属于顺磁性物质的是___________(填标号)。
 、
、 、
、 和
和 、
、 单质]制备
单质]制备 和高纯
和高纯 的流程如下。
的流程如下。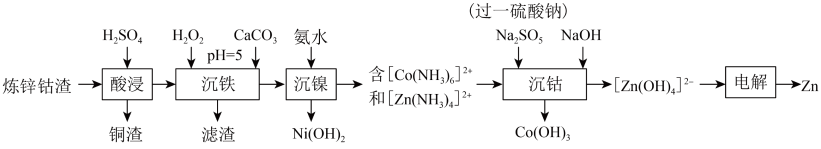
 时,
时,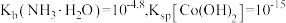
②锌的化合物与铝的化合物部分性质有相似性
请回答下列问题:
(1)写出“酸浸”过程中
 发生反应的离子方程式
发生反应的离子方程式(2)“沉铁”过程中
 实际用量远大于理论用量的主要原因
实际用量远大于理论用量的主要原因 的作用为
的作用为(3)“沉镍”过程
 对溶液中
对溶液中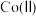 、
、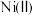 含量的影响如图。
含量的影响如图。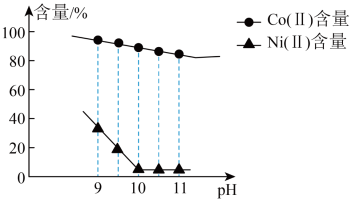

②该过程
 可能发生的反应如下:
可能发生的反应如下: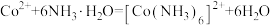
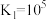


则

(4)“沉钴”过程生成
 的离子方程式为
的离子方程式为(5)在电解过程中为了保持电解液成分稳定,应不断加入
(6)将含有未成对电子的物质置于外磁场中,会使磁场的强度增大,称其为顺磁性物质。下列物质中,属于顺磁性物质的是___________(填标号)。
A. | B. | C. | D.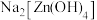 |
您最近一年使用:0次
10 . 已知反应: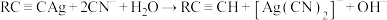 ,该反应可用于提纯炔烃。下列说法错误的是
,该反应可用于提纯炔烃。下列说法错误的是
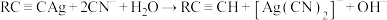 ,该反应可用于提纯炔烃。下列说法错误的是
,该反应可用于提纯炔烃。下列说法错误的是A. 的电子式为 的电子式为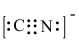 |
B.基态O原子的价电子排布图为 |
C. 的空间填充模型为 的空间填充模型为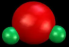 |
D.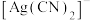 中 中 键与 键与 键的个数比为1:2 键的个数比为1:2 |
您最近一年使用:0次
2024-05-20更新
|
260次组卷
|
3卷引用:辽宁省协作校2023-2024学年高三下学期三模化学试题




