1 . 以废旧镍氢电池的金属电极芯[主要成分为 和
和 ,还含有少量铁、铝的氧化物]为原料回收钴、镍的化合物,流程如图:
,还含有少量铁、铝的氧化物]为原料回收钴、镍的化合物,流程如图:
②酸性条件下的氧化性: >
> 。
。
回答下列问题:
(1)“氧化”时 作
作_____ (填“氧化剂”或“还原剂”,下同),“浸出”时 作
作______ 。
(2)写出“沉钴1”中 转化为
转化为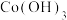 的离子方程式:
的离子方程式:_______ 。
(3)设计“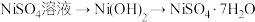 ”的目的是
”的目的是_______ 。
(4)“沉钴2”中发生反应的离子方程式为_______ ,_______ (填“能”或“不能”)用 替代
替代 ,理由是
,理由是_______ 。
(5)设计实验检验 是否洗净:
是否洗净:_______ 。
(6)水溶液中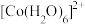 、
、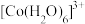 的颜色与分裂能大小有关。定义1个电子从较低能量的d轨道跃迁到较高能量的d轨道所需的能量为d轨道的分裂能。d轨道分裂能:
的颜色与分裂能大小有关。定义1个电子从较低能量的d轨道跃迁到较高能量的d轨道所需的能量为d轨道的分裂能。d轨道分裂能: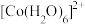
_______ (填“>”“<”或“=”)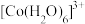 。
。
(7)镍单质晶胞有两种形式,如图所示。已知:图1晶胞棱长为acm,图2中晶胞底边长为bcm,高为ccm。图1、图2(正六棱柱)镍晶体密度之比为_______ 。
 和
和 ,还含有少量铁、铝的氧化物]为原料回收钴、镍的化合物,流程如图:
,还含有少量铁、铝的氧化物]为原料回收钴、镍的化合物,流程如图:
| 离子 |  |  |  |  |  |  |
| 开始沉淀的pH | 6.3 | 1.5 | 3.4 | 6.2 | 7.2 | |
| 完全沉淀的pH | 8.3 | 2.8 | 4.7 | 8.9 | 9.2 | 1.1 |
 >
> 。
。回答下列问题:
(1)“氧化”时
 作
作 作
作(2)写出“沉钴1”中
 转化为
转化为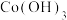 的离子方程式:
的离子方程式:(3)设计“
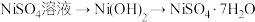 ”的目的是
”的目的是(4)“沉钴2”中发生反应的离子方程式为
 替代
替代 ,理由是
,理由是(5)设计实验检验
 是否洗净:
是否洗净:(6)水溶液中
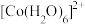 、
、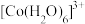 的颜色与分裂能大小有关。定义1个电子从较低能量的d轨道跃迁到较高能量的d轨道所需的能量为d轨道的分裂能。d轨道分裂能:
的颜色与分裂能大小有关。定义1个电子从较低能量的d轨道跃迁到较高能量的d轨道所需的能量为d轨道的分裂能。d轨道分裂能: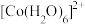
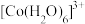 。
。(7)镍单质晶胞有两种形式,如图所示。已知:图1晶胞棱长为acm,图2中晶胞底边长为bcm,高为ccm。图1、图2(正六棱柱)镍晶体密度之比为

您最近一年使用:0次
昨日更新
|
36次组卷
|
3卷引用:2024届河南省百所名校仿真模拟大联考三模考试理综试题-高中化学
2 . Fe氧簇MOF催化 与
与 反应的机理如图所示。下列说法正确的是
反应的机理如图所示。下列说法正确的是
 与
与 反应的机理如图所示。下列说法正确的是
反应的机理如图所示。下列说法正确的是
A.根据 分子的结构推测其电子式为 分子的结构推测其电子式为 |
B.总反应方程式为 |
| C.该反应中极性键和非极性键均有断裂和形成 |
| D.该反应中Fe元素的化合价和配位数未发生变化 |
您最近一年使用:0次
名校
解题方法
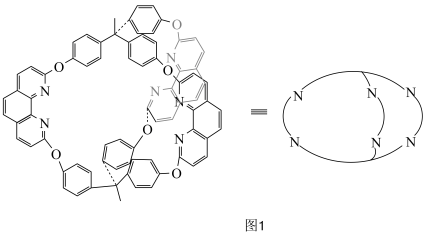
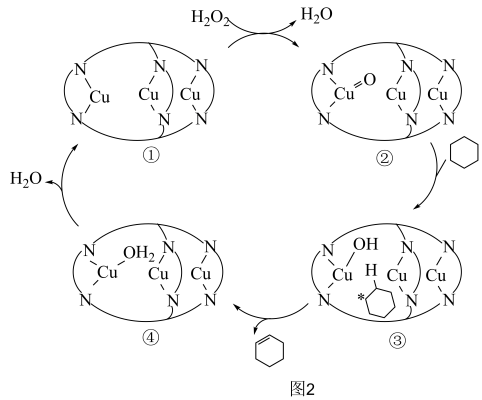
3 . 研发高效、绿色催化剂是化学科学发展的重要领域。某分子笼状有机化合物的结构如图1所示,其分子笼铜配合物结构及其催化环己烷氧化去饱和化反应的可能机理如图2所示。回答下列问题: 原子价层电子的轨道表示式为
原子价层电子的轨道表示式为_______ ,其位于元素周期表中_______ 区。
(2)平面形有机物 中N原子的杂化轨道类型为
中N原子的杂化轨道类型为_______ ,C、N原子的 轨道重叠形成
轨道重叠形成_______ 电子大π键。
(3)图1有机物中所涉及元素的电负性由大到小的顺序为_______ (用元素符号表示)。
(4)图2化合物④中 的配位数为
的配位数为_______ ,该配合物中键角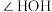
_______ (填“>”“<”或“=”) 中
中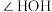 ,其原因为
,其原因为_______ 。
(5)图2中 参与氧化反应的总反应方程式为
参与氧化反应的总反应方程式为_______ 。
(6)已知有机物中N原子的电子云密度越大,其碱性越强。下列四种有机物的碱性由强到弱的顺序为_______ (填字母)。
 原子价层电子的轨道表示式为
原子价层电子的轨道表示式为(2)平面形有机物
 中N原子的杂化轨道类型为
中N原子的杂化轨道类型为 轨道重叠形成
轨道重叠形成(3)图1有机物中所涉及元素的电负性由大到小的顺序为
(4)图2化合物④中
 的配位数为
的配位数为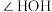
 中
中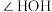 ,其原因为
,其原因为(5)图2中
 参与氧化反应的总反应方程式为
参与氧化反应的总反应方程式为(6)已知有机物中N原子的电子云密度越大,其碱性越强。下列四种有机物的碱性由强到弱的顺序为
a.  b.
b.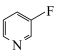 c.
c. 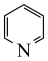 d.
d.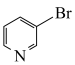
您最近一年使用:0次
2024-06-02更新
|
59次组卷
|
2卷引用:河南省部分示范性高中2023-2024学年高二下学期5月联考 化学试题
名校
解题方法
4 . 某科研团队,在前期新型电荷转移金属配合物研究中取得了一系列重要进展,引入金属Ni离子取代四硫富瓦烯四苯羧酸(M)配体中的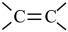 单元(如图所示),合成了具有不饱和配位点和新的氧化还原活性金属中心的N,从而赋予材料更加丰富的物理、化学功能。下列有关说法正确的是
单元(如图所示),合成了具有不饱和配位点和新的氧化还原活性金属中心的N,从而赋予材料更加丰富的物理、化学功能。下列有关说法正确的是
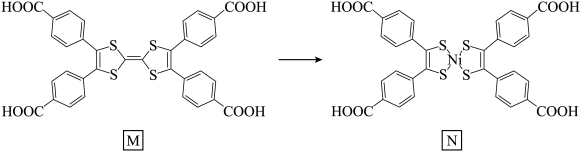
| A.M、N中所有原子一定共面 |
| B.N中Ni的配体和配位数均为4 |
| C.M与N中C原子的杂化方式完全相同 |
D.由于形成了共轭大 键,故M属于导电高分子 键,故M属于导电高分子 |
您最近一年使用:0次
2024-05-31更新
|
342次组卷
|
3卷引用:2024届河南省周口市高三5月全真模拟理科综合试题-高中化学
5 . 法莫替丁片是一种治疗消化性溃疡病的药物,其有效成分(T)的结构简式如图所示。下列叙述正确的是
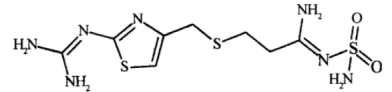
A.T中N原子都是 杂化,S原子都是 杂化,S原子都是 杂化 杂化 |
B. 中N原子最多能与质子 中N原子最多能与质子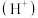 形成 形成 配位键 配位键 |
C. 分子含 分子含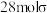 键 键 |
D.第一电离能: |
您最近一年使用:0次
名校
解题方法
6 . 利用亚铜离子为模板合成的索烃结构如图。下列说法正确的是
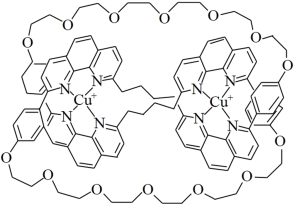
A.基态 价电子排布为 价电子排布为 ,因此 ,因此 在酸性溶液中很稳定 在酸性溶液中很稳定 |
B.基态原子第一电离能: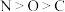 |
C.该索烃中碳原子和氮原子均为 杂化 杂化 |
D.1mol该索烃中所含配位原子数目为 |
您最近一年使用:0次
解题方法
7 . 冠醚因分子结构形如皇冠而得名,基于18-冠-6(结构如图所示)的吸附剂可用于分离 (锶离子)。下列说法正确的是
(锶离子)。下列说法正确的是
 (锶离子)。下列说法正确的是
(锶离子)。下列说法正确的是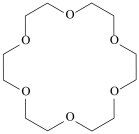
| A.电负性:O>C>Sr>H |
B.18-冠-6(空穴适配 )可增加KI在苯中的溶解度 )可增加KI在苯中的溶解度 |
| C.18-冠-6中C和O原子的杂化轨道类型不同 |
D.18-冠-6可与 形成超分子,该超分子中存在配位键、氢键等化学键 形成超分子,该超分子中存在配位键、氢键等化学键 |
您最近一年使用:0次
8 . 从高铁炉渣(含 、
、 、
、 、
、 、
、 、
、 、
、 等)中回收
等)中回收 及制得
及制得 的工艺流程如下图1所示.
的工艺流程如下图1所示. )
)
回答下列问题:
(1)为提高酸浸效率,可以采取的措施为__________ (答出一条即可)。
(2)除铁外,滤渣2的主要成分为__________ ; 的作用为
的作用为__________ 。
(3)观察图2,常温下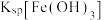
_____ (填“>”“<”或“=”) ;
; 时,溶液中
时,溶液中 的浓度为
的浓度为__________ 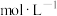 。
。__________ ;煅烧时发生反应的化学方程式为__________ 。
(5)镍能形成多种不同的化合物.图3是镍的一种螯合物(含有多个配位原子的配体与同一中心离子通过螯合配位成环而形成的配合物为螯合物)的结构示意图,图3是一种镍的氧化物的晶胞示意图. 该配合物通过螯合作用形成的配位键为
该配合物通过螯合作用形成的配位键为__________  。
。
②图4所示晶胞的化学式为__________ ;与 配位的
配位的 形成的空间构型为
形成的空间构型为__________ .若晶胞参数 ,该晶体的密度为
,该晶体的密度为__________  (设
(设 为阿伏加德罗常数的值,列出计算式即可)。
为阿伏加德罗常数的值,列出计算式即可)。
 、
、 、
、 、
、 、
、 、
、 、
、 等)中回收
等)中回收 及制得
及制得 的工艺流程如下图1所示.
的工艺流程如下图1所示.
 )
)回答下列问题:
(1)为提高酸浸效率,可以采取的措施为
(2)除铁外,滤渣2的主要成分为
 的作用为
的作用为(3)观察图2,常温下
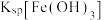
 ;
; 时,溶液中
时,溶液中 的浓度为
的浓度为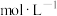 。
。
(5)镍能形成多种不同的化合物.图3是镍的一种螯合物(含有多个配位原子的配体与同一中心离子通过螯合配位成环而形成的配合物为螯合物)的结构示意图,图3是一种镍的氧化物的晶胞示意图.

 该配合物通过螯合作用形成的配位键为
该配合物通过螯合作用形成的配位键为 。
。②图4所示晶胞的化学式为
 配位的
配位的 形成的空间构型为
形成的空间构型为 ,该晶体的密度为
,该晶体的密度为 (设
(设 为阿伏加德罗常数的值,列出计算式即可)。
为阿伏加德罗常数的值,列出计算式即可)。
您最近一年使用:0次
名校
9 . 四氮化四硫(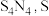 为
为 价)为橙黄色固体,易被氧化,难溶于水,易溶于四氯化碳,可用氨气与
价)为橙黄色固体,易被氧化,难溶于水,易溶于四氯化碳,可用氨气与 反应制备,反应装置如图所示(夹持和加热装置已省略)。
反应制备,反应装置如图所示(夹持和加热装置已省略)。
已知: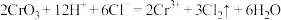 ;
;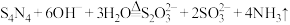
步骤如下: ,打开
,打开 和
和 ,先向装置C中通入干燥纯净的
,先向装置C中通入干燥纯净的 ,待装置C中充满黄绿色气体时,开始加热C,使
,待装置C中充满黄绿色气体时,开始加热C,使 与
与 在
在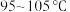 下反应生成
下反应生成 ;
;
②待装置C中的 全部反应后,关闭止水夹
全部反应后,关闭止水夹 ,撤掉装置A、B;
,撤掉装置A、B;
③ 处连接制
处连接制 的装置,关闭止水夹
的装置,关闭止水夹 ,打开
,打开 和
和 ,通入干燥纯净的
,通入干燥纯净的 ,反应制得
,反应制得 。
。
回答下列问题:
(1)装置A用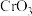 粉末与浓盐酸反应制取
粉末与浓盐酸反应制取 ,发生装置A可以选用
,发生装置A可以选用_________ 。(填选项) 时为使装置C受热均匀,可采用的最佳加热方式为
时为使装置C受热均匀,可采用的最佳加热方式为____________ ;
(3)制取 的同时装置C中还生成一种常见固体单质和一种盐,写出反应的化学方程式
的同时装置C中还生成一种常见固体单质和一种盐,写出反应的化学方程式_____________ ;
(4)装置E的作用是____________ 、_________ ;
(5)测定 的纯度:称取
的纯度:称取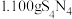 样品(杂质不参与反应),加入
样品(杂质不参与反应),加入 溶液,并加热,释放出的氨气用足量
溶液,并加热,释放出的氨气用足量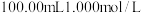 硼酸吸收[假定溶液体积不变,反应为:
硼酸吸收[假定溶液体积不变,反应为: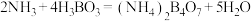 ].反应后的溶液再用
].反应后的溶液再用 的盐酸进行滴定[滴定反应为:
的盐酸进行滴定[滴定反应为: ],重复三次实验.实验数据记录如下表所示:
],重复三次实验.实验数据记录如下表所示:
____________ .(填选项)
A.滴定时应先快后慢滴入盐酸,且眼睛注视滴定管中液面变化
B.滴加最后半滴方法是:将旋塞稍稍转动,使半滴溶液悬于管口,用锥形瓶内壁将半滴溶液沾落,再用洗瓶以少量蒸馏水吹洗锥形瓶内壁,使溶液流入锥形瓶,振荡摇匀
C.滴定终点装盐酸的滴定管液面如图所示,则读数为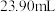
D.滴定管在滴定前有气泡,滴定后气泡消失,导致测定的结果偏高
②制得的 的纯度为
的纯度为____________ 。(保留四位有效数字)
(6)副产物 溶于水加入硫酸铜溶液中先沉淀后溶解,再向溶解后的深蓝色溶液中加入乙醇后,析出深蓝色晶体,下列叙述正确的是____________.(填选项)
溶于水加入硫酸铜溶液中先沉淀后溶解,再向溶解后的深蓝色溶液中加入乙醇后,析出深蓝色晶体,下列叙述正确的是____________.(填选项)
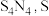 为
为 价)为橙黄色固体,易被氧化,难溶于水,易溶于四氯化碳,可用氨气与
价)为橙黄色固体,易被氧化,难溶于水,易溶于四氯化碳,可用氨气与 反应制备,反应装置如图所示(夹持和加热装置已省略)。
反应制备,反应装置如图所示(夹持和加热装置已省略)。已知:
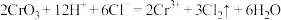 ;
;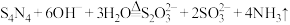
步骤如下:

 ,打开
,打开 和
和 ,先向装置C中通入干燥纯净的
,先向装置C中通入干燥纯净的 ,待装置C中充满黄绿色气体时,开始加热C,使
,待装置C中充满黄绿色气体时,开始加热C,使 与
与 在
在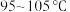 下反应生成
下反应生成 ;
;②待装置C中的
 全部反应后,关闭止水夹
全部反应后,关闭止水夹 ,撤掉装置A、B;
,撤掉装置A、B;③
 处连接制
处连接制 的装置,关闭止水夹
的装置,关闭止水夹 ,打开
,打开 和
和 ,通入干燥纯净的
,通入干燥纯净的 ,反应制得
,反应制得 。
。回答下列问题:
(1)装置A用
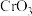 粉末与浓盐酸反应制取
粉末与浓盐酸反应制取 ,发生装置A可以选用
,发生装置A可以选用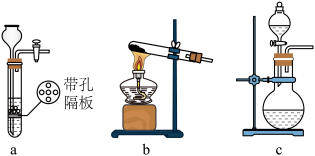
 时为使装置C受热均匀,可采用的最佳加热方式为
时为使装置C受热均匀,可采用的最佳加热方式为(3)制取
 的同时装置C中还生成一种常见固体单质和一种盐,写出反应的化学方程式
的同时装置C中还生成一种常见固体单质和一种盐,写出反应的化学方程式(4)装置E的作用是
(5)测定
 的纯度:称取
的纯度:称取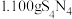 样品(杂质不参与反应),加入
样品(杂质不参与反应),加入 溶液,并加热,释放出的氨气用足量
溶液,并加热,释放出的氨气用足量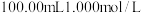 硼酸吸收[假定溶液体积不变,反应为:
硼酸吸收[假定溶液体积不变,反应为: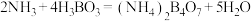 ].反应后的溶液再用
].反应后的溶液再用 的盐酸进行滴定[滴定反应为:
的盐酸进行滴定[滴定反应为: ],重复三次实验.实验数据记录如下表所示:
],重复三次实验.实验数据记录如下表所示:实验序号 | 初始读数 | 最终读数 |
Ⅰ | 0.20 | 20.42 |
Ⅱ | 0.40 | 24.85 |
Ⅲ | 1.00 | 21.18 |

A.滴定时应先快后慢滴入盐酸,且眼睛注视滴定管中液面变化
B.滴加最后半滴方法是:将旋塞稍稍转动,使半滴溶液悬于管口,用锥形瓶内壁将半滴溶液沾落,再用洗瓶以少量蒸馏水吹洗锥形瓶内壁,使溶液流入锥形瓶,振荡摇匀
C.滴定终点装盐酸的滴定管液面如图所示,则读数为
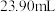
D.滴定管在滴定前有气泡,滴定后气泡消失,导致测定的结果偏高
②制得的
 的纯度为
的纯度为(6)副产物
 溶于水加入硫酸铜溶液中先沉淀后溶解,再向溶解后的深蓝色溶液中加入乙醇后,析出深蓝色晶体,下列叙述正确的是____________.(填选项)
溶于水加入硫酸铜溶液中先沉淀后溶解,再向溶解后的深蓝色溶液中加入乙醇后,析出深蓝色晶体,下列叙述正确的是____________.(填选项)A.析出的深蓝色晶体为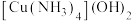 |
| B.深蓝色晶体中的阴阳离子构型都为正四面体形 |
C. 与 与 形成的配位键比 形成的配位键比 与 与 形成的配位键更稳定 形成的配位键更稳定 |
D.由配体 形成配离子 形成配离子 的过程中 的过程中 键角变大 键角变大 |
您最近一年使用:0次
2024-05-26更新
|
119次组卷
|
2卷引用:河南省许昌高级中学2023-2024学年高三下学期5月月考化学试题
名校
10 . 下列说法错误的是
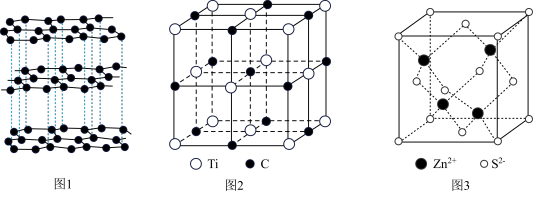
| A.图1晶体中既存在共价键又存在范德华力,属于混合型晶体 |
| B.图2为某气态团簇分子的结构,该气态团簇分子的化学式为TiC |
C.图3为ZnS的晶胞结构, 的配位数为4 的配位数为4 |
D.图3为ZnS的晶胞结构,已知该晶体的密度为 , , 为阿伏加德罗常数的值,则晶胞中 为阿伏加德罗常数的值,则晶胞中 和 和 的最近距离为 的最近距离为 |
您最近一年使用:0次
2024-05-26更新
|
125次组卷
|
2卷引用:河南省许昌高级中学2023-2024学年高三下学期5月月考化学试题




