1 . 实验室在如图所示装置中制取 ,将
,将 通入
通入 溶液,当生成的蓝色沉淀溶解为深蓝色溶液,再滴加乙醇可获得
溶液,当生成的蓝色沉淀溶解为深蓝色溶液,再滴加乙醇可获得 晶体。已知:
晶体。已知: 呈蓝色。下列说法
呈蓝色。下列说法不正确 的是
 ,将
,将 通入
通入 溶液,当生成的蓝色沉淀溶解为深蓝色溶液,再滴加乙醇可获得
溶液,当生成的蓝色沉淀溶解为深蓝色溶液,再滴加乙醇可获得 晶体。已知:
晶体。已知: 呈蓝色。下列说法
呈蓝色。下列说法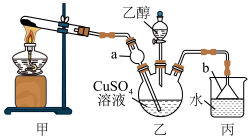
A.在装置甲试管中加入 和 和 固体加热制取 固体加热制取 |
B.装置乙中的 和装置丙中的 和装置丙中的 均可防止倒吸 均可防止倒吸 |
C. 晶体在乙醇中的溶解度小于在水中的溶解度 晶体在乙醇中的溶解度小于在水中的溶解度 |
D.与 相比, 相比, 更易与 更易与 形成配位键 形成配位键 |
您最近一年使用:0次
解题方法
2 . 氢气是重要的资源,可通过多种途径制备得到。
(1)氨硼烷( )在催化剂的作用下与水反应释放
)在催化剂的作用下与水反应释放 并生成
并生成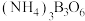 。
。
①氨硼烷分子中所有原子均达到稳定结构,其电子式为_______ 。
②已知 含有
含有 、
、 相间的六元环的结构(环上含有6个原子),
相间的六元环的结构(环上含有6个原子), 原子采取
原子采取 杂化,
杂化, 的结构式可表示为
的结构式可表示为_______ 。
(2) 的强碱溶液在
的强碱溶液在 改性的
改性的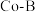 催化剂作用下与水反应生成
催化剂作用下与水反应生成 的部分反应机理如图所示。
的部分反应机理如图所示。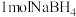 与
与 反应最多产生
反应最多产生 的物质的量为
的物质的量为_______ 。
②若用 代替
代替 ,步骤2中生成气体的化学式为
,步骤2中生成气体的化学式为_______ 。
(3)在密闭容器中,通过铁粉与 溶液反应可以制得
溶液反应可以制得 和
和 。活性
。活性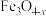 是
是 转化为
转化为 的催化剂,其可能反应机理如图所示:
的催化剂,其可能反应机理如图所示: 酸性强于
酸性强于 的原因是
的原因是_______ 。
②根据元素电负性的变化规律,图中所示的反应步骤Ⅰ可描述为_______ 。
(1)氨硼烷(
 )在催化剂的作用下与水反应释放
)在催化剂的作用下与水反应释放 并生成
并生成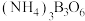 。
。①氨硼烷分子中所有原子均达到稳定结构,其电子式为
②已知
 含有
含有 、
、 相间的六元环的结构(环上含有6个原子),
相间的六元环的结构(环上含有6个原子), 原子采取
原子采取 杂化,
杂化, 的结构式可表示为
的结构式可表示为(2)
 的强碱溶液在
的强碱溶液在 改性的
改性的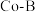 催化剂作用下与水反应生成
催化剂作用下与水反应生成 的部分反应机理如图所示。
的部分反应机理如图所示。
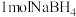 与
与 反应最多产生
反应最多产生 的物质的量为
的物质的量为②若用
 代替
代替 ,步骤2中生成气体的化学式为
,步骤2中生成气体的化学式为(3)在密闭容器中,通过铁粉与
 溶液反应可以制得
溶液反应可以制得 和
和 。活性
。活性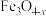 是
是 转化为
转化为 的催化剂,其可能反应机理如图所示:
的催化剂,其可能反应机理如图所示: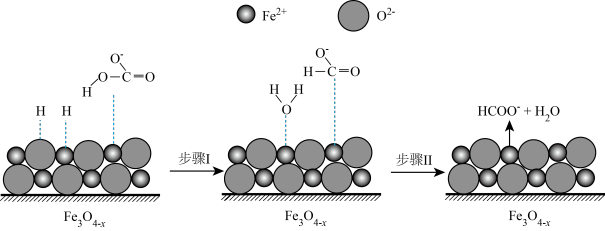
 酸性强于
酸性强于 的原因是
的原因是②根据元素电负性的变化规律,图中所示的反应步骤Ⅰ可描述为
您最近一年使用:0次
解题方法
3 . 软锰矿(主要成分MnO2)和黄铁矿(主要成分FeS2)可以制取电子工业原料MnCO3固体。
(1)浸取。将软锰矿粉和黄铁矿粉投入20%H2SO4溶液中浸取锰元素,反应机理如图-1所示。___________ (填序号)。
A.适当提高浸取温度 B.加快搅拌 C.延长浸取时间 D.加入HNO3
②Fe2+与Fe3+之间的循环是浸取的关键,浸取后期该循环过程受阻,其原因是___________ 。
③一定条件下,用足量黄铁矿浸锰,浸取时间与溶液中Fe2+、Fe3+浓度关系如图-2所示。80~100min时,Fe3+浓度变化较小而Fe2+浓度迅速上升的原因是___________ 。___________ (用离子方程式表示)。
(3)制备MnCO3。向滤液中滴加NH4HCO3溶液至沉淀完全,过滤、洗涤、干燥,得MnCO3固体。
①检验沉淀是否洗涤干净的方法是___________ 。
②不使用Na2CO3溶液做沉淀剂的原因是___________ 。
(4)滤渣利用。浸锰后的滤渣可生产补铁剂甘氨酸亚铁 [Fe(H2NCH2COO)2·2H2O],该物质中Fe2+与H2NCH2COO—配位形成两个五元环。请在下图中补充完整该物质的结构简式________ 。
(1)浸取。将软锰矿粉和黄铁矿粉投入20%H2SO4溶液中浸取锰元素,反应机理如图-1所示。

A.适当提高浸取温度 B.加快搅拌 C.延长浸取时间 D.加入HNO3
②Fe2+与Fe3+之间的循环是浸取的关键,浸取后期该循环过程受阻,其原因是
③一定条件下,用足量黄铁矿浸锰,浸取时间与溶液中Fe2+、Fe3+浓度关系如图-2所示。80~100min时,Fe3+浓度变化较小而Fe2+浓度迅速上升的原因是

(3)制备MnCO3。向滤液中滴加NH4HCO3溶液至沉淀完全,过滤、洗涤、干燥,得MnCO3固体。
①检验沉淀是否洗涤干净的方法是
②不使用Na2CO3溶液做沉淀剂的原因是
(4)滤渣利用。浸锰后的滤渣可生产补铁剂甘氨酸亚铁 [Fe(H2NCH2COO)2·2H2O],该物质中Fe2+与H2NCH2COO—配位形成两个五元环。请在下图中补充完整该物质的结构简式

您最近一年使用:0次
解题方法
4 . 由金属钛、铝形成的Tebbe试剂常用作有机反应的烯化试剂,其结构如图所示。下列说法正确的是

| A.Al3+与Cl-具有相同的电子层结构 |
| B.该结构中不存在配位键 |
| C.Tebbe试剂中的Al原子轨道杂化类型为sp3 |
| D.该结构中Al的化合价为+4 |
您最近一年使用:0次
5 . 实验室以柠檬酸亚铁、柠檬酸铵等为原料可制得柠檬酸铁铵。已知:柠檬酸结构简式为 ,是易溶于水的晶体,可用
,是易溶于水的晶体,可用 表示;柠檬酸可与
表示;柠檬酸可与 反应制柠檬酸亚铁。
反应制柠檬酸亚铁。
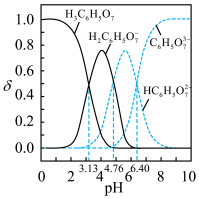
 ,测定其组成的实验方案如下:取适量样品溶于蒸馏水配成100mL溶液。取20.00mL溶液加入足量NaOH溶液充分反应,过滤、洗涤,灼烧至恒重,测得固体质量为0.32g。取20.00mL溶液于锥形瓶中,依次加入足量EDTA(能与部分金属离子结合)、HCHO溶液充分反应,滴入2滴酚酞试液,用1.00
,测定其组成的实验方案如下:取适量样品溶于蒸馏水配成100mL溶液。取20.00mL溶液加入足量NaOH溶液充分反应,过滤、洗涤,灼烧至恒重,测得固体质量为0.32g。取20.00mL溶液于锥形瓶中,依次加入足量EDTA(能与部分金属离子结合)、HCHO溶液充分反应,滴入2滴酚酞试液,用1.00 NaOH标准液滴定至终点,消耗标准液12.00mL。[
NaOH标准液滴定至终点,消耗标准液12.00mL。[ ;
;
 ]。加入EDTA的作用为
]。加入EDTA的作用为(3)避光条件下,柠檬酸铁铵与铁氰化钾[
 ]反应得到普鲁士黄(PY),其立方晶胞结构如图所示。
]反应得到普鲁士黄(PY),其立方晶胞结构如图所示。
 均与
均与 形成配位键。结合电子式解释
形成配位键。结合电子式解释 作配体的原因:
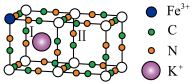
作配体的原因:②普鲁士蓝(PB)晶胞结构如图所示, 周围最近且等距的
周围最近且等距的 有12个,“○”位置被
有12个,“○”位置被 或
或 占据,用“
占据,用“ ”在图上补全PB结构图中Ⅰ和Ⅱ两个小立方体中的
”在图上补全PB结构图中Ⅰ和Ⅱ两个小立方体中的 。
。
 能容易地嵌入和脱嵌,因此PB可作为钾离子电池的正极材料。充电过程中,推测
能容易地嵌入和脱嵌,因此PB可作为钾离子电池的正极材料。充电过程中,推测 会从PB中脱嵌出来,理由是
会从PB中脱嵌出来,理由是(4)补充完整由铁泥(主要含有单质铁、少量
 和铁的氧化物)制备
和铁的氧化物)制备 的实验方案,部分装置如图所示:取一定量的铁泥,
的实验方案,部分装置如图所示:取一定量的铁泥, 。(须使用试剂:
。(须使用试剂: 、
、 溶液、稀硫酸)
溶液、稀硫酸)
您最近一年使用:0次
6 . Cu、Ag位于元素周期表ⅠB族。Ag与空气中微量 接触发生反应生成黑色
接触发生反应生成黑色 。Cu可以形成
。Cu可以形成 、
、 、
、 、
、 等化合物。有研究表明,无水
等化合物。有研究表明,无水 为长链状结构,其片断如图
为长链状结构,其片断如图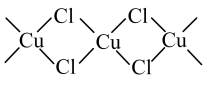 。下列物质结构与性质或物质性质与用途
。下列物质结构与性质或物质性质与用途
A. 中的O存在孤电子对, 中的O存在孤电子对, 能与 能与 形成 形成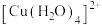 |
B. 中H元素呈+1价,浓 中H元素呈+1价,浓 具有强氧化性 具有强氧化性 |
C. 具有杀菌能力,可用于游泳池的水处理 具有杀菌能力,可用于游泳池的水处理 |
D.无水 吸水后显现蓝色,可用于检验乙醇所含的微量水分 吸水后显现蓝色,可用于检验乙醇所含的微量水分 |
您最近一年使用:0次
名校
解题方法
7 . NH3可用于生产铵盐、硝酸等。液氨中 和
和 的性质类似于水中的
的性质类似于水中的 和OH-;NH3中的一个H被-NH2取代形成N2H4,N2H4中的两个H被-CH3取代形成
和OH-;NH3中的一个H被-NH2取代形成N2H4,N2H4中的两个H被-CH3取代形成 。下列说法正确的是
。下列说法正确的是
 和
和 的性质类似于水中的
的性质类似于水中的 和OH-;NH3中的一个H被-NH2取代形成N2H4,N2H4中的两个H被-CH3取代形成
和OH-;NH3中的一个H被-NH2取代形成N2H4,N2H4中的两个H被-CH3取代形成 。下列说法正确的是
。下列说法正确的是| A.电负性:H<O<N | B.键角: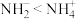 |
C. 存在顺反异构 存在顺反异构 | D. N2H4和 都可做配体 都可做配体 |
您最近一年使用:0次
8 . 砷化镓是一种高性能半导体材料,被广泛应用于光电子器件等领域。砷化镓立方晶胞(晶胞参数为 )如图1。下列说法正确的是
)如图1。下列说法正确的是
 )如图1。下列说法正确的是
)如图1。下列说法正确的是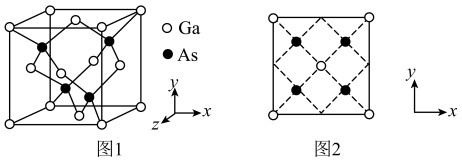
A. 的配位数为2 的配位数为2 | B.该晶胞沿z轴方向的平面投影如图2 |
| C.晶体中配位键占共价键总数的25% | D.晶胞中砷原子与镓原子间的最短距离为 |
您最近一年使用:0次
2024-06-03更新
|
556次组卷
|
5卷引用:江苏省南京师范大学附属中学2024届高三下学期5月模拟化学试题
9 . 卤族元素单质及其化合物应用广泛。海洋是一个巨大的卤素资源宝库,从海水中能获得NaCl,NaCl的晶胞如下图所示。以NaCl为原料可制得Cl2、HClO、ClO2、 、
、 。工业常通过电解NaCl饱和溶液制备Cl2,Cl2氧化卤水中Br-可得到Br2.KClO3酸性溶液中加入H2C2O4可制得黄绿色气体ClO2,该气体常用作自来水消毒剂。F2能与熔融的Na2SO4反应生成硫酰氟(SO2F2)。标况下,氟化氢呈液态。
。工业常通过电解NaCl饱和溶液制备Cl2,Cl2氧化卤水中Br-可得到Br2.KClO3酸性溶液中加入H2C2O4可制得黄绿色气体ClO2,该气体常用作自来水消毒剂。F2能与熔融的Na2SO4反应生成硫酰氟(SO2F2)。标况下,氟化氢呈液态。
 、
、 。工业常通过电解NaCl饱和溶液制备Cl2,Cl2氧化卤水中Br-可得到Br2.KClO3酸性溶液中加入H2C2O4可制得黄绿色气体ClO2,该气体常用作自来水消毒剂。F2能与熔融的Na2SO4反应生成硫酰氟(SO2F2)。标况下,氟化氢呈液态。
。工业常通过电解NaCl饱和溶液制备Cl2,Cl2氧化卤水中Br-可得到Br2.KClO3酸性溶液中加入H2C2O4可制得黄绿色气体ClO2,该气体常用作自来水消毒剂。F2能与熔融的Na2SO4反应生成硫酰氟(SO2F2)。标况下,氟化氢呈液态。 
| A.HClO呈弱酸性,可用于漂白纸张 |
| B.ClO2具有强氧化性,可用于自来水杀菌消毒 |
C.Cl-有孤电子对,可与 形成 形成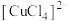 |
| D.HF分子间存在氢键,HF沸点较高 |
您最近一年使用:0次
名校
10 .  的综合利用具有重要意义。
的综合利用具有重要意义。 的捕集方法众多,可以形成
的捕集方法众多,可以形成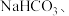
 、尿素
、尿素 等重要化合物,
等重要化合物, 还可以催化转化为高附加值化学品
还可以催化转化为高附加值化学品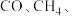
 等。如用镍基催化剂催化电解
等。如用镍基催化剂催化电解 可得到
可得到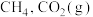 和
和 反应生成
反应生成
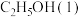 和
和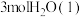 可放出
可放出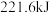 的热量。下列物质结构与性质或物质性质与用途具有对应关系的是
的热量。下列物质结构与性质或物质性质与用途具有对应关系的是
 的综合利用具有重要意义。
的综合利用具有重要意义。 的捕集方法众多,可以形成
的捕集方法众多,可以形成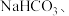
 、尿素
、尿素 等重要化合物,
等重要化合物, 还可以催化转化为高附加值化学品
还可以催化转化为高附加值化学品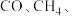
 等。如用镍基催化剂催化电解
等。如用镍基催化剂催化电解 可得到
可得到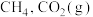 和
和 反应生成
反应生成
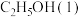 和
和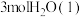 可放出
可放出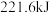 的热量。下列物质结构与性质或物质性质与用途具有对应关系的是
的热量。下列物质结构与性质或物质性质与用途具有对应关系的是A. 受热易分解,可用作化肥 受热易分解,可用作化肥 |
B. 性质稳定,可作为燃料电池的燃料 性质稳定,可作为燃料电池的燃料 |
C. 与水分子之间形成氢键,医用酒精可使蛋白质变性 与水分子之间形成氢键,医用酒精可使蛋白质变性 |
D. 可与血红蛋白中的 可与血红蛋白中的 以配位键结合, 以配位键结合, 会引起人体中毒 会引起人体中毒 |
您最近一年使用:0次



