名校
1 . 回答下列问题。
(1)氨气极易溶于水的原因___________
(2)HCl极易溶于水的原因___________
(3)硫酸铜溶液中逐滴加入浓氨水,写出对应的离子方程式___________
(4)金属铜单独与氨水或单独与过氧化氢都不能反应,但可与氨水和过氧化氢的混合溶液反应,写出对应的离子方程式______________________
(5)水结冰后,水分子之间最大程度的形成氢键,该氢键可表示为______ ,水分子和氢键的物质的量之比为_____ ,当温度有0℃升高到4℃时,水的密度逐渐______ (填“增大”、“减小”)。
(1)氨气极易溶于水的原因
(2)HCl极易溶于水的原因
(3)硫酸铜溶液中逐滴加入浓氨水,写出对应的离子方程式
(4)金属铜单独与氨水或单独与过氧化氢都不能反应,但可与氨水和过氧化氢的混合溶液反应,写出对应的离子方程式
(5)水结冰后,水分子之间最大程度的形成氢键,该氢键可表示为
您最近一年使用:0次
名校
2 . 比较下列物质的熔沸点,按由大到小的顺序写
(1)H2O、SO2、NaCl、SiO2___________
(2)Al2O3、AlCl3___________
(3)MgO、MgCl2___________
(4)HF、HCl、HBr___________
(5)CH4、SiH4、GeH4___________
(1)H2O、SO2、NaCl、SiO2
(2)Al2O3、AlCl3
(3)MgO、MgCl2
(4)HF、HCl、HBr
(5)CH4、SiH4、GeH4
您最近一年使用:0次
11-12高一下·吉林长春·期中
名校
解题方法
3 . 图中每条折线表示IVA~VIIA中的某一族元素氢化物的沸点变化,其中a点代表的是


| A.H2S | B.HCl | C.PH3 | D.SiH4 |
您最近一年使用:0次
2021-12-03更新
|
71次组卷
|
34卷引用:宁夏石嘴山市第三中学2021-2022学年高二上学期期中考试化学试题
宁夏石嘴山市第三中学2021-2022学年高二上学期期中考试化学试题(人教版2019)选择性必修2 第二章 分子结构与性质 第三节 分子结构与物质的性质高二选择性必修2(人教版2019)第二章 分子结构与性质 第三节综合训练四川省巴中市平昌县驷马中学2020-2021学年高二上学期期末测试化学试题(已下线)2.4 分子间作用力-2020-2021学年高二化学课时同步练(鲁科2019选择性必修2) (已下线)2.3 分子的结构与物质的性质(A级基础练)-2020-2021学年高二化学章节分层检测ABC(人教版2019选择性必修2)广西桂林市第十八中学2020-2021学年高一下学期开学考试化学试题福建省建瓯市芝华中学2020-2021学年高二下学期第一阶段考试化学试题河北省衡水市武强中学2020-2021学年高二下学期第一次月考化学试题(已下线)2011-2012学年吉林长春市十一高高一下学期期中考试化学试卷(已下线)2011-2012学年吉林省吉林一中高一下学期期中考试化学试卷2014-2015学年吉林省长春市十一中高一下期中化学试卷2016-2017学年湖南师范大学附属中学高一下学期第一次阶段性测试化学试卷湖南省衡阳市八中、澧县一中、鼎城中学等重点中学2016-2017学年高一下学期期末联考化学试题江西省抚州市临川区第一中学2017-2018学年高一下学期第一次月考化学试题上海市高二上学期第二章《初识元素周期律》综合测试题第4节 分子间作用力与物质性质——A学习区 夯实基础(鲁科版选修3)湖北省黄冈市黄梅县第一中学2019-2020学年高一下学期期中考试化学试题(已下线)专题5.3 化学键(讲)——2020年高考化学一轮复习讲练测吉林省通化市通化县综合高级中学2019-2020学年高二下学期期中考试化学试题(已下线)吉林省长春市实验中学2019-2020学年高一下学期期中考试化学试题吉林省长春市实验中学2019-2020学年高一下期中考试化学试题贵州省贵阳市第十四中学2019-2020学年高一下学期期末考试化学试题苏教版(2020)高一必修第一册专题5第二单元课时2 化学键 分子间作用力人教版(2019)高一必修第一册 第四章 第三节课时2 化学键 分子间作用力贵州省贵阳十四中2019-2020学年高一下学期期末考试化学试题湖北省武汉市江夏区金口中学2019-2020学年沆二下学期月考化学试题浙江省嘉兴市第五高级中学2018-2019学年高一下学期期中考试化学试题云南省玉溪市民族中学2021-2022学年高二上学期期末考试化学试题北京市第一五六中学 2021-2022学年高二下学期期中考试化学试题天津市第三中学2021-2022学年高二下学期期末质量检测化学试题云南省文山州一中2021-2022学年高一下学期3月份考试化学试题天津市红桥区2021-2022学年高二下学期期末考试化学试题广东省惠州市丰湖高级中学2022-2023学年高二下学期第一次段考化学试题
名校
4 . 下列说法正确的是
| A.硫酸氢钠溶于水、加热至熔融态都破坏了离子键和共价键 |
| B.氯化氢气体溶于水破坏了离子键,金刚石熔化破坏了共价键 |
| C.冰→水→氢气和氧气依次破坏了氢键和范德华力,共价键 |
| D.利用微机械剥离石墨制得石墨烯破坏了共价键和大π键 |
您最近一年使用:0次
名校
5 . 富马酸亚铁是治疗贫血药物的一种。能有效避免添加无机铁对维生素等活性物质的破坏。请根据下列信息回答对应的问题:
(1)在“富马酸亚铁”中,亚铁离子的核外电子排布式为_______ ,其未成对电子数数量为_______
(2)富马酸的结构如图所示,结合其结构特点,下列几种溶剂中,可以溶解富马酸的有_______(填写字母选项)

(3)富马酸结构中,碳原子的杂化类型是_______ ,其中元素的电负性由大到小排序为_______ 。
(4)如图是富马酸的一种同分异构体:马来酸,其结构如图所示,查阅资料发现,富马酸的熔点在300oC,而马来酸熔点仅140oC,请用文字说明其熔点差异巨大原因:_______ 。

(5)铁系元素能与CO形成Fe(CO)5、Ni(CO)4等金属羰基化合物。已知室温时Fe(CO)5为浅黄色液体,沸点103oC,则Fe(CO)5中含有的化学键类型包括_______ 。Fe(CO)5的熔沸点_______ Ni(CO)4(填“高于”或“低于”)
A.极性共价键 B.离子键 C.配位键 D.金属键
(6)除了常规的药物补铁,老人家推崇“铁锅炒菜”补铁,这种补铁效果十分有限,主要原因是铁锅表面会覆盖一层四氧化三铁,或者氧化铁,不适合人体的直接吸收,反倒是锅底会存在少量的石墨与氧化亚铁,理想氧化亚铁晶体的晶胞如图所示:

已知:氧化亚铁晶体的密度为ρ g/cm3,NA代表阿伏加德罗常数的值。在该晶胞中,Fe2+的个数为_______ ,与O2-紧邻且等距离的O2-数目为_______ ;Fe2+与O2-最短核间距为_______ pm。
(1)在“富马酸亚铁”中,亚铁离子的核外电子排布式为
(2)富马酸的结构如图所示,结合其结构特点,下列几种溶剂中,可以溶解富马酸的有_______(填写字母选项)

| A.水 | B.乙醚 | C.乙醇 | D.苯 |
(4)如图是富马酸的一种同分异构体:马来酸,其结构如图所示,查阅资料发现,富马酸的熔点在300oC,而马来酸熔点仅140oC,请用文字说明其熔点差异巨大原因:

(5)铁系元素能与CO形成Fe(CO)5、Ni(CO)4等金属羰基化合物。已知室温时Fe(CO)5为浅黄色液体,沸点103oC,则Fe(CO)5中含有的化学键类型包括
A.极性共价键 B.离子键 C.配位键 D.金属键
(6)除了常规的药物补铁,老人家推崇“铁锅炒菜”补铁,这种补铁效果十分有限,主要原因是铁锅表面会覆盖一层四氧化三铁,或者氧化铁,不适合人体的直接吸收,反倒是锅底会存在少量的石墨与氧化亚铁,理想氧化亚铁晶体的晶胞如图所示:

已知:氧化亚铁晶体的密度为ρ g/cm3,NA代表阿伏加德罗常数的值。在该晶胞中,Fe2+的个数为
您最近一年使用:0次
2021-11-02更新
|
187次组卷
|
2卷引用:宁夏银川市第一中学2021-2022学年高三上学期第三次月考理科综合化学试题
解题方法
6 . 回答下列问题:
(1)碳是形成化合物种类最多的元素。
①C元素是形成有机物的主要元素,下列分子中含有 和
和 杂化方式的是
杂化方式的是___________ (填字母)。
a. b.
b. c.
c. d.
d.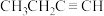
②乙醇( )与二甲醛(
)与二甲醛( )的分子式均为
)的分子式均为 ,但
,但 的沸点高于
的沸点高于 的沸点,其原因是
的沸点,其原因是___________ 。
(2) 能与
能与 反应生成
反应生成 ,
, 中
中 原子的杂化轨道类型为
原子的杂化轨道类型为___________ , 与
与 之间形成
之间形成___________ 键。硼酸( )在水溶液中能与水反应生成
)在水溶液中能与水反应生成 而体现一元弱酸的性质。
而体现一元弱酸的性质。 中
中 的原子杂化类型为
的原子杂化类型为___________ ,不考虑空间构型, 的结构可用示意图表示为
的结构可用示意图表示为___________ 。
(3)麻醉剂的发现和使用是人类医学史上一项了不起的成就。
①“笑气”( )是人类最早应用于医疗的麻醉剂之一、已知
)是人类最早应用于医疗的麻醉剂之一、已知 分子中氧原子只与一个氮原子相连,则
分子中氧原子只与一个氮原子相连,则 的电子式可表示为
的电子式可表示为___________ ,其分子立体构型是___________ 形。
②另一种常用麻醉剂氯仿常因保存不慎而被氧化,产生剧毒光气( ):
):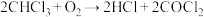 ,光气(
,光气( )分子的立体构型是
)分子的立体构型是___________ 形。
(4)丁二酮肟常用于检验 :在稀氨水介质中,丁二酮肟与
:在稀氨水介质中,丁二酮肟与 反应可生成鲜红色沉淀,其结构如图所示。
反应可生成鲜红色沉淀,其结构如图所示。

①该结构中,碳碳之间的共价键类型是 键,碳氮之间的共价键类型是
键,碳氮之间的共价键类型是___________ ,氮镍之间形成的化学键是___________ 。
②该结构中,氧氢之间除共价键外还可存在___________ 。
③该结构中,碳原子的杂化轨道类型有___________ 。
(1)碳是形成化合物种类最多的元素。
①C元素是形成有机物的主要元素,下列分子中含有
 和
和 杂化方式的是
杂化方式的是a.
 b.
b. c.
c. d.
d.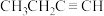
②乙醇(
 )与二甲醛(
)与二甲醛( )的分子式均为
)的分子式均为 ,但
,但 的沸点高于
的沸点高于 的沸点,其原因是
的沸点,其原因是(2)
 能与
能与 反应生成
反应生成 ,
, 中
中 原子的杂化轨道类型为
原子的杂化轨道类型为 与
与 之间形成
之间形成 )在水溶液中能与水反应生成
)在水溶液中能与水反应生成 而体现一元弱酸的性质。
而体现一元弱酸的性质。 中
中 的原子杂化类型为
的原子杂化类型为 的结构可用示意图表示为
的结构可用示意图表示为(3)麻醉剂的发现和使用是人类医学史上一项了不起的成就。
①“笑气”(
 )是人类最早应用于医疗的麻醉剂之一、已知
)是人类最早应用于医疗的麻醉剂之一、已知 分子中氧原子只与一个氮原子相连,则
分子中氧原子只与一个氮原子相连,则 的电子式可表示为
的电子式可表示为②另一种常用麻醉剂氯仿常因保存不慎而被氧化,产生剧毒光气(
 ):
):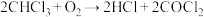 ,光气(
,光气( )分子的立体构型是
)分子的立体构型是(4)丁二酮肟常用于检验
 :在稀氨水介质中,丁二酮肟与
:在稀氨水介质中,丁二酮肟与 反应可生成鲜红色沉淀,其结构如图所示。
反应可生成鲜红色沉淀,其结构如图所示。
①该结构中,碳碳之间的共价键类型是
 键,碳氮之间的共价键类型是
键,碳氮之间的共价键类型是②该结构中,氧氢之间除共价键外还可存在
③该结构中,碳原子的杂化轨道类型有
您最近一年使用:0次
解题方法
7 . 圆明园十二生肖兽首都是用铜质材料铸造而成的,我国铜的应用与冶炼由来已久,西汉刘安的《淮南万毕术》中有“曾青得铁则化为铜”,这是湿法治金的雏形。
(1)基态铁原子的电子排布式为___________ ;基态的 有
有___________ 个未成对电子。
(2)向硫酸铜溶液中滴加过量的氨水可形成 深蓝色溶液。
深蓝色溶液。
① 和
和 之间形成的化学键称为
之间形成的化学键称为___________ ,提供孤电子对的原子是___________ (填名称)。
② 中阴离子的立体构型是
中阴离子的立体构型是___________ 。
③氨的沸点___________ (填“高于”“低于”或“等于”)膦( )的,原因是
)的,原因是___________ ; 是
是___________ 分子(填“极性”或“非极性”),中心原子的轨道杂化类型为___________ 。
(3)铁和铜都是___________ 晶体(填“离子”“分子”“原子”或“金属”); 的第三电离能(
的第三电离能( )、第四电离能(
)、第四电离能( )分别为
)分别为 、
、 ,
, 的原因是
的原因是___________ 。
(4)铜晶胞如图所示。已知: 代表阿伏加德罗常数的值,铜晶胞的密度为
代表阿伏加德罗常数的值,铜晶胞的密度为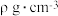 。
。

①铜原子半径为 ,则
,则
___________ 。
②铜晶胞的空间利用率为___________ 。(注明:晶胞的空间利用率 )
)
(1)基态铁原子的电子排布式为
 有
有(2)向硫酸铜溶液中滴加过量的氨水可形成
 深蓝色溶液。
深蓝色溶液。①
 和
和 之间形成的化学键称为
之间形成的化学键称为②
 中阴离子的立体构型是
中阴离子的立体构型是③氨的沸点
 )的,原因是
)的,原因是 是
是(3)铁和铜都是
 的第三电离能(
的第三电离能( )、第四电离能(
)、第四电离能( )分别为
)分别为 、
、 ,
, 的原因是
的原因是(4)铜晶胞如图所示。已知:
 代表阿伏加德罗常数的值,铜晶胞的密度为
代表阿伏加德罗常数的值,铜晶胞的密度为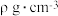 。
。
①铜原子半径为
 ,则
,则
②铜晶胞的空间利用率为
 )
)
您最近一年使用:0次
名校
8 . 下列各项叙述中不正确的是
| A.无机含氧酸HClO、H2SO3、HNO3的酸性逐渐增强 |
| B.Cr、Mn、Fe三种元素基态原子的未成对电子数逐渐增多 |
| C.CaF2、NaCl、CsCl三种晶体中阴离子的配位数逐渐增大 |
D.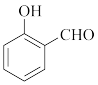 、 、 、 、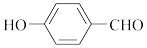 三种有机物的沸点逐渐升高 三种有机物的沸点逐渐升高 |
您最近一年使用:0次
2021-09-09更新
|
361次组卷
|
4卷引用:宁夏银川市第六中学2020-2021学年高二下学期期末考试化学试题
宁夏银川市第六中学2020-2021学年高二下学期期末考试化学试题河北省石家庄市第一中学2020-2021学年高二下学期学情反馈(一)化学试题四川省遂宁市第二中学校2021-2022学年高二上学期期中考试化学试题(已下线)微专题51 极性、溶解性、手性、无机含氧酸酸性的判断-备战2023年高考化学一轮复习考点微专题
名校
解题方法
9 . 下列叙述中正确的是
| A.一切四面体空间构型的分子内键角均为109°28′ |
| B.Cu(OH)2能溶于过量氨水形成[Cu(NH3)4]2+,中心离子为Cu2+,配体是NH3 |
| C.任何晶体,若含阳离子也一定含阴离子 |
| D.水分子稳定是因为水分子间存在氢键作用 |
您最近一年使用:0次
2021-09-09更新
|
275次组卷
|
3卷引用:宁夏吴忠中学2021-2022学年高三上学期第一次月考化学试题
名校
10 . 下列关于物质结构的命题中,正确的项数有
①乙醛分子中碳原子的杂化类型有sp2和sp3两种
②元素Ge位于周期表第四周期IVA族,核外电子排布式为[Ar]4s24p2,属于P区
③非极性分子往往具有高度对称性,如BF3、PCl5、H2O2、CO2这样的分子
④Na2O、Na2O2中阴阳离子个数比相同
⑤Cu(OH)2是一种蓝色絮状沉淀,既能溶于硝酸、也能溶于氨水,是两性氢氧化物
⑥氨水中大部分NH3与H2O以氢键(用“…”表示)结合成NH3·H2O分子,根据氨水的性质可知NH3·H2O的结构式可记为:
⑦HF晶体沸点高于HCl,是因为HCl共价键键能小于HF
①乙醛分子中碳原子的杂化类型有sp2和sp3两种
②元素Ge位于周期表第四周期IVA族,核外电子排布式为[Ar]4s24p2,属于P区
③非极性分子往往具有高度对称性,如BF3、PCl5、H2O2、CO2这样的分子
④Na2O、Na2O2中阴阳离子个数比相同
⑤Cu(OH)2是一种蓝色絮状沉淀,既能溶于硝酸、也能溶于氨水,是两性氢氧化物
⑥氨水中大部分NH3与H2O以氢键(用“…”表示)结合成NH3·H2O分子,根据氨水的性质可知NH3·H2O的结构式可记为:

⑦HF晶体沸点高于HCl,是因为HCl共价键键能小于HF
| A.2项 | B.3项 | C.4项 | D.5项 |
您最近一年使用:0次



