名校
1 . 设NA为阿伏加德罗常数的值,下列叙述错误的是

| A.含16 g氧原子的二氧化硅晶体中含有的δ键数目为2NA |
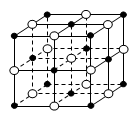
| B.23.4 g NaCl晶体中含有0.1NA个如图所示的结构单元 |
| C.常温常压下,5 gD2O含有的质子数、电子数、中子数均为2.5NA |
| D.2 mol SO2和1 mol O2在一定条件下反应所得混合气体分子数小于2NA |
您最近一年使用:0次
2016-12-09更新
|
340次组卷
|
6卷引用:四川省绵阳市南山中学2020-2021学年高二下学期开学考试化学试题
真题
名校
2 . [化学——选修3:物质结构与性质]碳及其化合物广泛存在于自然界中,回答下列问题:
(1)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用___________ 形象化描述。在基态原子中,核外存在______ 对自旋相反的电子。
(2)碳在形成化合物时,其键型以共价键为主,原因是_____________ 。
(3)CS2分子中,共价键的类型有_____________ ,C原子的杂化轨道类型是_______ ,写出两个与CS2具有相同空间构型和键合形式的分子或离子_______________ 。
(4)CO能与金属Fe形成Fe(CO)5,该化合物的熔点为253K,沸点为376K,其固体属于_____ 晶体。
碳有多种同素异形体,其中石墨烯与金刚石的晶体结构如图所示:

①在石墨烯晶体中,每个C原子连接_____ 个六元环,每个六元环占有___ 个C原子。
②在金刚石晶体中,C原子所连接的最小环也为六元环,每个C原子连接________ 个六元环,六元环中最多有________ 个C原子在同一平面。
(1)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用
(2)碳在形成化合物时,其键型以共价键为主,原因是
(3)CS2分子中,共价键的类型有
(4)CO能与金属Fe形成Fe(CO)5,该化合物的熔点为253K,沸点为376K,其固体属于
碳有多种同素异形体,其中石墨烯与金刚石的晶体结构如图所示:

①在石墨烯晶体中,每个C原子连接
②在金刚石晶体中,C原子所连接的最小环也为六元环,每个C原子连接
您最近一年使用:0次
2016-12-09更新
|
5107次组卷
|
12卷引用:重庆市垫江县2018届高三上学期模底考试理综化学试题
重庆市垫江县2018届高三上学期模底考试理综化学试题四川省宜宾市第四中学2021届高三上学期开学考试理综化学试题2015年全国普通高等学校招生统一考试化学(新课标I卷)2016届广东省深圳第二外国语学校高三上学期第二次教学质检化学试卷2016届黑龙江省哈尔滨一中高三上学期12月月考化学试卷宁夏石嘴山市第三中学2018届高三9月月考化学试题百所名校联考-物质结构与性质云南省曲靖市第一中学2020届高三化学仿真模拟考试理科综合化学试题云南省曲靖一中2020届高考化学仿真试卷河北省石家庄市第二中学2020届高中毕业班四月份教学质量监测卷理科综合化学部分安徽省马鞍山市2020届高考第二次模拟理综化学试题辽宁省沈阳东北育才中学2020年高中毕业班教学质量监测卷理科综合化学试题
名校
解题方法
3 . 我国从国外进口某原料经测定主要含有A、B、C、D、E五种前四周期元素,且原子序数依次增大。元素A、B、C、D、E的原子结构等信息如下:
请回答下列问题:(用A、B、C、D、E所对应的元素符号作答)
(1)B、C、D第一电离能由大到小为______________________ 。
(2)E的二价离子的电子排布式为________________________ 。
(3)A2B2D4常用作除锈剂,该分子中B的杂化方式为________ ;1 mol A2B2D4分子中含有σ键数目为________ 。
(4)与化合物BD互为等电子体的阴离子化学式为________ 等。
(5)B2A6、C2A4分子中均含有18个电子,它们的沸点相差较大,主要原因是_______________ 。
(6)BD2在高温高压下所形成晶体的晶胞如图所示,一个该晶胞中含________ 个D原子。

| 元素 | 元素性质或原子结构 |
| A | 周期表中原子半径最小的元素 |
| B | 原子核外有三种不同的能级且各个能级所填充的电子数相同 |
| C | 最外层P轨道半充满 |
| D | 位于短周期,其原子的核外成对电子数是未成对电子数的3倍 |
| E | 位于ds区且原子的最外层电子数与A的相同 |
(1)B、C、D第一电离能由大到小为
(2)E的二价离子的电子排布式为
(3)A2B2D4常用作除锈剂,该分子中B的杂化方式为
(4)与化合物BD互为等电子体的阴离子化学式为
(5)B2A6、C2A4分子中均含有18个电子,它们的沸点相差较大,主要原因是
(6)BD2在高温高压下所形成晶体的晶胞如图所示,一个该晶胞中含

您最近一年使用:0次
2016-12-09更新
|
745次组卷
|
7卷引用:2016届江苏省扬州中学高三上学期开学考试化学试卷
2016届江苏省扬州中学高三上学期开学考试化学试卷2015届江苏省泰州市高三第二次模拟考试化学试卷西藏自治区拉萨中学2018届高三上学期第三次月考理综化学试题(已下线)二轮复习 专题17 物质结构与性质 押题专练步步为赢 高二化学暑假作业:作业十四 物质结构与性质(选修3)西藏自治区日喀则市2020届高三上学期学业水平测试(模拟)理综化学试题(已下线)易错点15 化学键-备战2023年高考化学考试易错题
名校
解题方法
4 . 目前半导体生产展开了一场“铜芯片”革命——在硅芯片上用铜代替铝布线,古老的金属铜在现代科技应用上取得了突破,用黄铜矿(主要成分为CuFeS2)生产粗铜,其反应原理如下:

回答下列问题:
(1)基态铜原子的电子排布式为___________ ,硫、氧元素相比,第一电离能较小的元素是___________ (填元素符号)。
(2)反应①、②中均生成有相同的气体分子,该分子的中心原子杂化类型是___________ ,其立体结构是___________ 。
(3)某学生用硫酸铜溶液与氨水做了一组实验:CuSO4溶液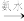 蓝色沉淀
蓝色沉淀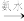 沉淀溶解,得到深蓝色透明溶液。写出蓝色沉淀溶于氨水的离子方程式
沉淀溶解,得到深蓝色透明溶液。写出蓝色沉淀溶于氨水的离子方程式___________ ;深蓝色透明溶液中的阳离子(不考虑H+)内存在的全部化学键类型有___________ 。
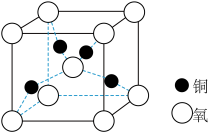
(4)铜是第四周期最重要的过渡元素之一,其单质及化合物具有广泛用途,铜晶体中铜原子堆积模型为___________ ;铜的某种氧化物晶胞结构如图所示,若该晶体的密度为d g/cm3,阿伏加德罗常数的值为NA,则该晶胞中铜原子与氧原子之间的距离为___________ pm。(用含d和NA的式子表示)。

回答下列问题:
(1)基态铜原子的电子排布式为
(2)反应①、②中均生成有相同的气体分子,该分子的中心原子杂化类型是
(3)某学生用硫酸铜溶液与氨水做了一组实验:CuSO4溶液
 蓝色沉淀
蓝色沉淀 沉淀溶解,得到深蓝色透明溶液。写出蓝色沉淀溶于氨水的离子方程式
沉淀溶解,得到深蓝色透明溶液。写出蓝色沉淀溶于氨水的离子方程式(4)铜是第四周期最重要的过渡元素之一,其单质及化合物具有广泛用途,铜晶体中铜原子堆积模型为

您最近一年使用:0次
2016-12-09更新
|
152次组卷
|
10卷引用:2016届辽宁省五校协作体高三上学期期初考试化学试卷
13-14高三·湖北武汉·开学考试
名校
解题方法
5 . 氮的化合物在无机化工领域有着重要的地位。请回答下列问题:
(1)基态氮原子的价电子排布图为___________ 。
(2)氮的最高价氧化物为无色晶体,它由两种离子构成:已知其阴离子构型为平面正三角形,则其阳离子的构型为___________ 形,阳离子中氮的杂化方式为___________ 。
(3)某氮铝化合物X具有耐高温、抗冲击、导热性好等优良性质,广泛用于陶瓷工业等领域。工业上用氮气、氧化铝和碳在一定条件下反应生成CO和X (X的晶体结构如图所示),工业制备X的化学方程式为___________ 。
(4)X晶体中包含的化学键类型为___________(填字母标号)。
(5)已知氮化硼与X晶体类型相同,且氮化硼的熔点比X高,其原因是___________ 。
(6)若X的密度为ρg/cm3,则晶体中最近的两个Al原子的距离为___________ cm (阿伏加德罗常数用 NA表示,不必化简)。

(1)基态氮原子的价电子排布图为
(2)氮的最高价氧化物为无色晶体,它由两种离子构成:已知其阴离子构型为平面正三角形,则其阳离子的构型为
(3)某氮铝化合物X具有耐高温、抗冲击、导热性好等优良性质,广泛用于陶瓷工业等领域。工业上用氮气、氧化铝和碳在一定条件下反应生成CO和X (X的晶体结构如图所示),工业制备X的化学方程式为
(4)X晶体中包含的化学键类型为___________(填字母标号)。
| A.离子键 | B.共价键 | C.配位键 | D.金属键 |
(6)若X的密度为ρg/cm3,则晶体中最近的两个Al原子的距离为

您最近一年使用:0次
2016-12-09更新
|
524次组卷
|
4卷引用:2015届湖北省武汉市部分学校新高三起点调研测试化学试卷
(已下线)2015届湖北省武汉市部分学校新高三起点调研测试化学试卷2015届上海市青浦区高考二模化学试卷2017届广东省惠州市高三上学期调研一化学试卷广东省汕头市金山中学2018届高三摸底考试理科综合化学试题
6 . 周期表前四周期的元素a、b、c、d、e原子序数依次增大。a的核外电子总数与其周期数相同,b的价电子层中的未成对电子有3个,c的最外层电子数为其内层电子数的3倍,d与c同族;e的最外层只有1个电子,但次外层有18个电子。
回答下列问题:
(1)b、c、d中第一电离能最大的是____________ (填元素符号),e的价层电子排布图为_________ 。
(2)a和其他元素形成的二元共价化合物中,分子呈三角锥形,该分子的中心原子的杂化方式为_________ ;分子中既含有极性共价键、又含有非极性共价键的化合物是__________ (填化学式,写出两种)。
(3)这些元素形成的含氧酸中,分子的中心原子的价层电子对数为3的酸是_________ (任写一种);酸根呈三角锥结构的酸是___________ (填化学式)。
(4)e和c形成的一种离子化合物的晶体结构如图1所示,则e离子的电荷为__________ 。
(5)这5种元素形成的一种1:1型离子化合物中,阴离子呈四面体结构;阳离子呈轴向狭长的八面体结构(如图2所示)。该化合物中,阴离子为__________ ,阳离子中存在的化学键类型有____________ ;该化合物加热时首先失去的组分是____________ ,判断理由是___________________ 。


回答下列问题:
(1)b、c、d中第一电离能最大的是
(2)a和其他元素形成的二元共价化合物中,分子呈三角锥形,该分子的中心原子的杂化方式为
(3)这些元素形成的含氧酸中,分子的中心原子的价层电子对数为3的酸是
(4)e和c形成的一种离子化合物的晶体结构如图1所示,则e离子的电荷为
(5)这5种元素形成的一种1:1型离子化合物中,阴离子呈四面体结构;阳离子呈轴向狭长的八面体结构(如图2所示)。该化合物中,阴离子为


您最近一年使用:0次
2016-12-09更新
|
4357次组卷
|
8卷引用:广西钦州市钦州港经济技术开发区中学2018届高三上学期开学考试化学试题
2014·广东惠州·一模
名校
7 . 北大和中科院已成功研制出碱金属与C60形成的球碳盐K3C60,实验测知该物质属于离子晶体,具有良好的超导性。有关分析正确的是
| A.K3C60中只有离子键 | B.K3C60中碳元素显-3价 |
| C.该晶体在熔融状态下能导电 | D.该晶体熔点较低 |
您最近一年使用:0次
8 . A~G是前四周期除稀有气体之外原子序数依次增大的七种元素。A与其他元素既不同周期又不同族;B、C的价电子层中未成对电子数都是2;E核外的s、p能级的电子总数相等;F与E同周期且第一电离能比E小;G的+1价离子(G+)的各层电子全充满。回答下列问题:
(1)写出元素名称:B_______ ,G_______ 。
(2)写出F的价电子排布图:_______ 。
(3)写出化合物BC的结构式:__________________ 。
(4)由A、C、F三元素形成的离子[F(CA)4]— 是F在水溶液中的一种存在形式,其中F的杂化类型是________________ 。
(5)在测定A、D形成的化合物的相对分子质量时,实验测定值一般高于理论值的主要原因是______________________ 。
(6)E的一种晶体结构如图甲,则其一个晶胞中含有_______ 个E;G与D形成的化合物的晶胞结构如图乙,若晶体密度为ag/cm3,则G与D最近的距离为____ pm
(阿伏加德罗常数用NA表示,列出计算表达式,不用化简;乙中○为G,●为D。)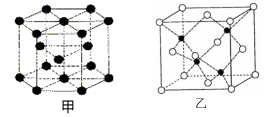
(1)写出元素名称:B
(2)写出F的价电子排布图:
(3)写出化合物BC的结构式:
(4)由A、C、F三元素形成的离子[F(CA)4]— 是F在水溶液中的一种存在形式,其中F的杂化类型是
(5)在测定A、D形成的化合物的相对分子质量时,实验测定值一般高于理论值的主要原因是
(6)E的一种晶体结构如图甲,则其一个晶胞中含有
(阿伏加德罗常数用NA表示,列出计算表达式,不用化简;乙中○为G,●为D。)

您最近一年使用:0次
2016-12-09更新
|
888次组卷
|
5卷引用:云南省元阳县第一中学2020届高三上学期开学考试化学试题
云南省元阳县第一中学2020届高三上学期开学考试化学试题云南省凤庆县一中2020届高三上学期开学考试理综化学试题(已下线)2014届吉林省吉林市高三下学期第二次模拟考试理综化学试卷(已下线)2013-2014湖南省怀化市高三第三次模拟考试理综化学试卷贵州省平塘县民族中学2020届高三上学期开学考试(理综)化学试题
9 . 已知某化合物是由钙、钛、氧三种元素组成的晶体,其晶胞结构如图所示,则该物质的化学式为
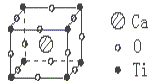

| A.CaTiO3 | B.CaTiO6 | C.Ca4TiO3 | D.CaTiO12 |
您最近一年使用:0次
名校
10 . 氮化碳结构如下图所示,其硬度超过金刚石晶体,成为首屈一指的超硬新材料。下列有关氮化碳的说法不 正确的是 ( )
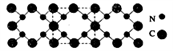

| A.氮化碳属于原子晶体 |
| B.氮化碳中碳显-4价,氮显+3价 |
| C.氮化碳的化学式为C3N4 |
| D.每个碳原子与四个氮原子相连,每个氮原子与三个碳原子相连 |
您最近一年使用:0次
2016-12-09更新
|
1095次组卷
|
14卷引用:山西省太原市阳曲县第一中学2019-2020学年高二5月复学检测化学试题
山西省太原市阳曲县第一中学2019-2020学年高二5月复学检测化学试题2014-2015学年浙江省衢州第二中学高二上学期期中化学试卷【全国百强校】广东省中山市第一中学2017-2018学年高二下学期第二次段考化学试题上海市大同中学2019—2020学年第一学期高三化学期中测试2020届高三化学二轮物质结构题型专攻—— 均摊法及晶体的相关计算【选择专练】辽宁省凌源市第二高级中学2019-2020学年高二第四次网上测试化学试题(人教版2019)选择性必修2 第三章 晶体结构与性质 第二节 分子晶体与共价晶体鲁科版2019选择性必修2第3章综合检测卷(人教版2019)选择性必修2 第三章 晶体结构与性质 综合检测卷(人教版2019)选择性必修2 第三章 晶体结构与性质 第二节 分子晶体与共价晶体 课时2 共价晶体北京市丰台区2021-2022学年高二下学期期中联考化学试题(A卷)江苏省苏州市2021-2022学年高二上学期期末模块测评化学试题山西省太原市英才学校2022-2023学年高二下学期3月阶段测试化学试题北京市大兴区第一中学2023-2024学年高二下学期3月月考化学试题



