1 . (1)1mol金刚石中有___ molC—C键,1mol二氧化硅中含有___ molSi—O键。
(2)N2H4的电子式为___ 。
(3)有机物乙醇和乙酸都可以和水互溶的原因是:___ 。
(2)N2H4的电子式为
(3)有机物乙醇和乙酸都可以和水互溶的原因是:
您最近一年使用:0次
2 . 碳元素的单质有多种形式,如图依次是C60、石墨和金刚石的结构图:回答下列问题:

(1)C60属于__ 晶体(填“金属”、“分子”或“原子”,下同),金刚石属于__ 晶体。
(2)在金刚石晶体中,碳原子数与化学键数之比为__ 。
(3)石墨晶体中,层内C—C键的键长为142pm,而金刚石中C—C键的键长为154pm。推测金刚石的熔点___ (填“>”“<”或“=”)石墨的熔点。

(1)C60属于
(2)在金刚石晶体中,碳原子数与化学键数之比为
(3)石墨晶体中,层内C—C键的键长为142pm,而金刚石中C—C键的键长为154pm。推测金刚石的熔点
您最近一年使用:0次
解题方法
3 . 填写下列空格:
(1)写出正丁烷的结构简式_______ 。
(2)金刚石的晶体类型_______ 。
(3)下述属于取代反应的是_______ ;属于加成反应的是_______ 。
A.乙烯使溴水褪色 B.乙烯使酸性高锰酸钾溶液褪色
C.苯与浓硝酸制硝基苯 D.乙醇与金属钠反应
(1)写出正丁烷的结构简式
(2)金刚石的晶体类型
(3)下述属于取代反应的是
A.乙烯使溴水褪色 B.乙烯使酸性高锰酸钾溶液褪色
C.苯与浓硝酸制硝基苯 D.乙醇与金属钠反应
您最近一年使用:0次
解题方法
4 . 硼镍镧合金具有很强的储氢能力。
(1)用价层电子对互斥理论推测三氟化硼分子的立体构型为_______ ,硼原子的杂化类型为_______ 。
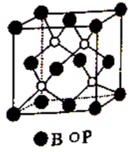
(2)磷化硼是一种受到高度关注的耐磨涂料,它可用作金属的表面保护层。如图是磷化硼晶体的晶胞示意图,该晶体的晶体类型是_______ 。
(3)硼酸(H3BO3)是一种片层状结构的白色晶体,层内的H3BO3分子间通过氢键相连,硼酸溶于水生成弱电解质一水合硼酸B(OH)3·H2O,它电离生成少量[B(OH)4]-和H+,[B(OH)4]-含有的化学键类型为_______ 。
(4)镧镍合金、铜钙合金及铈钴合金都具有相同类型的晶胞结构,写出铜原子的基态原子核外电子排布式_______ 。
(1)用价层电子对互斥理论推测三氟化硼分子的立体构型为
(2)磷化硼是一种受到高度关注的耐磨涂料,它可用作金属的表面保护层。如图是磷化硼晶体的晶胞示意图,该晶体的晶体类型是

(3)硼酸(H3BO3)是一种片层状结构的白色晶体,层内的H3BO3分子间通过氢键相连,硼酸溶于水生成弱电解质一水合硼酸B(OH)3·H2O,它电离生成少量[B(OH)4]-和H+,[B(OH)4]-含有的化学键类型为
(4)镧镍合金、铜钙合金及铈钴合金都具有相同类型的晶胞结构,写出铜原子的基态原子核外电子排布式
您最近一年使用:0次
5 . 氮的化合物在无机化工领域有着重要的地位。请回答下列问题:
(1)基态氮原子的电子排布式为_______ 。
(2)某氮铝化合物X具有耐高温、抗冲击、导热性好等优良性质,广泛用于陶瓷工业等领域。工业上用氮气、氧化铝和碳在高温条件下反应生成CO和X (X的晶体结如图所示),工业制备X的化学方程式为_____ 。

(3)X晶体中包含的化学键类型为_______ (填字母标号)。
A.离子键 B.共价键 C.配位键 D.金属键
(4)已知氮化硼与X晶体类型相同,且氮化硼的熔点比X高,其原因是_______ 。
(5)若X的密度为ρg/cm3,则晶体中最近的两个Al原子的距离为_______ cm (阿伏加德罗常数用 NA表示,不必化简)。
(1)基态氮原子的电子排布式为
(2)某氮铝化合物X具有耐高温、抗冲击、导热性好等优良性质,广泛用于陶瓷工业等领域。工业上用氮气、氧化铝和碳在高温条件下反应生成CO和X (X的晶体结如图所示),工业制备X的化学方程式为

(3)X晶体中包含的化学键类型为
A.离子键 B.共价键 C.配位键 D.金属键
(4)已知氮化硼与X晶体类型相同,且氮化硼的熔点比X高,其原因是
(5)若X的密度为ρg/cm3,则晶体中最近的两个Al原子的距离为
您最近一年使用:0次
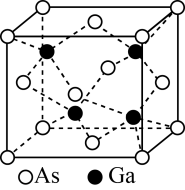
6 . GaAs的熔点为1 238 ℃,密度为ρ g·cm-3,其晶胞结构如图所示。该晶体的类型为___________ ,Ga与As以___________ 键键合。Ga和As的摩尔质量分别为MGa g·mol-1和MAs g·mol-1,原子半径分别为rGa pm和rAs pm,阿伏加德罗常数值为NA,则GaAs晶胞中原子的体积占晶胞体积的百分率为___________ 。

您最近一年使用:0次
2020·浙江宁波·一模
7 . (1)已知酸性H2CO3>HClO> ,用一个离子方程式表示ClO-和
,用一个离子方程式表示ClO-和 结合H+的相对强弱
结合H+的相对强弱___________ 。
(2) NaNH2是离子化合物,各原子均满足稳定结构。写出NaNH2的电子式___________ 。
(3)在常压下,金刚石的硬度比足球烯(C60) 高。主要原因是___________ 。
 ,用一个离子方程式表示ClO-和
,用一个离子方程式表示ClO-和 结合H+的相对强弱
结合H+的相对强弱(2) NaNH2是离子化合物,各原子均满足稳定结构。写出NaNH2的电子式
(3)在常压下,金刚石的硬度比足球烯(C60) 高。主要原因是
您最近一年使用:0次
解题方法
8 . (1)  在30℃时生成一硝基取代产物,而
在30℃时生成一硝基取代产物,而 在60℃时生成一硝基取代产物。两者反应温度不同的主要原因是
在60℃时生成一硝基取代产物。两者反应温度不同的主要原因是_____________ 。
(2)NH2Cl中各原子均满足电子稳定结构。写出NH2Cl的电子式:___________ 。
(3)二氧化碳晶体硬度很小,而二氧化硅晶体的硬度很大,其原因是____________ 。
 在30℃时生成一硝基取代产物,而
在30℃时生成一硝基取代产物,而 在60℃时生成一硝基取代产物。两者反应温度不同的主要原因是
在60℃时生成一硝基取代产物。两者反应温度不同的主要原因是(2)NH2Cl中各原子均满足电子稳定结构。写出NH2Cl的电子式:
(3)二氧化碳晶体硬度很小,而二氧化硅晶体的硬度很大,其原因是
您最近一年使用:0次
解题方法
9 . 现有 ①BaCl2晶体 ②金刚石 ③碘片 ④干冰 ⑤二氧化硅 ⑥氢氧化钾 ⑦钠 七种物质,请按下列要求回答(填序号):
(1)属于只含离子键的离子晶体的是______ (填序号,下同)。
(2)属于分子晶体的单质是_______ 。
(3)属于原子晶体的化合物是______ 。
(1)属于只含离子键的离子晶体的是
(2)属于分子晶体的单质是
(3)属于原子晶体的化合物是
您最近一年使用:0次
解题方法
10 . 回答下列问题。
(1)SO2与O3互为等电子体。SO2的VSEPR模型名称是_____ ,与O3分子互为等电子体的一种阴离子为(写化学式)______ 。
(2)氯化钠和氯化铯是两种不同类型的晶体结构。晶体结构不同的主要原因是______ 。
(3)SiO2 和GeO2具有类似的晶体结构,其中熔点较高的是______ (写化学式),原因是_____ 。
(4)向盛有氯化银的试管中加入氨水,沉淀溶解。请写出反应的化学方程式:______ 。
(1)SO2与O3互为等电子体。SO2的VSEPR模型名称是
(2)氯化钠和氯化铯是两种不同类型的晶体结构。晶体结构不同的主要原因是
(3)SiO2 和GeO2具有类似的晶体结构,其中熔点较高的是
(4)向盛有氯化银的试管中加入氨水,沉淀溶解。请写出反应的化学方程式:
您最近一年使用:0次



