名校
解题方法
1 . 下列说法错误的是
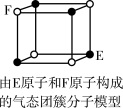
A.从CH4、 、 、 为正四面体结构,可推测PH 为正四面体结构,可推测PH 、 、 也为正四面体结构 也为正四面体结构 |
| B.1mol金刚石晶体中,平均含有2molC-C键 |
| C.水的沸点比硫化氢的高,是因为H2O分子间存在氢键,H2S分子间不能形成氢键 |
| D.某气态团簇分子结构如图所示,该气态团簇分子的分子式为EF或FE |
您最近一年使用:0次
2022-10-31更新
|
243次组卷
|
8卷引用:吉林省汪清县汪清四中2020-2021学年高二下学期期末考试化学试题
名校
解题方法
2 . 碳族中的碳、硅、锗及其化合物在多领域有重要用途。
(1)基态 的电子排布式为
的电子排布式为___________ 。
(2)我国科学家研发的“液态阳光”计划是通过太阳能发电电解水制氢,再采用高选择性催化剂将二氧化碳加氢合成甲醇。 分子中存在
分子中存在___________ 个 键和
键和___________ 个 键,
键, 分子是
分子是___________ 分子(填“极性”或“非极性”)。
(3)关于 、
、 及其化合物的结构与性质,下列论述
及其化合物的结构与性质,下列论述不正确 的是___________。
(4) 与
与 -甲基咪唑(
-甲基咪唑(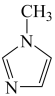 )反应可以得到
)反应可以得到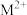 ,其结构如下图所示:
,其结构如下图所示:

 -甲基咪唑中碳原子的杂化轨道类型有
-甲基咪唑中碳原子的杂化轨道类型有___________ 。
(5)汞( )、锗(
)、锗( )、锑(
)、锑( )形成的一种新物质
)形成的一种新物质 为潜在的拓扑绝缘体材料。
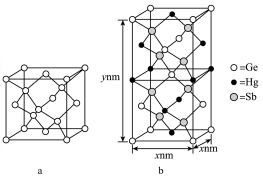
为潜在的拓扑绝缘体材料。 的晶体(晶胞为下图
的晶体(晶胞为下图 )可视为
)可视为 晶体(晶胞为下图
晶体(晶胞为下图 )中部分
)中部分 原子被
原子被 和
和 取代后形成。
取代后形成。
 的最简式的相对分子质量为
的最简式的相对分子质量为 ,阿伏加德罗常数的数值为
,阿伏加德罗常数的数值为 ,则
,则 晶体的密度为
晶体的密度为___________  (列出计算式)。注:
(列出计算式)。注:
(1)基态
 的电子排布式为
的电子排布式为(2)我国科学家研发的“液态阳光”计划是通过太阳能发电电解水制氢,再采用高选择性催化剂将二氧化碳加氢合成甲醇。
 分子中存在
分子中存在 键和
键和 键,
键, 分子是
分子是(3)关于
 、
、 及其化合物的结构与性质,下列论述
及其化合物的结构与性质,下列论述A.键能 、 、 ,因此 ,因此 稳定性小于 稳定性小于 |
B. 是与金刚石结构相似的共价晶体,因此 是与金刚石结构相似的共价晶体,因此 具有较高的硬度 具有较高的硬度 |
C. 中 中 的化合价为 的化合价为 , , 中 中 的化合价为 的化合价为 ,因此 ,因此 还原性小于 还原性小于 |
D. 原子间难形成双键和三键而 原子间难形成双键和三键而 原子间可以,是因为 原子间可以,是因为 的原子半径大于 的原子半径大于 ,因此难以形成 ,因此难以形成 键 键 |
 与
与 -甲基咪唑(
-甲基咪唑( )反应可以得到
)反应可以得到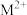 ,其结构如下图所示:
,其结构如下图所示:
 -甲基咪唑中碳原子的杂化轨道类型有
-甲基咪唑中碳原子的杂化轨道类型有(5)汞(
 )、锗(
)、锗( )、锑(
)、锑( )形成的一种新物质
)形成的一种新物质 为潜在的拓扑绝缘体材料。
为潜在的拓扑绝缘体材料。 的晶体(晶胞为下图
的晶体(晶胞为下图 )可视为
)可视为 晶体(晶胞为下图
晶体(晶胞为下图 )中部分
)中部分 原子被
原子被 和
和 取代后形成。
取代后形成。
 的最简式的相对分子质量为
的最简式的相对分子质量为 ,阿伏加德罗常数的数值为
,阿伏加德罗常数的数值为 ,则
,则 晶体的密度为
晶体的密度为 (列出计算式)。注:
(列出计算式)。注:
您最近一年使用:0次
名校
解题方法
3 . SiS2的无限长链状结构截取部分如图所示。下列说法不正确的是
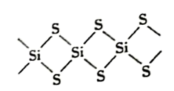

| A.92gSiS2中含有4mol共价键 | B.SiS2为原子晶体 |
| C.SiS2的熔沸点比CS2高 | D.SiS2水解产生H2S |
您最近一年使用:0次
2021-09-17更新
|
661次组卷
|
3卷引用:浙江省名校新高考研究联盟(Z20联盟)2022届高三上学期第一次联考化学试题
解题方法
4 . (1)碳可以形成CO、CO2、H2CO3等多种无机化合物。
①国家实验室成功地在高压下将CO2转化为具有类似SiO2结构的原子晶体,CO2原子晶体的晶胞如图所示,下列关于CO2的原子晶体说法正确的是_______ (填字母)。

A.CO2原子晶体的熔点比SiO2晶体低
B.1molCO2原子晶体和1molCO2分子晶体均有2mol共价键
C.在一定条件下,CO2原子晶体转化为CO2分子晶体属于化学变化
②在反应CO转化成CO2的过程中,下列说法正确的是_______ (填字母)。
A.每个分子中孤对电子数不变 B.分子极性变化 C.原子间成键方式改变
(2)氨硼烷(NH3BH3)是一种新型储氢材料,其分子中存在配位键,则氨硼烷分子结构式为_______ ,写出一种与氨硼烷互为等电子体的分子_______ (填化学式)。
(3)硼酸(B(OH)3)本身不能电离出H+,因在水中能生成[B(OH)4]-而体现弱酸性,请写出硼酸溶于水呈酸性的离子方程式_______ 。
(4)Na3OCl是一种良好的离子半导体,Na3OCl晶体属于立方晶系,晶胞结构如图所示,Na3OCl晶胞中,Cl位于各顶点位置,则Na位于_______ 位置(填“顶点”,“体心”或“面心”)。晶胞有两种基本要素,其中一种是原子坐标参数,表示晶胞内部各原子的相对位置,其中原子坐标参数A为(0,0,0),B为(0.5,0.5,0),则C点的原子坐标参数为_______ 。
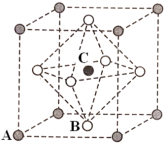

①国家实验室成功地在高压下将CO2转化为具有类似SiO2结构的原子晶体,CO2原子晶体的晶胞如图所示,下列关于CO2的原子晶体说法正确的是

A.CO2原子晶体的熔点比SiO2晶体低
B.1molCO2原子晶体和1molCO2分子晶体均有2mol共价键
C.在一定条件下,CO2原子晶体转化为CO2分子晶体属于化学变化
②在反应CO转化成CO2的过程中,下列说法正确的是
A.每个分子中孤对电子数不变 B.分子极性变化 C.原子间成键方式改变
(2)氨硼烷(NH3BH3)是一种新型储氢材料,其分子中存在配位键,则氨硼烷分子结构式为
(3)硼酸(B(OH)3)本身不能电离出H+,因在水中能生成[B(OH)4]-而体现弱酸性,请写出硼酸溶于水呈酸性的离子方程式
(4)Na3OCl是一种良好的离子半导体,Na3OCl晶体属于立方晶系,晶胞结构如图所示,Na3OCl晶胞中,Cl位于各顶点位置,则Na位于


您最近一年使用:0次
2021-04-30更新
|
233次组卷
|
2卷引用:福建省龙岩市长汀、连城、上杭、武平、漳平、永定六校(一中)2020-2021学年高二下学期期中联考化学试题
5 . 据古籍《燕闲清赏笺》记载:“宣窑之青,乃苏勃泥青”,说明宣德时期青花瓷使用的颜料是“苏勃泥青”,它是从一种钻毒砂[主要成分:( ,
, )
) ]中提取出来的。回答下列问题:
]中提取出来的。回答下列问题:
(1)基态S原子的价层电子排布图为_______ ,其原子核外电子共有_______ 种空间运动状态。
(2)比较元素第一电离能:S_______ P(填“>”、“<”或=)。
(3) 位于周期表的第
位于周期表的第_______ 周期 _______ 族,_______ (填“d”或“ds”)区。
(4)区分晶体与非晶体最可靠的科学方法是_______ 。
(5)砷化镓晶胞结构如图所示。晶胞中 与周围最近且等距的
与周围最近且等距的 形成的空间结构为
形成的空间结构为_______ 。已知 晶胞棱长为apm,其密度
晶胞棱长为apm,其密度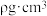 ,则阿伏加德罗常数的数值为
,则阿伏加德罗常数的数值为_______ (列出计算式即可, 的摩尔质量为
的摩尔质量为 )。
)。

(6) 的熔点为
的熔点为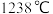 ,
, 与
与 晶体类型相同,
晶体类型相同, 的熔点
的熔点_______ (填“>”、“<”或“=”)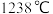 。
。
 ,
, )
) ]中提取出来的。回答下列问题:
]中提取出来的。回答下列问题:(1)基态S原子的价层电子排布图为
(2)比较元素第一电离能:S
(3)
 位于周期表的第
位于周期表的第(4)区分晶体与非晶体最可靠的科学方法是
(5)砷化镓晶胞结构如图所示。晶胞中
 与周围最近且等距的
与周围最近且等距的 形成的空间结构为
形成的空间结构为 晶胞棱长为apm,其密度
晶胞棱长为apm,其密度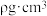 ,则阿伏加德罗常数的数值为
,则阿伏加德罗常数的数值为 的摩尔质量为
的摩尔质量为 )。
)。
(6)
 的熔点为
的熔点为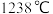 ,
, 与
与 晶体类型相同,
晶体类型相同, 的熔点
的熔点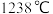 。
。
您最近一年使用:0次



