12-13高二上·四川遂宁·期中
名校
解题方法
1 . 下列说法错误的是
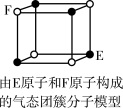
A.从CH4、 、 、 为正四面体结构,可推测PH 为正四面体结构,可推测PH 、 、 也为正四面体结构 也为正四面体结构 |
| B.1mol金刚石晶体中,平均含有2molC-C键 |
| C.水的沸点比硫化氢的高,是因为H2O分子间存在氢键,H2S分子间不能形成氢键 |
| D.某气态团簇分子结构如图所示,该气态团簇分子的分子式为EF或FE |
您最近一年使用:0次
2022-10-31更新
|
243次组卷
|
8卷引用:2012-2013学年四川省遂宁二中高二上学期期中考试化学试卷
名校
解题方法
2 . 生命起源假说认为,在地球生命形成初期(约36亿年前),由NH3、CO、H2O、H2、H2S等小分子在放电条件下形成了多种氨基酸,继而合成了蛋白质而形成单细胞。
(1)写出基态S原子的价电子排布式____ ,其基态原子具有____ 种不同能量的电子。
(2)H2S的沸点低于H2O的沸点,其原因是____ 。
(3)NH3的VSEPR模型名称为____ ,H2O分子中孤对电子占据2个____ 杂化轨道。
(4)太阳能电池种类繁多,如铜铟镓硒镍薄膜太阳能电池等。1molNi(CO)4中π键与σ键的个数比为____ 。高温下CuO容易转化为Cu2O,试从原子结构角度解释原因:____ 。
(5)①金刚石的晶胞如图,其中C原子的配位数是____ ;晶体硅、金刚砂(SiC)的结构与之相似,则金刚石、晶体硅、金刚砂的熔点由高到低的排列顺序是____ (用化学式表示);

②金刚石的晶胞参数为a pm。 1cm3晶体的平均质量为___ g(只要求列出算式,阿伏加德罗常数值为NA)
(1)写出基态S原子的价电子排布式
(2)H2S的沸点低于H2O的沸点,其原因是
(3)NH3的VSEPR模型名称为
(4)太阳能电池种类繁多,如铜铟镓硒镍薄膜太阳能电池等。1molNi(CO)4中π键与σ键的个数比为
(5)①金刚石的晶胞如图,其中C原子的配位数是

②金刚石的晶胞参数为a pm。 1cm3晶体的平均质量为
您最近一年使用:0次
2020-11-20更新
|
543次组卷
|
2卷引用:四川省遂宁市2021届高三零诊考试理综化学试题
名校
解题方法
3 . 下面是C60、金刚石、二氧化碳和S8分子的模型。


请回答下列问题:
(1)硅与碳同主族,写出硅原子基态时的核外电子排布式:_________ 。
(2)从晶体类型来看,C60属于_________ 晶体。
(3)二氧化硅结构跟金刚石结构相似,即二氧化硅的结构相当于在硅晶体结构中每个硅与硅的化学键之间插入一个O原子。观察图乙中金刚石的结构,分析二氧化硅的空间网状结构中,Si、O原子形成的最小环上有________ 个原子;晶体硅中硅原子与共价键的个数比为__________ 。
(4)图丙是二氧化碳的晶胞模型,图中显示出的二氧化碳分子数为14个。实际上一个二氧化碳晶胞中含有________ 个二氧化碳分子,二氧化碳分子中 键与
键与 键的个数比为
键的个数比为 _______ 。
(5)S单质的常见形式为S8,其环状结构如上图所示,S原子采用的轨道杂化方式是______ ;
(6)Se和S同主族,H2Se的热稳定性比H2S_________ (填“强”或“弱”)。气态SeO3分子的立体构型为_________________ 。
(7) H2SO4比 H2SO3酸性强的原因是______


请回答下列问题:
(1)硅与碳同主族,写出硅原子基态时的核外电子排布式:
(2)从晶体类型来看,C60属于
(3)二氧化硅结构跟金刚石结构相似,即二氧化硅的结构相当于在硅晶体结构中每个硅与硅的化学键之间插入一个O原子。观察图乙中金刚石的结构,分析二氧化硅的空间网状结构中,Si、O原子形成的最小环上有
(4)图丙是二氧化碳的晶胞模型,图中显示出的二氧化碳分子数为14个。实际上一个二氧化碳晶胞中含有
 键与
键与 键的个数比为
键的个数比为 (5)S单质的常见形式为S8,其环状结构如上图所示,S原子采用的轨道杂化方式是
(6)Se和S同主族,H2Se的热稳定性比H2S
(7) H2SO4比 H2SO3酸性强的原因是
您最近一年使用:0次
名校
解题方法
4 . 如图所示,NaCl是一种重要的化工原料,可以制备一系列物质。以下是钠法(液氨法)制备NaN3的工艺流程:

(1)工业可通过电解熔融NaCl制得金属钠,请写出电解时阳极的电极反应式:____ 。
(2)用电子式表示NH3分子的形成过程____ 。
(3)工业上在210-220℃合成NaN3,请写出该合成反应的化学方程式____ 。
(4)NaN3是一种易溶于水、有爆炸性的白色固体,销毁NaN3可用NaClO溶液,该销毁反应的离子方程式为____ ( 被氧化为N2)。
被氧化为N2)。
(5)生成过程中产生的Cl2、H2用途广泛,其中可用于生产高纯硅。
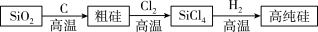
①硅元素位于周期表第____ 周期____ 族。
②SiO2熔点1723℃,质地硬而脆;SiCl4常温下为液体,易挥发。请根据性质推断SiO2属于____ 晶体,SiCl4晶体微粒间的作用力为____ 。

(1)工业可通过电解熔融NaCl制得金属钠,请写出电解时阳极的电极反应式:
(2)用电子式表示NH3分子的形成过程
(3)工业上在210-220℃合成NaN3,请写出该合成反应的化学方程式
(4)NaN3是一种易溶于水、有爆炸性的白色固体,销毁NaN3可用NaClO溶液,该销毁反应的离子方程式为
 被氧化为N2)。
被氧化为N2)。(5)生成过程中产生的Cl2、H2用途广泛,其中可用于生产高纯硅。

①硅元素位于周期表第
②SiO2熔点1723℃,质地硬而脆;SiCl4常温下为液体,易挥发。请根据性质推断SiO2属于
您最近一年使用:0次
名校
解题方法
5 . (1)氯酸钾熔化,粒子间克服了________ 的作用力;二氧化硅熔化,粒子间克服了________ 的作用力;碘的升华,粒子间克服了________ 的作用力。三种晶体的熔点由高到低的顺序是______ (填化学式)。
(2)下列六种晶体:①CO2,②NaCl,③Na,④Si,⑤CS2,⑥金刚石,它们的熔点从低到高的顺序为________ (填序号)。
(3)在H2、(NH4)2SO4、SiC、CO2、HF中,由极性键形成的非极性分子是________ ,由非极性键形成的非极性分子是________ ,能形成分子晶体的物质是________ ,含有氢键的晶体的化学式是__________ ,属于离子晶体的是_________ ,属于原子晶体的是_______ ,五种物质的熔点由高到低的顺序是__________ 。
(4)A、B、C、D为四种晶体,性质如下:
A 固态时能导电,能溶于盐酸
B 能溶于CS2,不溶于水
C 固态时不导电,液态时能导电,可溶于水
D 固态、液态时均不导电,熔点为3 500℃
试推断它们的晶体类型:
A.______ ;B.______ ;C.________ ;D._____ 。
(5)相同压强下,部分元素氟化物的熔点见下表:
试解释上表中氟化物熔点差异的原因:__________
(6)镍粉在CO中低温加热,生成无色挥发性液态Ni(CO)4,呈四面体构型。150 ℃时,Ni(CO)4分解为Ni和CO。Ni(CO)是________ 晶体,Ni(CO)4易溶于下列________ (填序号)
a 水 b 四氯化碳 c 苯 d 硫酸镍溶液
(2)下列六种晶体:①CO2,②NaCl,③Na,④Si,⑤CS2,⑥金刚石,它们的熔点从低到高的顺序为
(3)在H2、(NH4)2SO4、SiC、CO2、HF中,由极性键形成的非极性分子是
(4)A、B、C、D为四种晶体,性质如下:
A 固态时能导电,能溶于盐酸
B 能溶于CS2,不溶于水
C 固态时不导电,液态时能导电,可溶于水
D 固态、液态时均不导电,熔点为3 500℃
试推断它们的晶体类型:
A.
(5)相同压强下,部分元素氟化物的熔点见下表:
| 氟化物 | NaF | MgF2 | SiF4 |
| 熔点/℃ | 1266 | 1534 | 183 |
试解释上表中氟化物熔点差异的原因:
(6)镍粉在CO中低温加热,生成无色挥发性液态Ni(CO)4,呈四面体构型。150 ℃时,Ni(CO)4分解为Ni和CO。Ni(CO)是
a 水 b 四氯化碳 c 苯 d 硫酸镍溶液
您最近一年使用:0次
6 . 有一应用前景广阔的纳米材料甲,其由A、B两种短周期非金属元素组成,难溶于水,且硬度大,熔点高。取材料甲与熔融的烧碱反应,生成一种含A元素的含氧酸盐乙和一种含B元素的气体丙,丙能使湿润的红色石蕊试纸变蓝;乙能溶于水,加盐酸产生白色沉淀,盐酸过量沉淀不溶解。
(1)甲的化学式为____________ ,其晶体属于____________ 晶体。
(2)乙的水溶液可以用来做________________________ (写出一种用途)。
(3)B元素的一种氢化物丁,相对分子质量为32,常温下为液体,其燃烧放热多且燃烧产物对环境无污染,因此可用作火箭燃料、燃料电池燃料等。则
①丁的电子式为_____ 。
②丁可由次氯酸钠与过量氨气反应制得,其化学方程式________________________ 。
甲的制备过程中氨气需要过量的理由是____________________________________ 。
③丁的水溶液呈弱碱性,室温下其电离常数K1≈1.0×10-6,则0.01 mol·L-1丁水溶液的pH等于____________ (忽略丁的二级电离和H2O的电离)。
(1)甲的化学式为
(2)乙的水溶液可以用来做
(3)B元素的一种氢化物丁,相对分子质量为32,常温下为液体,其燃烧放热多且燃烧产物对环境无污染,因此可用作火箭燃料、燃料电池燃料等。则
①丁的电子式为
②丁可由次氯酸钠与过量氨气反应制得,其化学方程式
甲的制备过程中氨气需要过量的理由是
③丁的水溶液呈弱碱性,室温下其电离常数K1≈1.0×10-6,则0.01 mol·L-1丁水溶液的pH等于
您最近一年使用:0次
2019-09-06更新
|
249次组卷
|
2卷引用:浙江省浙南名校联盟2018-2019学年高二下学期期末考试化学试题
名校
解题方法
7 . 结构决定性质,研究物质的组成、结构对于学习物质的性质至关重要。
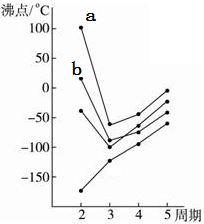
(1)如图中每条折线表示周期表ⅣA~ⅦA族中的某一族元素氢化物的沸点变化,每个小黑点代表一种氢化物,其中a点、b点分别代表的是___________ 、___________ (写化学式),a比b的沸点高的原因是__________________________________ 。
(2)在超高压下,科学家用激光器将CO2加热到1800K,成功制得了类似石英的CO2原子晶体。由此推测该CO2晶体中O—C—O键角为__________ ,与石英相比该晶体的熔点、沸点________ (“更高”或“更低”),理由是_________________________________ 。
(3)利用铜萃取剂M可通过如下反应实现铜离子的富集:

①M所含元素的电负性由大到小顺序为____ ,其中氮原子以__ 轨道与氧原子形成σ键。
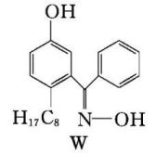
②M与W(右图)相比,M的水溶性较小,更利于Cu2+的萃取。M水溶性较小的主要原因是___________________________________ 。
(4)常用 表示分子中的大π键,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,例如苯分子中的大π键可表示为
表示分子中的大π键,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,例如苯分子中的大π键可表示为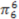 。已知吡咯(下图)中的各个原子均在同一平面内且吡咯分子中也含有大π键,请问:吡咯分子中的大π键应表示为
。已知吡咯(下图)中的各个原子均在同一平面内且吡咯分子中也含有大π键,请问:吡咯分子中的大π键应表示为________ ,吡咯分子中N原子的杂化类型为 ________ ,1mol吡咯分子中所含的σ键数目为________ 。

(1)如图中每条折线表示周期表ⅣA~ⅦA族中的某一族元素氢化物的沸点变化,每个小黑点代表一种氢化物,其中a点、b点分别代表的是

(2)在超高压下,科学家用激光器将CO2加热到1800K,成功制得了类似石英的CO2原子晶体。由此推测该CO2晶体中O—C—O键角为
(3)利用铜萃取剂M可通过如下反应实现铜离子的富集:


①M所含元素的电负性由大到小顺序为
②M与W(右图)相比,M的水溶性较小,更利于Cu2+的萃取。M水溶性较小的主要原因是
(4)常用
 表示分子中的大π键,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,例如苯分子中的大π键可表示为
表示分子中的大π键,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,例如苯分子中的大π键可表示为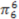 。已知吡咯(下图)中的各个原子均在同一平面内且吡咯分子中也含有大π键,请问:吡咯分子中的大π键应表示为
。已知吡咯(下图)中的各个原子均在同一平面内且吡咯分子中也含有大π键,请问:吡咯分子中的大π键应表示为
您最近一年使用:0次



