名校
解题方法
1 . 由Li、Al、Si构成的某三元化合物固态晶胞结构如图所示:

| A.晶体中Li、Al、Si三种微粒的比例为1:1:1 |
B.图中所指Si原子的坐标为( , , , , ) ) |
| C.晶体中与每个Al紧邻的Li为6个,与每个Si紧邻的Si为12个 |
| D.晶体中Al和Li构成CsCl型晶体结构,晶体中Al和Si构成金刚石型晶体结构 |
您最近一年使用:0次
2024-04-04更新
|
278次组卷
|
3卷引用:吉林省吉林地区普通高中2024届高三三模考试化学试卷
吉林省吉林地区普通高中2024届高三三模考试化学试卷2024届河北省雄安新区部分高中高三下学期三模化学试题(已下线)压轴题10?晶体结构及相关计算(5大题型+方法总结+压轴题速练)-2024年高考化学压轴题专项训练(新高考通用)
2 . 已知A、B、C、D、E和F都是元素周期表中前36号的元素,它们的原子序数依次增大。A与其他4种元素既不在同一周期又不在同一主族。B原子价电子排布式为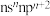 ,C和D属同一主族,E和F属同一周期,又知F是周期表中1~18列中的第13列元素。C是周期表中电负性最大的元素,C跟E可形成离子化合物其晶胞结构如图。
,C和D属同一主族,E和F属同一周期,又知F是周期表中1~18列中的第13列元素。C是周期表中电负性最大的元素,C跟E可形成离子化合物其晶胞结构如图。
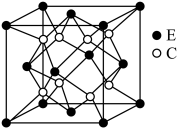
(1)元素F的符号是_____ ,基态F原子中有_____ 种能量不同的电子,其价电子轨道表示式为_____ 。
(2)C与A形成的化合物比D与A形成的化合物沸点高,其原因是_____ 。
(3)从图中可以看出,C跟E形成的离子化合物的化学式为_____ ;E离子配位数为_____ 。
(4) 是一种强氧化剂,由
是一种强氧化剂,由 和
和 在低温下合成,
在低温下合成, 分子的电子式为
分子的电子式为_____ , 是
是_____ (填“极性”或“非极性”)分子。
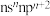 ,C和D属同一主族,E和F属同一周期,又知F是周期表中1~18列中的第13列元素。C是周期表中电负性最大的元素,C跟E可形成离子化合物其晶胞结构如图。
,C和D属同一主族,E和F属同一周期,又知F是周期表中1~18列中的第13列元素。C是周期表中电负性最大的元素,C跟E可形成离子化合物其晶胞结构如图。
(1)元素F的符号是
(2)C与A形成的化合物比D与A形成的化合物沸点高,其原因是
(3)从图中可以看出,C跟E形成的离子化合物的化学式为
(4)
 是一种强氧化剂,由
是一种强氧化剂,由 和
和 在低温下合成,
在低温下合成, 分子的电子式为
分子的电子式为 是
是
您最近一年使用:0次
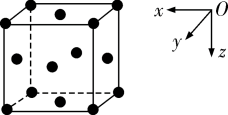
3 . 氮化铬有优异的化学稳定性和耐磨性,被广泛用作材料的涂层,某氮化铬的晶胞结构与氯化钠的相同,已知N原子在晶胞中的位置如图所示,下列说法不正确的是

A.基态Cr原子的价层电子排布式为 |
| B.距离Cr原子最近的N原子有12个 |
| C.Cr原子位于N原子构成的八面体空隙中 |
D.晶胞中Cr原子沿x轴方向的投影为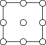 |
您最近一年使用:0次
名校
解题方法
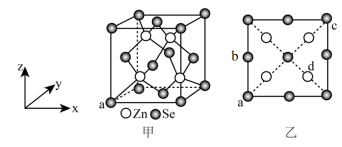
4 . 硒化锌是一种重要的半导体材料,图甲为其晶胞结构,图乙为晶胞的俯视图。已知a点的坐标(0,0,0),b点的坐标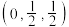 。下列说法正确的是
。下列说法正确的是
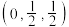 。下列说法正确的是
。下列说法正确的是
| A.Se2-的配位数为8 |
| B.基态Se核外有34种不同空间运动状态的电子 |
C.晶胞中d点原子分数坐标为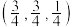 |
| D.Zn2+堆积方式也是面心立方堆积 |
您最近一年使用:0次
解题方法
5 . N-羧基丙氨酸酸酐广泛用于生物领域,用碳酸二甲酯 和丙氨酸
和丙氨酸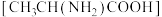 为原料可以制备N-羧基丙氨酸酸酐,其反应机理如图所示。下列说法错误的是
为原料可以制备N-羧基丙氨酸酸酐,其反应机理如图所示。下列说法错误的是
 和丙氨酸
和丙氨酸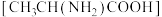 为原料可以制备N-羧基丙氨酸酸酐,其反应机理如图所示。下列说法错误的是
为原料可以制备N-羧基丙氨酸酸酐,其反应机理如图所示。下列说法错误的是
| A.在强酸性环境不利于反应进行 |
B.该过程中 元素的化合价发生改变 元素的化合价发生改变 |
C.反应过程中有 的断裂和形成 的断裂和形成 |
D.用甘氨酸 代替丙氨酸,可制得 代替丙氨酸,可制得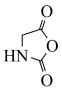 |
您最近一年使用:0次
2024-04-01更新
|
334次组卷
|
4卷引用:2024届湖南省岳阳市高三下学期第二次教学质量监测(二模)化学试题
2024届湖南省岳阳市高三下学期第二次教学质量监测(二模)化学试题(已下线)提升练03 反应历程探究与催化原理-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)东北三省四市教研联合体2024届高三下学期高考模拟(二)化学试题2024届东北三省四市教研联合体高三下学期高考模拟(二)化学试卷
名校
解题方法
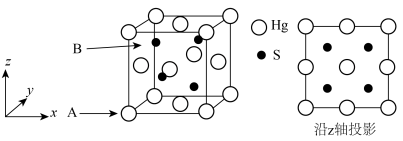
6 . 朱砂(硫化汞)在众多先秦考古遗址中均有发现,其立方晶系 型晶胞如下图所示,晶胞参数为anm,A原子的分数坐标为(0,0,0),阿伏加德罗常数的值为
型晶胞如下图所示,晶胞参数为anm,A原子的分数坐标为(0,0,0),阿伏加德罗常数的值为 ,下列说法正确的是
,下列说法正确的是
 型晶胞如下图所示,晶胞参数为anm,A原子的分数坐标为(0,0,0),阿伏加德罗常数的值为
型晶胞如下图所示,晶胞参数为anm,A原子的分数坐标为(0,0,0),阿伏加德罗常数的值为 ,下列说法正确的是
,下列说法正确的是
| A.S的配位数是6 |
B.晶胞中B原子分数坐标为(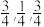 ) ) |
C.该晶体的密度是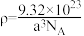 g/cm3 g/cm3 |
D.相邻两个Hg的最短距离为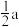 nm nm |
您最近一年使用:0次
7 . 2022年北京冬季奥运会场馆建设使用了大量不锈钢材质,不锈钢属于铁碳合金,常含铬(Cr)、镍(Ni)等元素。回答下列问题:
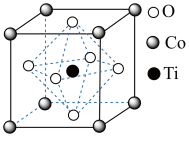
(1)某钛酸盐晶体结构模型如图所示。该晶体的化学式是_______ ,在晶体中1个Co原子周围距离最近的O原子数目为_______ 个,钛离子配位数为_______ 。
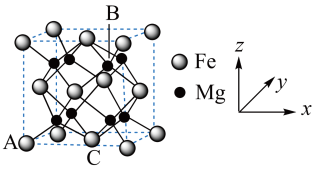
(2)铁合金用途广泛,某种铁镁合金储氢效率很高,其晶胞如图所示。晶体中每个镁原子周围距离最近的铁原子有_______ 个,该铁镁合金中原子个数比Fe:Mg=_______ ;原子坐标参数可以表示晶胞内部各原子的相对位置,其中原子坐标参数A为 ,C为
,C为 ,B点坐标参数为
,B点坐标参数为_______ 。
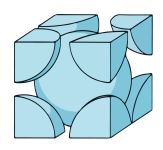
(3)金属铬晶胞如图,已知其密度为a g∙cm-3,阿伏加德罗常数的值为NA,则晶体中铬原子的半径为_______ cm(用含NA的表达式表示)。
(1)某钛酸盐晶体结构模型如图所示。该晶体的化学式是

(2)铁合金用途广泛,某种铁镁合金储氢效率很高,其晶胞如图所示。晶体中每个镁原子周围距离最近的铁原子有
 ,C为
,C为 ,B点坐标参数为
,B点坐标参数为
(3)金属铬晶胞如图,已知其密度为a g∙cm-3,阿伏加德罗常数的值为NA,则晶体中铬原子的半径为

您最近一年使用:0次
名校
解题方法
8 . 为践行社会主义核心价值观,创建和谐社会,实现碳达峰和碳中和,我国科学家独创了一种二氧化碳转化新路径:通过电催化与生物合成相结合,以二氧化碳和水为原料成功合成了葡萄糖(C6H12O6)和脂肪酸,为人工和半人工合成“粮食”提供了新路径。关于上述物质,下列说法正确的是
| A. CO2和H2O均为极性分子,故CO2易溶于水 |
| B.干冰 CO2晶体属于面心立方晶胞,晶体中一个CO2分子周围紧邻的CO2分子有12个 |
| C. H2O分子中O原子上有2对孤电子对,故H2O分子的VSEPR模型为V形 |
| D.葡萄糖由分子构成,脂肪酸由离子构成 |
您最近一年使用:0次
9 . X、Y、Z、M、N是原子序数依次增大的前四周期元素,X、M、N的最外层电子数相等,且X的价电子数和原子序数相等,M是前四周期中金属性最强的元素,N的内层轨道全充满电子,Y的基态原子中共有4种不同的空间运动状态的电子,Z是电负性最强的元素。一种由Z、M、N三种元素组成的晶体的晶胞结构如图所示,下列说法正确的是
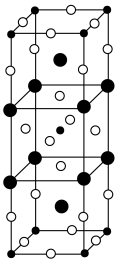

| A.原子半径:M>Z>Y>X |
| B.该晶体中N的化合价为+2 |
| C.X和Y形成的化合物的沸点低于X和Z形成的化合物的沸点 |
| D.该晶胞中N的配位数为8 |
您最近一年使用:0次
10 . 纳米材料是指在三维空间中至少有一维处于纳米尺寸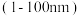 或由它们作为基本单元构成的材料。一种纳米线的制备中使用到
或由它们作为基本单元构成的材料。一种纳米线的制备中使用到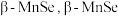 的结构中
的结构中 为面心立方最密堆积,晶胞结构如图所示。
为面心立方最密堆积,晶胞结构如图所示。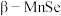 中距
中距 最近的
最近的 有
有_____ 个。
(2)若该晶体的晶胞边长为 ,阿伏加德罗常数为
,阿伏加德罗常数为 ,则
,则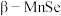 的密度为
的密度为_____ 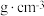 。
。
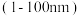 或由它们作为基本单元构成的材料。一种纳米线的制备中使用到
或由它们作为基本单元构成的材料。一种纳米线的制备中使用到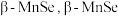 的结构中
的结构中 为面心立方最密堆积,晶胞结构如图所示。
为面心立方最密堆积,晶胞结构如图所示。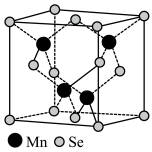
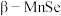 中距
中距 最近的
最近的 有
有(2)若该晶体的晶胞边长为
 ,阿伏加德罗常数为
,阿伏加德罗常数为 ,则
,则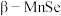 的密度为
的密度为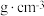 。
。
您最近一年使用:0次



