1 . 铁和硒( )都是人体所必需的微量元素,且在医药、催化、材料等领域有广泛应用,回答下列问题:
)都是人体所必需的微量元素,且在医药、催化、材料等领域有广泛应用,回答下列问题:
(1)乙烷硒啉(Ethaselen)是一种抗癌新药,其结构式如下:
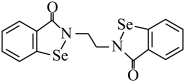
①该新药分子中有_____________ 种不同化学环境的C原子;
②比较键角大小:气态 分子
分子___________  离子(填“>”、“<”或“=”),原因是:
离子(填“>”、“<”或“=”),原因是:____________ 。
(2) 晶胞为立方体,边长为
晶胞为立方体,边长为 ,如图所示。
,如图所示。

①与 紧邻的阴离子个数为
紧邻的阴离子个数为___________ 。
②晶胞的密度为
___________  。
。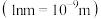
 )都是人体所必需的微量元素,且在医药、催化、材料等领域有广泛应用,回答下列问题:
)都是人体所必需的微量元素,且在医药、催化、材料等领域有广泛应用,回答下列问题:(1)乙烷硒啉(Ethaselen)是一种抗癌新药,其结构式如下:

①该新药分子中有
②比较键角大小:气态
 分子
分子 离子(填“>”、“<”或“=”),原因是:
离子(填“>”、“<”或“=”),原因是:(2)
 晶胞为立方体,边长为
晶胞为立方体,边长为 ,如图所示。
,如图所示。
①与
 紧邻的阴离子个数为
紧邻的阴离子个数为②晶胞的密度为

 。
。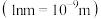
您最近一年使用:0次
2 . 已知有如图晶体结构:

下列有关晶体的叙述中,错误的是

下列有关晶体的叙述中,错误的是
A. 水分子最多可以形成 水分子最多可以形成 氢键 氢键 |
| B.金刚石晶体中碳原子所连接的最小环为六元环 |
| C.石墨晶体的二维结构,碳原子的配位数是3 |
D.在 晶体里,每个 晶体里,每个 周围有6个距离最近且相等的 周围有6个距离最近且相等的 |
您最近一年使用:0次
2023-05-08更新
|
283次组卷
|
2卷引用:浙江省北斗联盟2022-2023学年高二下学期期中联考化学试题
3 . AA705合金(含Al、Zn、Mg和Cu)被用于飞机机身和机翼、智能手机外壳上等。最近科学家将碳化钛纳米颗粒(大小仅为十亿分之一米)注入AA7075的焊丝内,这样可以更容易地连接其他难以焊接的金属和金属合金。回答下列问题:
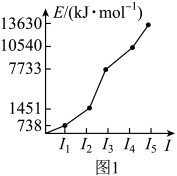
(1)第三周期某元素的前5个电子的电离能如图1所示。该元素是______ (填元素符号),判断依据是______ 。
(2)CN-、NH3、H2O和OH-等配体都能与Zn2+形成配离子。则[Zn(NH3)4]2+中心离子的配位数为______ 。
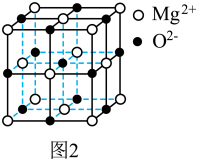
(3)氧化镁是一种熔点极高的离子晶体,结构类似NaCl,其晶胞如图2所示,该晶胞中Mg2+数目为______ ;1个O2-周围有_____ 个Mg2+最近且等距离。
(1)第三周期某元素的前5个电子的电离能如图1所示。该元素是

(2)CN-、NH3、H2O和OH-等配体都能与Zn2+形成配离子。则[Zn(NH3)4]2+中心离子的配位数为
(3)氧化镁是一种熔点极高的离子晶体,结构类似NaCl,其晶胞如图2所示,该晶胞中Mg2+数目为

您最近一年使用:0次
4 . 利用 可实现人工合成金刚石。下列关于该反应的说法错误的是
可实现人工合成金刚石。下列关于该反应的说法错误的是
 可实现人工合成金刚石。下列关于该反应的说法错误的是
可实现人工合成金刚石。下列关于该反应的说法错误的是| A.C(金刚石)属于共价晶体 |
| B.该反应利用了Na的强还原性 |
C.晶体硅和金刚石中的Si、C的杂化方式都是 |
D.NaCl晶体中每个 周围与它最接近且距离相等的 周围与它最接近且距离相等的 有12个 有12个 |
您最近一年使用:0次
名校
解题方法
5 . 某荧光材料由 与
与 组成,其摩尔质量为
组成,其摩尔质量为 ,
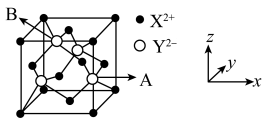
, 为阿伏加德罗常数的值。其晶胞结构如图所示。下列叙述不正确的是
为阿伏加德罗常数的值。其晶胞结构如图所示。下列叙述不正确的是
 与
与 组成,其摩尔质量为
组成,其摩尔质量为 ,
, 为阿伏加德罗常数的值。其晶胞结构如图所示。下列叙述不正确的是
为阿伏加德罗常数的值。其晶胞结构如图所示。下列叙述不正确的是
| A.该晶体的化学式是XY |
B.该晶胞参数为anm,则其晶体密度为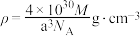 |
C. 的配位数是4, 的配位数是4, 的配位数也是4 的配位数也是4 |
D.若A点的原子坐标为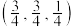 ,则B点的原子坐标为 ,则B点的原子坐标为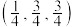 |
您最近一年使用:0次
2022-11-28更新
|
705次组卷
|
5卷引用:浙江省舟山中学2022-2023学年高三上学期首考模拟卷(三)化学试题
6 . 完成下列问题。
(1)已知气体溶解度(气体压强为 ,温度为293K,在100g水中的溶解度)数据如下表:
,温度为293K,在100g水中的溶解度)数据如下表:
结合上表信息,说明乙烷与乙炔气体的溶解度存在差异的原因:_______ 。
(2)已知乙酸( )的正交晶胞如图所示。阿伏加德罗常数为
)的正交晶胞如图所示。阿伏加德罗常数为 。
。
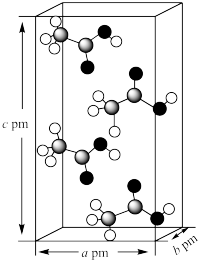
①第一电离能比C、O都大的同周期主族元素是:_______ (填元素符号)。
②乙酸晶胞的密度
_______  。
。
(3)某笼形络合物 结构中,金属离子与
结构中,金属离子与 连接形成平面层,两个平面层通过
连接形成平面层,两个平面层通过 分子连接,中间的空隙填充大小合适的分子(如
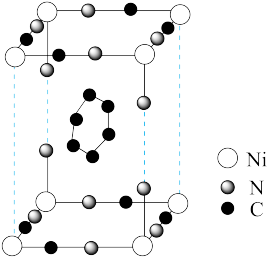
分子连接,中间的空隙填充大小合适的分子(如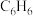 )。其基本结构如图(H原子未画出):
)。其基本结构如图(H原子未画出):
①
_______ 。
②该结构不是晶胞结构单元,理由是_______ ;
③通过分析,金属离子的配位数为_______ (填入序号)。
A.2、3 B.4、6 C.3、4 D.5、6
(1)已知气体溶解度(气体压强为
 ,温度为293K,在100g水中的溶解度)数据如下表:
,温度为293K,在100g水中的溶解度)数据如下表:| 气体 | 溶解度/g | 分子结构特点 |
| 乙烷 | 0.0062 | 中心原子 杂化,轨道半径较大,C负电性(δ-)及H正电性(δ+)不明显 杂化,轨道半径较大,C负电性(δ-)及H正电性(δ+)不明显 |
| 乙炔 | 0.117 | 中心原子sp杂化,轨道半径较小,C负电性(δ-)及H正电性(δ+)明显 |
结合上表信息,说明乙烷与乙炔气体的溶解度存在差异的原因:
(2)已知乙酸(
 )的正交晶胞如图所示。阿伏加德罗常数为
)的正交晶胞如图所示。阿伏加德罗常数为 。
。
①第一电离能比C、O都大的同周期主族元素是:
②乙酸晶胞的密度

 。
。(3)某笼形络合物
 结构中,金属离子与
结构中,金属离子与 连接形成平面层,两个平面层通过
连接形成平面层,两个平面层通过 分子连接,中间的空隙填充大小合适的分子(如
分子连接,中间的空隙填充大小合适的分子(如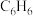 )。其基本结构如图(H原子未画出):
)。其基本结构如图(H原子未画出):
①

②该结构不是晶胞结构单元,理由是
③通过分析,金属离子的配位数为
A.2、3 B.4、6 C.3、4 D.5、6
您最近一年使用:0次
名校
解题方法
7 . 锂是高能电池的理想负极,常用乙腈、二甲基甲酰胺等有机溶剂和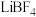 、LiBr等电解质制成锂非水电池。下列说法正确的是
、LiBr等电解质制成锂非水电池。下列说法正确的是
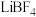 、LiBr等电解质制成锂非水电池。下列说法正确的是
、LiBr等电解质制成锂非水电池。下列说法正确的是A.乙腈(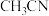 )中碳原子的杂化轨道类型为 )中碳原子的杂化轨道类型为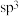 |
B.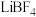 中存在离子键、共价键和配位键 中存在离子键、共价键和配位键 |
C.LiBr具有NaCl型晶体结构,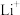 的配位数是12 的配位数是12 |
D.二甲基甲酰胺(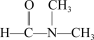 )中存在极性键和非极性键 )中存在极性键和非极性键 |
您最近一年使用:0次
2022-05-05更新
|
135次组卷
|
2卷引用:浙江省宁波市北仑中学2022-2023学年高二下学期期中考试化学试题
解题方法
8 . 下列说法正确的是
| A.中心原子是sp杂化的,其分子的空间构型一定是直线形 |
| B.在已知元素中,基态原子的4s能级中只有1个电子且位于d区的元素只有1种 |
| C.氯化钠晶体中,每个Na+周围距离最近且相等的Na+共有6个 |
| D.氢键(X—H…Y)中三原子在一条直线上时,作用力最弱 |
您最近一年使用:0次
9 . 锆( )和镉(
)和镉( )是目前光电材料广泛使用的元素。
)是目前光电材料广泛使用的元素。 和
和 的晶胞分别如图甲、图乙所示:
的晶胞分别如图甲、图乙所示:
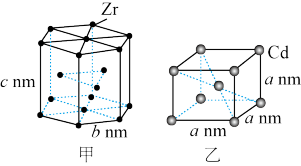
下列说法正确的是
 )和镉(
)和镉( )是目前光电材料广泛使用的元素。
)是目前光电材料广泛使用的元素。 和
和 的晶胞分别如图甲、图乙所示:
的晶胞分别如图甲、图乙所示:
下列说法正确的是
A.每个锆晶胞中含 原子个数为8 原子个数为8 |
B.在镉晶胞中两个镉原子最近核间距为  |
C.在镉晶胞中 的配位数为4 的配位数为4 |
D.锆晶体的密度为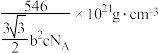 |
您最近一年使用:0次
2021-05-17更新
|
537次组卷
|
4卷引用:浙江省诸暨市海亮高级中学2021-2022学年高二上学期期中考试化学试题
浙江省诸暨市海亮高级中学2021-2022学年高二上学期期中考试化学试题湖北省2020-2021学年高三下学期新高考模拟联考化学试题(已下线)专题讲座(十二) 晶胞参数、坐标参数的分析与应用(精练)-2022年一轮复习讲练测甘肃省张掖市高台县第一中学2022-2023学年高二上学期12月月考化学试题
解题方法
10 . 下列有关说法不正确的是
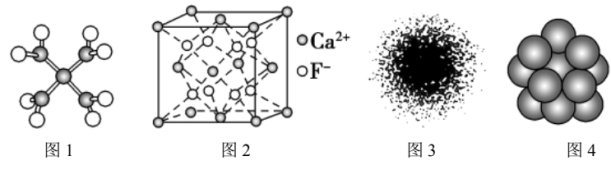

| A.四水合铜离子的模型如图1所示,1个四水合铜离子中有4个配位键 |
B. 晶体的晶胞如图2所示,设 晶体的晶胞如图2所示,设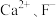 半径分别为 半径分别为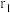 和 和 ,晶胞边长为a,则有 ,晶胞边长为a,则有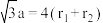 |
| C.H原子的电子云图如图3所示,H原子核外大多数电子在原子核附近运动 |
| D.金属Cu中原子堆积模型如图4所示,为最密堆积,Cu原子的配位数为12 |
您最近一年使用:0次
2021-04-16更新
|
755次组卷
|
3卷引用:第34届(2021年)高中化学奥林匹克竞赛浙江省预赛试题
第34届(2021年)高中化学奥林匹克竞赛浙江省预赛试题湖北省恩施高中、龙泉中学、宜昌一中2020-2021学年高三下学期4月联合考试化学试题(已下线)难点9 晶胞的相关计算-2021年高考化学【热点·重点·难点】专练(山东专用)



