1 . 已知图甲为金属钠的晶胞,晶胞边长为 ,其晶胞截面如图乙所示。图丙为ZnS晶胞截面,已知ZnS属立方晶体,假设晶胞边长为
,其晶胞截面如图乙所示。图丙为ZnS晶胞截面,已知ZnS属立方晶体,假设晶胞边长为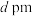 。下列关于ZnS晶胞的描述错误的是
。下列关于ZnS晶胞的描述错误的是
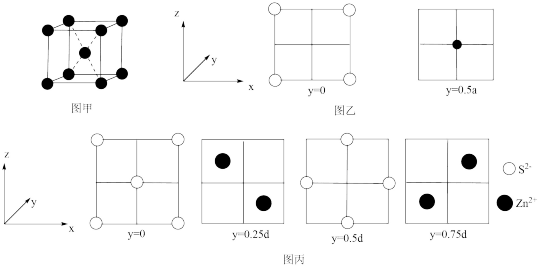
 ,其晶胞截面如图乙所示。图丙为ZnS晶胞截面,已知ZnS属立方晶体,假设晶胞边长为
,其晶胞截面如图乙所示。图丙为ZnS晶胞截面,已知ZnS属立方晶体,假设晶胞边长为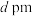 。下列关于ZnS晶胞的描述错误的是
。下列关于ZnS晶胞的描述错误的是
A.每个晶胞中含有的 数目为4 数目为4 |
B.与 距离最近且相等的 距离最近且相等的 有8个 有8个 |
C.该晶胞中两个距离最近的 和 和 的核间距的计算表达式为 的核间距的计算表达式为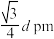 |
D.ZnS晶体的密度为 ( ( 表示阿伏加德罗常数) 表示阿伏加德罗常数) |
您最近一年使用:0次
2022-12-16更新
|
1137次组卷
|
3卷引用:辽宁省沈阳市五校协作体2022-2023学年高三上学期12月月考化学试题
解题方法
2 .  具有良好半导体性能。
具有良好半导体性能。 晶体与
晶体与 晶体的结构相似,如图给出了
晶体的结构相似,如图给出了 晶胞中的
晶胞中的 和位于晶胞体心的
和位于晶胞体心的 (
( 中的
中的 键位于晶胞体对角线上,晶胞中的其他
键位于晶胞体对角线上,晶胞中的其他 已省略)。下列有关该
已省略)。下列有关该 晶体的说法错误的是
晶体的说法错误的是

 具有良好半导体性能。
具有良好半导体性能。 晶体与
晶体与 晶体的结构相似,如图给出了
晶体的结构相似,如图给出了 晶胞中的
晶胞中的 和位于晶胞体心的
和位于晶胞体心的 (
( 中的
中的 键位于晶胞体对角线上,晶胞中的其他
键位于晶胞体对角线上,晶胞中的其他 已省略)。下列有关该
已省略)。下列有关该 晶体的说法错误的是
晶体的说法错误的是
A.一个晶胞中 的数目为2 的数目为2 | B. 的配位数为6 的配位数为6 |
| C.该晶体中存在非极性键 | D.晶胞中其他 均位于棱心 均位于棱心 |
您最近一年使用:0次
解题方法
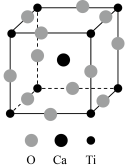
3 . 钙钛矿(CaTiO3)型化合物是一类可用于生产太阳能电池、传感器、固体电阻器等的功能材料,回答下列问题:
(1)基态Ti原子的核外电子排布式为____ 。Ti在元素周期表中的位置____ 。
(2)Ti的四卤化物熔点如表所示,TiF4熔点高于其他三种卤化物,自TiCl4至TiI4熔点依次升高,原因是____ 。
(3)CaTiO3的晶胞如图所示,其组成元素的电负性大小顺序是____ ;金属离子与氧离子间的作用力为____ ,Ca2+的配位数是____ 。
(1)基态Ti原子的核外电子排布式为
(2)Ti的四卤化物熔点如表所示,TiF4熔点高于其他三种卤化物,自TiCl4至TiI4熔点依次升高,原因是
| 化合物 | TiF4 | TiCl4 | TiBr4 | TiI4 |
| 熔点/℃ | 377 | ﹣24.12 | 38.3 | 155 |
(3)CaTiO3的晶胞如图所示,其组成元素的电负性大小顺序是

您最近一年使用:0次
名校
解题方法
4 . 某荧光材料由 与
与 组成,其摩尔质量为
组成,其摩尔质量为 ,
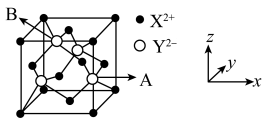
, 为阿伏加德罗常数的值。其晶胞结构如图所示。下列叙述不正确的是
为阿伏加德罗常数的值。其晶胞结构如图所示。下列叙述不正确的是
 与
与 组成,其摩尔质量为
组成,其摩尔质量为 ,
, 为阿伏加德罗常数的值。其晶胞结构如图所示。下列叙述不正确的是
为阿伏加德罗常数的值。其晶胞结构如图所示。下列叙述不正确的是
| A.该晶体的化学式是XY |
B.该晶胞参数为anm,则其晶体密度为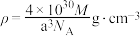 |
C. 的配位数是4, 的配位数是4, 的配位数也是4 的配位数也是4 |
D.若A点的原子坐标为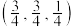 ,则B点的原子坐标为 ,则B点的原子坐标为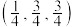 |
您最近一年使用:0次
2022-11-28更新
|
735次组卷
|
5卷引用:浙江省舟山中学2022-2023学年高三上学期首考模拟卷(三)化学试题
5 . 氧化锌常作为金属缓蚀剂,其结构有很多种,其中一种立方晶胞结构如图,晶胞边长为a 。下列说法错误的是
。下列说法错误的是

 。下列说法错误的是
。下列说法错误的是
| A.该晶体属于离子晶体 | B.O原子与O原子的最短距离为a |
C. 原子周围等距且最近的 原子周围等距且最近的 原子数为6 原子数为6 | D.该晶胞中含有4个O原子,4个 原子 原子 |
您最近一年使用:0次
6 . 完成下列问题。
(1)已知气体溶解度(气体压强为 ,温度为293K,在100g水中的溶解度)数据如下表:
,温度为293K,在100g水中的溶解度)数据如下表:
结合上表信息,说明乙烷与乙炔气体的溶解度存在差异的原因:_______ 。
(2)已知乙酸( )的正交晶胞如图所示。阿伏加德罗常数为
)的正交晶胞如图所示。阿伏加德罗常数为 。
。
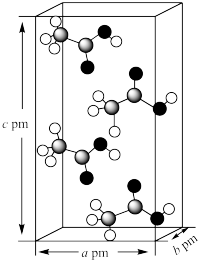
①第一电离能比C、O都大的同周期主族元素是:_______ (填元素符号)。
②乙酸晶胞的密度
_______  。
。
(3)某笼形络合物 结构中,金属离子与
结构中,金属离子与 连接形成平面层,两个平面层通过
连接形成平面层,两个平面层通过 分子连接,中间的空隙填充大小合适的分子(如
分子连接,中间的空隙填充大小合适的分子(如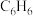 )。其基本结构如图(H原子未画出):
)。其基本结构如图(H原子未画出):
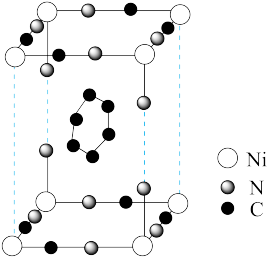
①
_______ 。
②该结构不是晶胞结构单元,理由是_______ ;
③通过分析,金属离子的配位数为_______ (填入序号)。
A.2、3 B.4、6 C.3、4 D.5、6
(1)已知气体溶解度(气体压强为
 ,温度为293K,在100g水中的溶解度)数据如下表:
,温度为293K,在100g水中的溶解度)数据如下表:| 气体 | 溶解度/g | 分子结构特点 |
| 乙烷 | 0.0062 | 中心原子 杂化,轨道半径较大,C负电性(δ-)及H正电性(δ+)不明显 杂化,轨道半径较大,C负电性(δ-)及H正电性(δ+)不明显 |
| 乙炔 | 0.117 | 中心原子sp杂化,轨道半径较小,C负电性(δ-)及H正电性(δ+)明显 |
结合上表信息,说明乙烷与乙炔气体的溶解度存在差异的原因:
(2)已知乙酸(
 )的正交晶胞如图所示。阿伏加德罗常数为
)的正交晶胞如图所示。阿伏加德罗常数为 。
。
①第一电离能比C、O都大的同周期主族元素是:
②乙酸晶胞的密度

 。
。(3)某笼形络合物
 结构中,金属离子与
结构中,金属离子与 连接形成平面层,两个平面层通过
连接形成平面层,两个平面层通过 分子连接,中间的空隙填充大小合适的分子(如
分子连接,中间的空隙填充大小合适的分子(如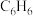 )。其基本结构如图(H原子未画出):
)。其基本结构如图(H原子未画出):
①

②该结构不是晶胞结构单元,理由是
③通过分析,金属离子的配位数为
A.2、3 B.4、6 C.3、4 D.5、6
您最近一年使用:0次
名校
7 . 火法炼铜首先要焙烧黄铜矿,其反应为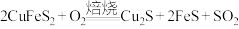 。某种产物的晶胞结构如图所示,下列说法错误的是
。某种产物的晶胞结构如图所示,下列说法错误的是

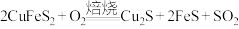 。某种产物的晶胞结构如图所示,下列说法错误的是
。某种产物的晶胞结构如图所示,下列说法错误的是
A. 为氧化剂, 为氧化剂, 既是氧化剂又是还原剂 既是氧化剂又是还原剂 |
| B.该晶胞结构图表示的是FeS |
| C.晶胞中与S紧邻的金属微粒个数为8 |
| D.每生成1mol FeS,有0.5mol硫被氧化 |
您最近一年使用:0次
8 . 高温下,超氧化钾晶体与氯化钠相似。晶体中氧的化合价可看作部分为0价,部分为-2价。下图为超氧化钾晶体的一个晶胞(晶体中最小的重复单元)。则下列说法正确的


| A.晶体中与每个K+距离最近的K+有4个 |
B.晶体中每个K+周围有8个 ,每个 ,每个 周围有8个K+ 周围有8个K+ |
C.超氧化钾的化学式为KO2,每个晶胞含有14个K+和13 个 |
| D.晶体中,0价氧原子与-2价氧原子的数目比可看作为3:1 |
您最近一年使用:0次
名校
解题方法
9 . 几种离子晶体的晶胞如图所示,下列说法正确的是
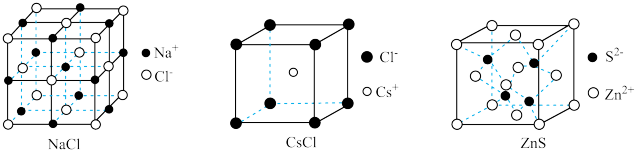

| A.熔沸点:NaCl<CsCl |
B.NaCl晶胞中, 做面心立方最密堆积, 做面心立方最密堆积, 填充正四面体空隙 填充正四面体空隙 |
C.若ZnS的晶胞边长为a pm,则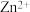 与 与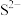 之间的最近距离为 之间的最近距离为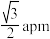 |
| D.上述三种晶胞中,阳离子的配位数:ZnS<NaCl<CsCl |
您最近一年使用:0次
名校
解题方法
10 . Wilson病是一种先天性铜代谢障碍性疾病,D-青霉胺具有排铜作用,用以治疗或控制Wilson病症。D-青霉胺结构简式如图:

回答下列问题:
(1)写出Cu的简化电子排布式_______ 。
(2)已知气态基态原子得到一个电子形成气态基态负一价离子所产生的能量变化称为该元素原子的第一电子亲合能(吸收能量为负值,释放能量为正值),试解释碳原子第一电子亲合能较大的原因_______ 。 第一电子亲合能可能为正值或负值,而第二电子亲合能均为负值,原因是_______ 。
(3)D-青霉胺中,硫原子的VSEPR模型为_______ ,碳原子的杂化方式为_______ 。
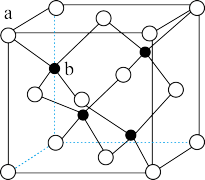
(4)青霉胺在临床治疗时对于症状改善较慢,常有并发症出现,因而近年采用锌剂(ZnSO4)替代治疗,可由硫化锌制备。立方硫化锌晶胞与金刚石晶胞类似,结构如图其中a代表S2-,b代表Zn2+。则该晶胞中S2-的配位数为_______ ,若晶体的密度为ρg·cm-3,则晶胞的体积为_______ cm3(列出计算式)。

回答下列问题:
(1)写出Cu的简化电子排布式
(2)已知气态基态原子得到一个电子形成气态基态负一价离子所产生的能量变化称为该元素原子的第一电子亲合能(吸收能量为负值,释放能量为正值),试解释碳原子第一电子亲合能较大的原因
(3)D-青霉胺中,硫原子的VSEPR模型为
(4)青霉胺在临床治疗时对于症状改善较慢,常有并发症出现,因而近年采用锌剂(ZnSO4)替代治疗,可由硫化锌制备。立方硫化锌晶胞与金刚石晶胞类似,结构如图其中a代表S2-,b代表Zn2+。则该晶胞中S2-的配位数为

您最近一年使用:0次
2022-10-23更新
|
234次组卷
|
2卷引用:海南省琼海市嘉积第三中学2021-2022学年高三下学期第三次月考化学科试题



